Стадии лечения глиобластомы
1-й этап – оперативное вмешательство
Цель операции заключается в как можно более полном полном удалении онкоочага. Последние исследования подтвердили, что наиболее полное удаление опухоли позволяет увеличить медиану продолжительности жизни и улучшает качество последующей лучевой терапии.
Если очаг имеет инфильтративный характер разрастания, оперативное устранение глиобластомы заметно затрудняется. При подобных условиях врачу трудно выявить четкие границы онкоочага, ведь он сильно сливается с близлежащими мозговыми тканями.
Чтобы опухоль все-таки можно было обнаружить, была разработана методика флуоресцентного выявления онкоклеток. В этом случае задействуется 5-аминолевулиновая кислота. Пациент выпивает раствор с данным элементом примерно за четыре часа до оперативного вмешательства.
Внутри организма рассматриваемая кислота превращается в протопорфирин, который начинает скапливаться в клеточных компонентах глиобластомы. Под особым освещением видоизмененный элемент подсвечивает онкоклетки.
Микроскоп
Во время хирургии задействуется микроскоп, оснащенный особым источником голубого света. Длина волны этого света составляет около 400 нанометров. Данный свет помогает выявить злокачественные очаги, поэтому у хирурга появляется возможность для их тщательного удаления.
До недавнего времени врачи и мечтать не могли о том, чтобы полностью удалять онкоочаг. Из-за его плохой видимости они оставляли часть опухоли нетронутой, т.к. боялись задеть здоровые ткани и вызвать дополнительные осложнения (паралич, речевые дефекты и т.д.).
2-й этап – облучение и Темодал
3-й этап – поддерживающие мероприятия с задействованием Темодала
Данный тип лечения стартует по истечении 4 недель после завершения курса лучевой обработки. Зачастую, больной проходит через 6 коротеньких курсов Темодаловой терапии. Каждый курс длится 5 суток с 23-дневными перерывами.
Если подытожить всю вышеописанную информацию, можно сделать вывод, что:
• комбинированное лечение глиобластомы, состоящее из оперативного устранения онкоочага, лучевой обработки и «химии», является стандартным во всем мире;
• частичное хирургическое удаление очага уже является устаревшей методикой;
• изолированное задействование облучения (без Темодала) имеет более низкую действенность;
• Темодал – основной участник комбинированного лечения;
• бороться с рассматриваемой патологией лучше в специализированных мед. учреждениях, имеющих солидный опыт в проведении всех вышеупомянутых процедур.
Терапия глиобластомы при помощи Авастина
Этот препарат разработали генетики. Он содержит в себе антитела к фактору разрастания, который вырабатывается эндотелием сосудов онкоформирования. Этот фактор является белковым компонентом, секретируемым глиобластомой.
Благодаря ему формируется сосудистая сетка, гарантирующая питание болезнетворного очага. Чем больше сосудов, тем быстрее прогрессирует опухоль. Авастин блокирует формирование сосудистой сетки, препятствуя прогрессированию онкоочага.
Нужно знать, что:
• Авастин задействуется при рецидивирующих формах глиобластомы;
• по сей день препарат не относится к категории средств, назначаемых в первую очередь при рецидивах;
• лекарство может прописываться в моно режиме либо в комбинации с другим средством под названием Иринотекан.
Роль Темодала
Химиотерапия Темодалом задействуется на ранних стадиях, как правило в комбинации с лучевой терапией. Методика включает 6-8 циклов по 5 суток каждый. К сожалению, такая терапия дает хороший результат лишь в 20% случаев.
При детской онкологии химия прописывается как заменитель радиационного лечения, пагубно воздействующего на развитие мозга. Данный вид терапии задействуется только после грамотного взвешивания всех его плюсов и минусов.
Курс его приема стартует по истечении 4 недель после лучевой обработки. Прием медикамента разделен на 6 коротеньких курсов длительностью по 5 суток каждый. Между курсами делается 23-дневный перерыв. Среди врачей эта схема именуется 5/28. Иными словами, лекарство употребляется 5 дней при каждом 28-суточном цикле.
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Глиобластома головного мозга
Глиобластома головного мозга – злокачественное образование, отличающееся агрессивным развитием. Редкая патология, среди онкологических больных диагностируется 1 раз на 1000 случаев. Свое начало опухоль берет в клетках головного мозга, которые называются глии. На фоне нарушения их деятельности начинается активное деление клеток, в том числе и в рядом расположенных – именно так развивается злокачественный процесс. Чаще всего глиобластома локализуется в височной и лобной частях головного мозга, но иногда диагностируется в мозжечке, спинном мозге и стволе головного мозга.
Различают 3 вида злокачественной опухоли:
Также классифицируется глиобластома на первичную и вторичную. В первом случае речь идет о стремительно развивающейся опухоли (максимум за 3 месяца до критического состояния), чаще диагностируется у мужчин старшего возраста. Вторичная глиобластома формируется из доброкачественных опухолей, чаще выявляется у женщин среднего, старшего возрастов.
Конкретных причин развития злокачественного процесса в клетках головного мозга нет, но врачи выделяют несколько провоцирующих факторов:
Симптомы, признаки глиобластомы головного мозга
Симптомы глиобластомы проявляются рано, поэтому диагностировать ее на ранней стадии не представляет трудностей. Врачи выделяют несколько первичных признаков заболевания:
По мере роста глиобластома начинает оказывать давление на определенные участки головного мозга и клиническая картина становится более расширенной. Добавляются специфические симптомы:
Сначала симптомы глиобластомы появляются периодически, больной отмечает повышенную сонливость, быструю утомляемость, понижение работоспособности. Затем признаки глиобластомы беспокоят в постоянном режиме, что означает активный рост образования.
Онкология головного мозга (глиобластома): методы диагностики
Важно выявить проблему на ранней стадии развития, тогда шансы на выздоровления повышаются в разы. Как только появляются первичные симптомы глиобластомы, стоит обратиться за помощью к специалистам для прохождения полноценного обследования. При подозрении на глиобластому врачи назначают КТ головного мозга – это современный метод лучевой диагностики. Врач сможет оценить состояние кровотока даже в самых мелких кровеносных сосудах головного мозга. Выполняется с применением контрастного вещества, которое вводится в периферическую вену.
КТ головного мозга является информативным методом диагностирования глиобластомы, потому что эта процедура:
При подозрении на опухоль головного мозга, врачи используют при обследовании пациента и другие диагностические процедуры:
Все вышеперечисленные диагностические мероприятия проводятся при выраженной клинической картине.
Лечение глиобластомы головного мозга
Если глиобластома головного мозга диагностирована на 4 стадии развития, то лечение будет нецелесообразным. Врачи назначают поддерживающую терапию, чтобы облегчить симптомы при глиобластоме и на некоторое время продлить жизнь больного. Но на остальных 3 стадиях лечение может дать отличные результаты. Чаще всего назначают:
Хирургическое вмешательство показано и на 3 стадии заболевания, но выполняется оно в качестве паллиативного лечения. Врач осуществляет шунтирование, что позволяет стабилизировать внутричерепное давление и сохранить функциональность головного мозга.
Иногда глиобластома локализуется в труднодоступных местах головного мозга и тогда врачи могут отказаться от проведения хирургического вмешательства.
Инновационный метод лечения в рамках клинического исследования.
Команда врачей НМИЦ радиологии во главе с А.Д. Каприным в составе 20 человек (нейрохирурги, анестезиологи, реаниматологи, кардиохирурги, перфузиологи сразу пяти научных медицинских институтов) провели первую в мире процедуру изолированной перфузии головного мозга пациентке с диагнозом «глиобластома». За счет особого строения и структуры тканей головного мозга опухоли данной локализации, к которым в том числе относят глиобластомы, крайне сложно поддаются лечению. Суть инновационного метода заключается в том, что во время медицинской манипуляции головной мозг кровоснабжается отдельно от тела с помощью аппарата искусственного кровообращения. На этом этапе к органу доставляются концентрированные дозы химиопрепарата, губительные для опухоли, но безопасные для самого органа. После того, как токсичность снижается, орган вновь подключается к общей системе кровообращения.
Прогнозы заболевания
Болезнь имеет крайне неблагоприятные прогнозы, хотя многое зависит от классификации глиобластомы головного мозга. Если врачами была проведена операция по удалению опухоли, то выживаемость составляет максимум 5 лет, но чаще 1-2 года. Если лечение будет полностью отсутствовать, то продолжительность жизни пациента сокращается до 3 месяцев.
Полное выздоровление возможно, если глиобластома была диагностирована на 1 и 2 стадии развития. Но это зависит от того, полностью или частично была удалена опухоль, были ли повреждены здоровые ткани головного мозга.
Глиобластома – агрессивная болезнь, которая может поражать разные части головного мозга. Но отчаиваться не стоит! Во-первых, симптомы новообразования специфичны, во-вторых, ранняя стадия отлично лечится путем операции и дальнейшей терапии. Нужно лишь вовремя обратиться для обследования в клинику – врачи воспользуются современными методами диагностики и смогут сохранить жизнь пациенту.
Филиалы и отделения, в которых лечат глиобластому головного мозга
МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Отделение нейроонкологии
Заведующий – к.м.н. ЗАЙЦЕВ Антон Михайлович
МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
Лечение глиобластомы
Глиобластома головного мозга – вид злокачественного новообразования, отличающегося высокой степенью агрессивности. Опухоль в головном мозге характеризуется стремительным и агрессивным ростом. Ранние признаки, как правило, отсутствуют, но по мере прогрессирования канцерогенеза, появляется соответствующая клиническая картина. Основной вид лечения – оперативное удаление патологического очага, подкрепленное радио- и химиотерапией. Глиобластома склонна к частому рецидивированию, поэтому прогнозы негативные.
Что такое глиобластома головного мозга
Глиобластома может развиваться из клеток головного или спинного мозга. Начало опухли дают клетки нейроглии, выполняющие вспомогательные функции. Они поддерживают жизнедеятельность и функционирование нейронов. Новообразование относится к самой высокой (четвертой) степени злокачественности, часто может формироваться из глиом (астроцитом) третьей степени злокачественности. В любом случае, опухоль ведет себя крайне агрессивно, быстро растет, прорастает в соседние ткани, не имеет четко выраженных границ, быстро и часто рецидивирует, что значительно затруднят лечение глиобластомы. Метастатический процесс развит слабо.
Обратите внимание. Данный вид рака головного мозга чаще образуется у мужчин от 40 до 65 лет. Почему так происходит понять пока не удалось.
На долю глиобластом приходится примерно 20% из общего числа всех первичных внутримозговых опухолей, но несмотря на это заболевание диагностируется довольно редко: до 3 случаев на сто тысяч человек. Без адекватного лечения летальный исход наступает в течение нескольких месяцев, потому что патологическая ткань быстро растет и поражает здоровые структуры. Наиболее часто глиобластомы формируются в височной или лобной зоне головного мозга. Под общим названием подразумевают такие формы заболевания:
Чаще всего формируется мультиформная глиобластома. Данный вид крайне агрессивен, потому что в новообразовании формируется много сосудов, при этом они рано подвергаются некрозу.
Глиобластомы являются самыми агрессивными опухолями из группы глиом. Ниже дана общепринятая классификация согласно степени злокачественности:
Причины
Как и в случае с другими видами рака, понять точные причины формирования злокачественных опухолей, образующихся в голове, пока не удалось. Образования могут быть первичными (из делящихся, растущих или переродившихся нейроглиальных клеток) или вторичными. В последнем случае начало канцерогенезу в мозговой ткани дают метастатические клетки. Провоцирующими факторами являются:
Обратите внимание. При наличии астроцитом в головном мозге, примерно у каждого десятого больного они модифицируются в глиобластомы.
Симптомы
Клинические признаки на ранней стадии, как правило, латентны. По мере прогрессирования заболевания, проявляется характерная симптоматика. Начальные признаки слабые, но они усиливаются при росте патологической ткани. Негативные проявления могут быть общими (общемозговые – спровоцированные увеличением внутричерепного давления и интоксикацией организма) и локальные, которые зависят от места формирования рака в головном мозге.
Общие признаки глиобластомы:
Локальные (очаговые) невротические признаки могут проявляться в нарушении работы зрительного, речевого и слухового анализаторов, нарушается обоняние, координация, равновесие, возможны судороги, парезы, паралич конечностей или частей тела, эпилептические припадки.
Диагностика
Успех и последствия лечения рака головного мозга во многом зависят от того, на какой стадии канцерогенеза обнаруживается опухоль. Чем раньше будет выявлена глиобластома, тем лучше проходит лечение. Золотым стандартом в исследовании головы остается компьютерная (КТ) и магнитно-резонансная (МТР) томография с использованием контраста. В последнее время широко используется ПЭТ – позитронно-эмиссионная томография. Наиболее точный диагноз и все его особенности удается выяснить путем цитогистологического анализа отобранного материала (биопсия). Это основные диагностические меры, кроме них могут быть проведены:
Стадии
Различают несколько этапов развития рака:
Лечение глиобластомы головного мозга
Лечение глиобластомы подбирается индивидуально, зависимо от стадийности канцерогенеза и общего состояния пациента. Сколько живут после удаления глиобластомы будет напрямую зависеть от того, на каком сроке болезни была сделана операция по удалению опухоли. На начальных стадиях, когда новообразование еще мало, возможно удаление глиобластомы новыми методами. Эти эндоскопические методики являются низкоинвазивными, они позволяют иссекать участок пораженной ткани без трепанации черепа. Микрооперацию проводят при помощи интраоперационной флуоресцентной навигации. Перед хирургическим вмешательством больному вводят раствор, окрашивающий ткани неоплазии, что позволяет лучше визуализировать опухоль. В этом случае удаление глиобластомы головного мозга проходит с минимальным травмированием, последствия оперативного вмешательства быстро заживают, что сокращает сроки реабилитации.
Краниотомию (открытая операция на головном мозге путем вскрытия черепной коробки) проводится часто, потому что, как правило, опухоль к моменту диагностирования достигает большого размера, поэтому удалить ее можно только путем трепанации или резекции черепа.
Из-за распространения опухоли, нечеткости ее границ и близости к жизненно важным зонам, провести тотальное удаление новообразования не всегда возможно. В таком случае операция по удалению глиобластомы будет считаться паллиативным лечением. Это позволит снизить внутричерепное давление, значительно уменьшит негативные проявления и увеличит срок жизни. Последствия операции по удалению глиобластомы будут зависеть от того, сколько удалено патологической ткани. Наилучший результат – когда опухоль удалена полностью.
Важно. При данном виде рака головного мозга оперативное лечение позволяет уменьшить негативные проявления и увеличить длительность жизни на год или более.
Важно отметить, что на поздних стадиях глиобластомы часто невозможно проведение хирургического вмешательства. В таком случае лечение неоперабельной глиобластомы проводят при помощи радиотерапии (которая становится основным методом лечения) подкрепленной назначением цитостатических препаратов. Однако, как показала практика, клетки глиобластомы проявляют высокую резистентность к ионизирующему облучению.
Для устранения неблагоприятной симптоматики назначается симптоматическое лечение:
Последствия операции
Реабилитационный период после малоинвазивных методик протекает относительно легко. После резекции или трепанации черепа восстановление сложное. Больной подлежит тщательной послеоперационной диагностике (с целью понимания успешности лечения) и постоянному мониторингу, поскольку глиобластомы принадлежат к группе опухолей, для которых характерно образование рецидивов. Нередко больным нужно снова учиться адаптироваться, разговаривать, ходить и т. д., поэтому к послеоперационной терапии подключают реабилитологов, психологов, логопедов, физиотерапевтов и других профильных специалистов. Противопоказаны физические перегрузки. Больной должен беспрекословно выполнять все требования докторов.
Важно. Глиобластомы – склонны к образованию рецидивов после операционного лечения. Их клетки низкочувствительны к радиотерапии, часто плохо поддаются лечению химиотерапией.
Прогноз жизни при глиобластоме
То, сколько проживет человек при данном виде рака, вопрос индивидуальный. Многое зависит от вида глиобластомы, срока болезни, качества хирургического лечения, возраста и общего состояния пациента. Без лечения (после постановки диагноза) более 3 месяцев проживет лишь 10% больных. При правильной терапии и успешной операции удается продлить срок жизни на полтора или два года, в 5% случаев больные могут прожить около пяти лет и даже дольше. Наиболее критический прогноз при диагностировании мультиформной глиобластомы головного мозга. В этом случае даже при успешной операции и адекватной противораковой терапии длительность жизни редко превышает более года.
Глиобластома мозга лечение
Среди опухолей головного мозга выделяют глиомные образования, из них глиобластома является самой злокачественной, она относится к опухолям 4 степени злокачественности, глиобластома отличается быстрым ростом, который по скорости можно сравнить с ростом человеческого плода. Очаг опухоли локализуется чаще в больших полушариях головного мозга, реже в мозжечке.
Новые технологии приходят в Россию.
Приглашаем пациентов принять участие в новых методах лечения онкологических заболеваний, а также в клинических испытаниях препаратов на основе Т-клеток (LAK-терапия). Терапия проводится в различных научно-исследовательских онкологических центрах, в зависимости от вида опухоли.
Отзыв о методе профессора Скворцовой В.И.
Комментарий о клеточных технологиях главного онколога России, академика Давыдова М.И.
Ученые отмечают, что в сравнении с традиционными методами лечения заболевания глиобластома у новых препаратов мало побочных эффектов.
Перечень диагностических исследований:
Инновационное лечение глиобластомы
Классификация
В зависимости от гистологической картины глиомные образования подразделяются:
Симптомы
Симптоматика зависит от локализации и размеров опухоли. Маленькие по размеру образования могут не давать длительное время никакой симптоматики, их диагностика часто происходит случайным образом.
Тревожными симптомами, которые должны насторожить человека, являются головная боль, не проходящая после приема анальгетиков, тошнота, рвота в утренние часы, изменения остроты зрения, разный диаметр зрачков, нарушения внимания и памяти.
Разные области мозга отвечают за определенные функции в организме, постепенное прорастание опухоли всегда дает клиническое проявление.
Хирургическое удаление
В данном случае опухоль стараются удалить полностью, но ровно настолько, чтобы не вызвать осложнений (например, паралич, потеря речи и прочее). Кроме того, удаление облегчает жизнь пациенту, особенно в тех случаях, когда она больших размеров и вызывает у пациента сильную головную боль или сдавливает жизненно важные структуры головного мозга. При ее удалении, возможно, что вся патологическая симптоматика, связанная с опухолью, пройдет.
Существенное значение в удалении играет расположение образования, прорастание в окружающие ткани, расположение относительно сосудов, кровоснабжающих мозг.
Для хирургических операций на головном мозге используют операционный микроскоп (обеспечивает дополнительный источник света и увеличивает изображение операционной площадки), ультразвуковой деструктор-аспиратор (облегчает удаление опухолевой ткани, сокращает время операции). Для того чтобы выбрать правильное направление для удаления образования глиобластома, используют нейронавигатор.
Для этого перед операцией пациенту проводят МРТ, результаты которого загружают в компьютер и преобразуют в 3D-изображения или «маршрут» к опухоли.
После удаления по показаниям используют интраоперационно фотодинамическую терапию с целью уничтожения опухолевых клеток, которые не удалось хирургически удалить.
Радиотерапия
В случаях, когда невозможно провести операцию либо когда она уже проведена, применяют лучевую терапию. Также возможно применение лучевой терапии в комплексе с химиотерапией препаратом Темодал. Лучевая терапия проводиться в течение 2-6 недель, доза облучения всегда максимальная, что часто приводит к выпадению волос в зоне облучения.
Виды радиотерапии
Химиотерапия

Наиболее распространенными препаратами при химиотерапии являются:
Темозоламид принимается внутрь, он ограниченно воздействует на костный мозг и не вызывает потерю волос.
При заболевании всегда используют комбинированное лечение, подбирает лечение нейрохирург и нейроонколог.
Прогноз жизни
Применение биоиммуно-препаратов: LAK терапии и дендритных вакцин, способно значительно повысить продолжительность жизни. Данные исследования проведены в США, г. Вашингтон, в Комплексном центре по исследованию рака «Georgetown Lombardi».
Приглашаем пациентов принять участие в новых методах лечения онкологических заболеваний, а также в клинических испытаниях новых препаратов
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Химиотерапия при глиобластоме головного мозга
ФГБУ «Научно-исследовательский институт нейрохирургии им. акад. Н.Н. Бурденко»
ГБУ НИИ нейрохирургии им. Н.Н. Бурденко
ФГБУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» РАМН, Москва
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко», Минздрава России, Москва, Россия
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
Результаты применения современных режимов химиотерапии первой линии в комплексном лечении пациентов с глиобластомой
Журнал: Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2016;80(6): 5-14
Абсалямова О. В., Кобяков Г. Л., Рыжова М. В., Поддубский А. А., Иноземцева М. В., Лодыгина К. С. Результаты применения современных режимов химиотерапии первой линии в комплексном лечении пациентов с глиобластомой. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2016;80(6):5-14.
Absaliamova O V, Kobiakov G L, Ryzhova M V, Poddubskiy A A, Inozemtseva M V, Lodygina K S. Outcomes of application of modern first-line chemotherapy regimens in complex treatment of glioblastoma patients. Zhurnal Voprosy Neirokhirurgii Imeni N.N. Burdenko. 2016;80(6):5-14.
https://doi.org/10.17116/neiro20168065-14
ФГБУ «Научно-исследовательский институт нейрохирургии им. акад. Н.Н. Бурденко»
Цель работы — описать порядок и результаты полноценного лечения первой линии у пациентов с глиобластомой. Материал и методы. Проанализированы 107 пациентов с глиобластомой, оперированных в 2010—2011 гг. Комбинированная химиолучевая терапия (ХЛТ) с одновременным приемом темозоломида (ТМЗ) 75 мг/м2 с последующим проведением химиотерапии и ТМЗ 200 мг/м2 в течение 5 дней каждые 28 дней проведена 75 пациентам. Отдельно рассмотрены 32 пациента с опухолями больших размеров, получавших альтернативные варианты лечения. Результаты. Медиана времени до прогрессирования составила 11,7 мес, в группах альтернативного лечения — 7,2 и 8,1 мес. Одногодичная выживаемость без прогрессирования составила 37%. Общая выживаемость составила 29,2 мес. Заключение. Для лечения пациентов после удаления ГБ оптимальным является режим химиолучевой терапии с ТМЗ с последующей монотерапией ТМЗ в течение года. При таком подходе в течение первого года у 1/3 пациентов не выявляется прогрессия опухоли. Тщательное изучение клинических и рентгенологических данных в ходе лечения позволяет достичь максимальной эффективности, избежать неоправданно раннего перехода к терапии второй линии и вовремя выявить признаки рецидива опухоли. Для оценки динамики размеров опухоли по данным МРТ целесообразно использовать критерии RANO (Международная группа Response Assessment in Neuro-Oncology). В группе больных с неоперабельными или частично удаленными опухолями показатели общей и безрецидивной выживаемости существенно ниже. Применявшиеся нами подходы дают лишь незначительные преимущества в контроле роста опухоли, что определяет необходимость поиска более эффективных вариантов лечения этих больных. Одним из них может быть добавление бевацизумаба в схему терапии первой линии. Проведено сравнение результатов выживаемости пациентов с различной продолжительностью применения химиотерапии в тех случаях, когда прекращение лечения не было обусловлено прогрессией опухоли. Проведен сравнительный анализ результатов лечения с отечественными и зарубежными данными и с собственными более ранними работами. Показано, что привело к высокой выживаемости без прогрессирования, полученной у данной группы пациентов. Рассмотрены современные подходы к оценке МРТ-данных с использованием критериев RANO, описано явление псевдопрогрессии. Предложены направления исследований для совершенствования первой линии лечения пациентов с глиобластомой.
ФГБУ «Научно-исследовательский институт нейрохирургии им. акад. Н.Н. Бурденко»
ГБУ НИИ нейрохирургии им. Н.Н. Бурденко
ФГБУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» РАМН, Москва
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко», Минздрава России, Москва, Россия
ФГАУ «НИИ нейрохирургии им. акад. Н.Н. Бурденко» Минздрава России, Москва, Россия
Глиобластома (ГБ) — самая распространенная злокачественная первичная опухоль центральной нервной системы у взрослых, частота ее встречаемости составляет 20%. ГБ характеризуется крайне неблагоприятным прогнозом: у большинства пациентов прогрессирование болезни выявляется в течение первого года после операции, а общая выживаемость (ОВ) долгое время не превышала 1 года [1]. В настоящее время к лечению пациентов с ГБ применяется комплексный подход, включающий хирургию, лучевую терапию (ЛТ) и химиотерапию (ХТ), а ожидаемая продолжительность жизни приближается к 2 годам.
«Золотым стандартом» в первой линии лечения пациентов с ГБ является максимально возможное удаление опухоли с последующим проведением комбинированной химиолучевой терапии (ХЛТ) с темозоломидом (ТМЗ) и последующей адъювантной химиотерапией (ТМЗ). ЛТ проводится на область опухоли (захватывая 2—3 см вокруг нее) до суммарной дозы 60 Гр при разовой дозе 2 Гр, на фоне приема ТМЗ (в дозе 75 мг/м 2 ).Через 28 дней после завершения этого лечения начинается проведение химиотерапии ТМЗ в дозе 200 мг/м 2 на прием (в течение 5 дней, затем 23 дня перерыв). Этот режим впервые описан R. Stupp и соавт. [2], которые показали, что добавление в схему лечения ТМЗ в указанном режиме увеличивает медиану времени до прогрессирования (МВДП) с 5 до 6,9 мес, а ОВ — с 12,1 до 14,6 мес в сравнении с группой пациентов, получавших только Л.Т. По данным исследования M. Gilbert и соавт. [3], завершенного в 2013 г., МВДП при применении этого режима составила 8,8 мес, а ОВ — 18,9 мес.
Цель работы — оценить показатели общей и безрецидивной выживаемости 107 пациентов с морфологически верифицированной глиобластомой, получавших лечение в НИИ нейрохирургии им. Н.Н. Бурденко в 2010—2011 гг.
Материал и методы
Проанализированы результаты лечения 107 пациентов с морфологически верифицированными ГБ, оперированных в 2010—2011 гг. и регулярно наблюдавшихся в НИИ нейрохирургии им. Н.Н. Бурденко. Мы ретроспективно анализировали результаты ежедневной работы, когда решение для каждого пациента принималось в соответствии с современными стандартами лечения ГБ с учетом индивидуальных особенностей, например размеров опухоли, общего статуса, наличия внутричерепной гипертензии.
Общие данные о пациентах представлены в табл. 1.

Для оценки динамики размеров опухоли использованы архивные данные МРТ-исследований головного мозга с контрастным усилением, выполненных перед проведением ХЛТ, через 1 мес после завершения ХЛТ, далее — после каждых 3 курсов Х.Т. По завершении лечения МРТ выполняли каждые 3—5 мес, а также при наличии клинических признаков прогрессии опухоли, с оценкой по критериям RANO (Международная группа Response Assessment in Neuro-Oncology).
Результаты
На момент анализа данных прогрессирование болезни выявлено у 91 (85%) из 107 пациентов. Выживаемость без прогрессирования более 1 года — 37% (40 человек). Без прогрессирования 17 (15,8%) человек прожили 12—18 мес, еще 12 (11,2%) прожили 18—24 мес, 11 человек прожили более 24 мес (10 — до 3 лет и 1 — более 3 лет). Без учета видов лечения МВДП составила 10,3 мес, ОВ — 29,2 мес. МВДП по группам лечения была следующей: комбинированная ХЛТ с ТМЗ с последующей терапией ТМЗ —11,7 мес, комбинированная ХЛТ с ТМЗ с последующей терапией ТК — 7,2 мес, пациенты, начавшие лечение с проведения ХТ, с возможным последующим проведением ЛТ — 8,1 мес (р=0,008) (рис. 1). Общая выживаемость составила 33,3, 26,3 и 18 мес соответственно (р=0,007).

Обсуждение
Цель работы — оценить результаты лечения больных с глиобластомой, с применением хирургической техники высокого уровня, современных методик ЛТ, проведением достаточного числа курсов ХТ в современных режимах.
Количество прослеженных пациентов
Мы описали результаты лечения лишь 107 пациентов, что составляет 31,4% от всех пациентов, впервые прооперированных по поводу ГБ в НИИ нейрохирургии им. Н.Н. Бурденко в 2010—2011 гг. Относительно небольшое количество пациентов, включенных в анализ, обусловлено как потерей катамнеза, так и несоблюдением стандартов лечения ГБ [4]. Наши данные совпадают с данными А.В. Смолина и соавт., проводивших Российское многоцентровое исследование по эпидемиологии злокачественных глиом с 01.01.2012 по 31.12.2013. В это исследование включены 325 пациентов из 29 медицинских центров России. Показано, что комбинированная ХЛТ проведена только каждому четвертому, 1/3 пациентов вообще не получали ХТ первой линии. Среди получавших ХТ первой линии часть пациентов получали иные препараты, но не ТМЗ [5].
Таким образом, высокие цифры МВДП, полученные в работе, обусловлены использованием современных режимов лечения глиобластомы, а больные, не лечившиеся, не обращавшиеся для повторной консультации, недоступные для сбора катамнеза и, возможно, умершие в ранние сроки после операции, не вошли в наше исследование.
Комбинированная химиолучевая терапия с темозоломидом с последующей адъювантной терапией темозоломидом
В исследуемой группе МВДП составила 11,7 мес. У пациентов, пролеченных под наблюдением в НИИ нейрохирургии им. Н.Н. Бурденко в идентичном режиме, в 2006—2007 гг., МВДП составила 9,7 мес [6].
В мировой практике стандартный режим ХЛТ с ТМЗ и последующей терапией ТМЗ подразумевает проведение только 6 курсов Х.Т. Тем не менее часть клиницистов склоняются к целесообразности проведения большего числа курсов, особенно для пациентов, имеющих контрастируемые остатки опухоли. Сравнительных рандомизированных исследований, определяющих эффективность такого подхода, не проводилось. При сравнении подходящих групп из разных исследований выявлено следующее. В исследовании M. Stupp и соавт. [2] в группе пациентов, получивших ХЛТ+6 курсов ТМЗ, МВДП составила 6,9 мес, в исследовании O. Chinot и соавт. [7] в группе ХЛТ+6 курсов ТМЗ — 6,2 мес, в исследовании М. Gilbert и соавт. [4] в группе пациентов, получивших ХЛТ + 12 курсов ТМЗ, МВДП была 8,8 мес. Следует отметить, что в исследовании R. Stupp и соавт. у 16—17% пациентов выполнена только биопсия опухоли, у O. Chinot и соавт. доля биопсий составила 9,5—13,1%, у M. Gilbert — 3%. Таким образом, остается неясным, что именно определило повышение МВДП — продолжительность ХТ или радикальность удаления опухоли.
В нашей серии только биопсия опухоли выполнена у 3,8% пациентов. При назначении более 6 курсов ХТ мы руководствовались в первую очередь переносимостью терапии и наличием остаточной опухоли. Если терапия переносилась (по показателям крови) удовлетворительно, мы продолжали лечение до 10 курсов. При ретроспективном анализе у 51 пациента после завершения ХЛТ и проведения 6 курсов ХТ не было прогрессирования, МВДП при прекращении ХТ или ее продолжении была 17,7 и 17,3 мес соответственно, различия недостоверны (р=0,512) (рис. 2). При продлении ХТ свыше 10 курсов мы руководствовались наличием контрастируемых остатков опухоли, отсутствием признаков прогрессирования на фоне продолжающегося лечения, а также повышенной метаболической активностью в опухоли по результатам позитронно-эмиссионной томографии (ПЭТ) головного мозга с С 11 метионином. У 20 пациентов, не имеющих прогрессирования после 10 курсов ХТ, МВДП при прекращении ХТ была 26,4 мес, а при продолжении ее свыше 10 курсов — 19,2 мес (р=0,015) (рис. 3). Различия не оказались достоверными. Из этого можно заключить, что таким пациентам требуется продолжение противоопухолевой терапии, но, вероятно, в других режимах.


Бевацизумаб в первой линии терапии ГБ
Одним из первых исследований, послуживших основанием к использованию бевацизумаба (БЕВ) при прогрессии ГБ, было исследование Cloughesy. Описаны 167 пациентов с рецидивом ГБ, пролеченных БЕВ или БЕВ в комбинации с иринотеканом, частичный ответ на лечение (уменьшение опухоли на 50% и более) был достигнут у 28,3% пациентов при применении БЕВ и у 37,8% пациентов при применении БЕВ+иринотекан, у нескольких пациентов достигнут полный ответ. Сходные данные получены нами у 36 пациентов с рецидивом ГБ, получавших комбинации различных цитостатиков с БЕВ (в России БЕВ разрешен для лечения ГБ с ноября 2009 г.) — 13 пациентов имели частичный ответ и 3 — полный ответ [9].
Применение БЕВ в первой линии лечения, в дополнение к режиму R. Stupp, по результатам проведенных исследований Avaglio и RTOG 0825, увеличивает МВДП, но не влияет на О.В. Так, среди пациентов, участвовавших в Avaglio, МВДП при использовании режима ХЛТ с ТМЗ составила 6,2 мес, а при добавлении к этому режиму БЕВ 10 мг/кг каждые 2 нед, начиная с первого дня ХЛТ и далее до прогрессирования, МВДП была 10,8 мес. ОВ составила 16,7 и 16,8 мес соответственно [7]. Подобная разница во влиянии БЕВ на МВДП и ОВ обусловлена тем, что пациенты, не получавшие БЕВ в первой линии, принимали его во второй линии лечения, в результате чего ОВ в обеих группах пациентов сравнялась. В настоящее время БЕВ не рекомендован в первой линии терапии ГБ.
Критерии оценки эффективности лечения опухолей центральной нервной системы
Говоря о прогрессии опухоли, нельзя обойти вниманием критерии определения признаков прогрессирования. С 1990 г. в нейроонкологии использовались критерии оценки опухолей по D. Macdonald и соавт. [10]. Они учитывали размеры опухоли, наличие новых очагов, динамику неврологической симптоматики, применение стероидной терапии. Одним из недостатков этих критериев является невозможность оценки неконтрастируемых опухолей. Другая серьезная проблема — использование критериев Macdonald для опухолей, подвергнутых терапии антиангиогенными препаратами (например, БЕВ), которые изменяют проницаемость капилляров и тем самым препятствуют контрастированию опухоли. В такой ситуации истинное ее распространение можно определить только в T2/FLAIR-режиме. Поэтому с 2010 г. в практику вошли критерии оценки RANO [11]. В критериях RANO оценивается динамика размеров опухоли по МРТ в режиме Т1 с контрастом и зоны гиперинтенсивного сигнала в режимах Т2 и FLAIR, а также учитывается неврологический статус и использование дексаметазона (табл. 2).

Клинический пример
Для иллюстрации примененной нами тактики лечения приведем следующее клиническое наблюдение.
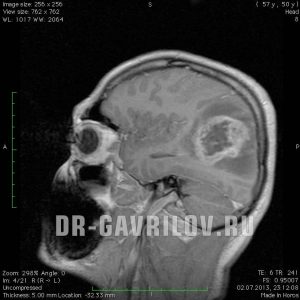
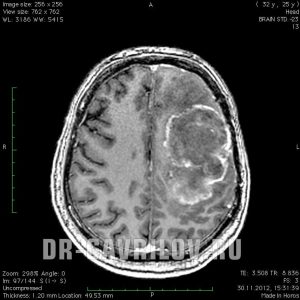
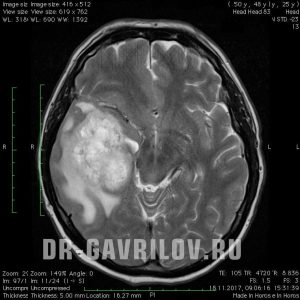
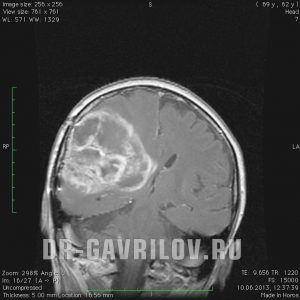
Больной Ч., 40 лет. С мая 2012 г. у пациента впервые возникли нарастающие головные боли, отмечен генерализованный судорожный приступ. МРТ головного мозга с внутривенным контрастированием 26 мая 2012 г. выявила объемное образование правой височной доли, активно накапливающее контраст, с выраженным перифокальным отеком (рис. 4, а). 02.07.12 проведено удаление опухоли. При гистологическом исследовании установлена ГБ. В июле — августе 2012 г. проведено ХЛТ: ЛТ РОД 2—3 Гр СОД 48 Гр (к сожалению, в ряде учреждений РФ в лечении больных с опухолями головного мозга используются нестандартные разовые дозы ЛТ) с одновременным приемом ТМЗ 140 мг внутрь ежедневно. На МРТ в сентябре 2012 г. не выявлено контрастируемых остатков опухоли (см. рис 4, б). С сентября 2012 г. по июль 2013 г. проведено 11 курсов химиотерапии ТМЗ 400 мг внутрь, 5 дней каждые 28 дней. На МРТ в июле 2013 г. не обнаружено контрастируемых остатков опухоли (см. рис 4, в). По данным ПЭТ головного мозга, с С 11 метионином в июле 2013 г. выявлен очаг повышенного накопления радиофармпрепарата, индекс накопления (ИН) 1,62 — остатки опухоли с умеренной метаболической активностью. На этом основании продолжена ХТ ТМЗ, к февралю 2014 г. проведено 17 курсов. Состояние пациента было удовлетворительным, стероидная терапия не проводилась, эпилептические приступы не возобновлялись, пациент вернулся к работе. С февраля 2014 г. по сентябрь 2015 г. (20 мес) химиотерапия не проводилась. При очередной МРТ в сентябре 2015 г. (38 мес после операции) выявлено увеличение площади гиперинтенсивного сигнала в режиме FLAIR в области операции и в полюсе височной доли справа. Нарастания неврологической симптоматики не отмечалось. ПЭТ, выполненная 28.09.15, показала в полюсе височной доли, соответственно выявленным изменениям по МРТ очаг гиперметаболизма с ИН 2,05 — продолженный рост опухоли (см. рис. 4, в). С 19.10.15 по 21.10.15 проведен курс стереотаксической радиотерапии в режиме гипофракционирования на область рецидива опухоли в правой височной доле с краевым захватом 3 мм (GTV/СTV=2,969/5,612 см 3 ), подведено 3 фракции по 8 Гр до СОД=24,82/24,1 Гр в среднем, методикой множественных пучков (N=145), до СОД=21,5 Гр по 81% предписанной изодозе. Возобновлена химиотерапия ТМЗ, с октября 2015 г. по март 2016 г. проведено 6 курсов. МРТ в феврале 2016 г. (44 мес после операции) демонстрирует уменьшение зоны гиперинтенсивного сигнала в режиме FLAIR в полюсе височной доли справа, стабильную картину в зоне операции. ПЭТ головного мозга с С 11 метионином: накопление радиофармпрепарата уменьшилось, ИН 1,23 (см. рис. 4, г). Ухудшения в неврологическом статусе не отмечается. Головная боль, эпилептические приступы не возобновлялись с момента выполнения оперативного лечения. На момент написания статьи прошло 48 мес, признаков прогрессирования заболевания нет.

Псевдопрогрессия
Термин «псевдопрогрессия» впервые предложен в 2007 г. Псевдопрогрессией (ПсП) называют подострые изменения, развивающиеся в течение 12 нед после ЛТ, рентгенологически выражающиеся в увеличении контрастируемых очагов более чем на 25%. Считается, что проведение комбинированной ХЛТ с ТМЗ увеличивает частоту феномена ПсП. Несмотря на МР-признаки прогрессирования болезни, у части таких пациентов в последующем наблюдается спонтанный регресс как клинических симптомов, так и контрастируемых очагов на МРТ. Частота ПсП составляет в среднем 20—30%. Показано, что развитие ПсП коррелирует с метилированным геном МГМТ в опухоли и, возможно, является предиктором высокой эффективности проводимой терапии [12]. Таким образом, применение вышеописанных критериев оценки актуально лишь в сроки после 12 нед по завершении ЛТ, ранее этого времени основным признаком прогрессии опухоли служит появление нового очага вне зоны облучения.
Для клиницистов феномен псевдопрогрессии является причиной сомнений в выборе дальнейшей тактики лечения. С одной стороны, игнорируя феномен ПсП и меняя план лечения, мы лишаем больного возможности продолжения эффективной и удобной терапии ТМЗ. С другой стороны, истинная прогрессия, при которой продолжение прежней терапии нецелесообразно, встречается гораздо чаще. Ряд исследователей [13] «модифицируют» критерии псевдопрогрессии, относя к ней лишь те случаи, когда увеличение контрастируемых очагов не вызывает нарастания симптоматики, а сроки, допустимые для диагноза ПсП, не превышают 1 мес после ХЛТ.
Определение истинной прогрессии и псевдопрогрессии крайне важно при планировании второй линии терапии Г.Б. При включении в исследование пациентов с ПсП могут быть получены ложновысокие показатели эффективности.
В нашей серии наблюдений увеличение контрастируемых очагов более 25% в сроки 160 дней от постановки диагноза, т. е. примерно через 12 нед после завершения ХЛТ, отмечено у 17 пациентов (10 из этих пациентов продолжили лечение). Более 1 года после выявления прогрессирования прожили 7 (41%) из 17 пациентов, на момент написания работы 6 человек умерли, 1 пациентка жива, общая выживаемость в этой группе составляет от 22 до 66 мес (выживаемость в среднем — 33 мес). Вероятнее всего, у этих 7 пациентов действительно был феномен псевдопрогрессии.
Для дифференцирования прогрессии и псевдопрогрессии могут быть применены метаболические, перфузионные, диффузионные рентгенологические исследования, достоверность и порядок их использования требуют дальнейшего изучения [12].
Пациенты с ГБ больших размеров и с неоперабельными ГБ
В 2009 г. на базе НИИ нейрохирургии им. Н.Н. Бурденко была завершена работа «Химиотерапия в лечении больных с неоперабельными супратенториальными злокачественными астроцитарными глиомами». По данным этой работы, у 37 больных с неоперабельными ГБ больших размеров, которым после СТБ проводилась только ХТ, были использованы три схемы: PCV — у 15 (40,5%) больных, ТМЗ — у 5 (13,5%), ТМЗ+цисплатин — у 17 (54%) больных. МВДП составила 5, 4 и 8 мес, медиана ОВ — 8,5, 6,0 и 10,5 мес соответственно. В случае проведения только ХТ наиболее высокая непосредственная эффективность получена при использовании схемы ТМЗ+цисплатин: полный ответ — у 2 пациентов, частичный ответ — у 10, стабилизация — у 7, прогрессирование — у 7. При использовании ТМЗ в монотерапии максимальным эффектом была стабилизация [14].
Предпосылкой к изучению комбинации ТМЗ+цисплатин явился ряд исследований, выполненных у больных с рецидивами Г.Б. Первой и самой большой серией наблюдений, показавшей эффективность комбинации ТМЗ+цисплатин при рецидивах ГБ у больных, не получавших ранее ХТ, было исследование A. Brandes и соавт. [15]. За основу были взяты исследования invitro, показавшие, что цис-платин способен не только редуцировать активность МГМТ, но и усиливать эффективность действия ТМЗ в этом направлении. Также показана эффективность комбинации ТМЗ+цисплатин у пациентов, уже применявших ТМЗ и имевших после этого ПРОП [16]. С. Balana и соавт. [17] показали эффективность применения ТМЗ+цисплатин в качестве первой линии лечения у пациентов с верифицированными неоперабельными ГБ.
Мы в данной группе больных с ГБ вместо цис-платина в комбинации с ТМЗ использовали карбоплатин. Карбоплатин обладает меньшей нефротоксичностью и существенно меньшей эметогенностью.
У 792 пациенток с распространенным раком яичников комбинация карбоплатин+паклитаксела была не менее эффективна, чем комбинация цисплатин+паклитаксел, обладала меньшим количеством побочных эффектов и более удобным режимом введения [18]. У 598 больных с герминогенными опухолями яичка при сравнении эффективности комбинаций блеомицин+этопозид+карбоплатин либо цисплатин (BEC/ВЕР) показано, что ВЕС существенно проигрывает BEP с точки зрения безрецидивной и общей выживаемости [19]. Опыт лечения 618 пациентов с распространенным немелкоклеточным раком легкого к режимах карбопла-тин+паклитаксел либо цисплатин+паклитаксел показал, что при одинаковом числе ответов на лечение ОВ пациентов была больше при применении комбинации цисплатин+паклитаксел, а комбинация карбоплатин+паклитаксел является разумной альтернативой, с аналогичным процентом ответа, хорошим профилем безопасности, приемлемой токсичностью и удобством применения [20]. Срав-нительная оценка эффективности комбинации темо-золомид+цисплатин и ТМЗ+карбоплатин у пациентов с неоперабельными глиомами не проводилась.
В нашей серии 12 пациентов в качестве первой линии терапии получали только ХТ. Первично-множественные ГБ были у 4 пациентов, одному из них проведена СТБ, остальным удален один из узлов опухоли. Распространенная диффузная ГБ была у 8 пациентов. В 2 случаях проведена СТБ, в 6 — частичное удаление опухоли. Во всех случаях размер имевшейся либо оставшейся после удаления опухоли препятствовал проведению Л.Т. Эти 12 пациентов получали ХТ в режиме Т.К. После уменьшения размеров опухоли у 6 пациентов проведена ЛТ. МВДП во всей группе составила 8,1 мес.
Основываясь на имеющихся данных об эффективности комбинации ТМЗ с препаратами платины при ГБ больших размеров, мы назначали ТК после завершения ХЛТ пациентам с частично удаленными Г.Б. Таких пациентов было 20. Из них у 16 пациентов прогрессирование опухоли выявлено ранее завершения 6 курсов Х.Т. Продолжили лечение более 6 курсов 4 человека, из них 3 пациента имели прогрессию после 8, 9 и 12 курсов соответственно. Остановлено лечение на 10 курсах у 1 больного. Медиана времени до прогрессирования в данной группе составила 7,2 мес.
Ретроспективные данные показывают, что пациенты с неоперабельными ГБ в случае только симптоматической терапии живут около 3 мес, при проведении ЛТ — 6—7 мес [21]. Таким образом, режимы темозоломид+цисплатин и ТМЗ+карбо-платин могут быть рекомендованы к применению у пациентов с распространенной диффузной глиобластомой. Однако, несмотря на достигнутые преимущества в ОВ, результаты лечения пациентов с ГБ больших размеров остаются неудовлетворительными.
Раннее прогрессирование опухоли у этих больных свидетельствует об относительно низкой эффективности проводимой терапии и необходимости применения более эффективных препаратов, например с использованием БЕВ.
Как уже было сказано выше, по результатам рандомизированных исследований III фазы БЕВ не показан в первой линии лечения Г.Б. Тем не менее анализ данных О. Chinot установил, что применение БЕВ в первой линии терапии неодинаково сказывается на выживаемости при различных подтипах Г.Б. Так, для пациентов с проневральным типом ГБ и отсутствием мутации гена IDH1 при применении БЕВ в первой линии лечения ОВ составила 17,1 мес, а в группе плацебо — 12,8 мес (р=0,002) [22]. Также было показано, что применение БЕВ давало достоверное увеличение времени до ухудшения статуса общего здоровья, физического, социального функционирования, моторного и коммуникационного дефицита. Описана способность БЕВ эффективно уменьшать отек головного мозга [23].
Следует также отметить, что критерии включения пациентов в Avaglio и RTOG 0825 подразумевали статус пациентов по шкале Карновского 70 и более, в то время как большинство пациентов нашей серии, получавших ТК, имели более низкий показатель. Таким образом, принимая во внимание высокую непосредственную эффективность БЕВ, выявляемую как клинически, так и при МРТ, имеет смысл изучить его эффективность в первой линии лечения у пациентов с диффузной распространенной Г.Б. Необходим поиск факторов, позволяющих прогнозировать преимущество применения БЕВ, например подтипа ГБ, содержания матриксной металлопротеиназы в плазме крови, статуса метилирования гена МГМТ.
Заключение
Для лечения пациентов после удаления ГБ оптимальным является режим химиолучевой терапии с темозоломидом с последующей монотерапией темозоломидом в течение года. При таком подходе в течение первого года у трети пациентов не выявляется прогрессия опухоли. Тщательное изучение клинических и рентгенологических данных обследования в ходе лечения позволяет извлечь из него максимум эффективности, избежать неоправданно раннего перехода к терапии второй линии и вовремя выявить признаки рецидива опухоли. Для оценки динамики размеров опухоли, по данным МРТ, целесообразно использовать критерии RANO. В группе больных с неоперабельными или частично удаленными опухолями показатели общей и безрецидивной выживаемости существенно ниже. Применяемые нами подходы дают лишь незначительные преимущества в контроле роста опухоли, что определяет необходимость поиска более эффективных вариантов лечения этих больных. Одним из них может быть добавление бевацизумаба в схему терапии первой линии.
Комментарий
Работа посвящена очевидно актуальной теме — лечению пациентов с глиобластомами головного мозга. Достоинством работы является анализ собственных результатов лечения больных в условиях рутинной практики, тщательный сбор катамнеза, вдумчивый анализ полученных результатов, использование при их обсуждении данных не только иностранных, но и отечественных исследований. Собрана информация о 107 пациентах, проходивших лечение в НИИ нейрохирургии им. Н.Н. Бурденко в 2010—2012 гг. Учитывая высокую стоимость, лечение глиобластом в РФ в значительном числе случаев не соответствует мировым стандартам. Большое количество пациентов, получавших лечение в одном учреждении в полном соответствии со стандартами, — редкость, однако, как показано в работе, именно такой подход позволяет не только воспроизводить, но и превышать результаты лечения в лучших мировых клиниках. Важное с практической точки зрения значение имеют полученные данные об отсутствии необходимости увеличения количества курсов химиотерапии с темозоломидом более шести.