Научная электронная библиотека
2.2. Физиологические механизмы компенсации нарушенных функций организма в центральной нервной системе
Компенсаторные реакции возникают в ответ на нарушение функций, структур, обменных процессов и являются реакцией целостного организма. Они направлены, прежде всего, на восстановление гармоничных, координированных взаимоотношений органов и систем
в интересах целостного организма; поддерживают и сохраняют равновесие организма со средой. В основе сложного механизма компенсации лежит перестройка функций организма, регулируемая центральной нервной системой (ЦНС).
Чем тяжелее дефект, тем большее количество систем организма включается в процесс компенсации. Наиболее сложные функциональные перестройки наблюдаются при нарушениях ЦНС, в том числе и анализаторов. Таким образом, степень сложности механизмов компенсаторных явлений находится в зависимости от тяжести дефекта.
Автоматизм включения компенсаторных функций не определяет сразу механизмы компенсации; так, при сложных нарушениях деятельности организма они формируются постепенно. Постепенность развития компенсаторных процессов проявляется в том, что они имеют определенные стадии становления, которые характеризуются особым составом и структурой динамических систем нервных связей и своеобразием протекания процессов возбуждения и торможения.
Материальным субстратом компенсаторных перестроек является центральная нервная система. Формирование механизмов компенсации подчинено законам высшей нервной деятельности. Современная теория компенсации рассматривает компенсаторные явления в свете рефлекторной теории И.П. Павлова. Эта теория, базирующаяся на трех основных принципах: причинность (детерминизм), единство анализа и синтеза и структурность.
Применительно к учению о компенсации нарушенных или утраченных функций принципы рефлекторной деятельности означают следующее:
Принцип причинности. Любой дефект неизбежно вызывает ответную реакцию организма, причем сила и характер этой реакции зависят не только от степени нарушения той или иной функции или органа, но и от состояния организма и тех условий, которые его окружают. Эта реакция имеет своим механизмом замыкание новых временных связей в коре больших полушарий головного мозга.
Так, известен случай, когда после четырехкратной операции по поводу опухоли мозга у 12-летнего ребенка была удалена большая часть левого полушария мозжечка. Сразу после каждой операции у ребенка возникали нарушения двигательной сферы, речи и других функций мозга. Однако довольно быстро эти нарушения компенсировались. Компенсаторные возможности мозга с возрастом уменьшаются, это обусловлено ослаблением лабильности в формировании новых функциональных связей.
Принцип единства анализа и синтеза. В процессе анализа и синтеза, внешних воздействии у человека образуется весьма сложная, по строению функциональная система анализаторов. Полное или частичное нарушение функций какого-либо анализатора приводит к определенным нарушениям этой системы, что отражается в первую очередь на аналитической деятельности. Включение компенсаторных функций приводит к перестройке сохранных анализаторов, благодаря чему способность к аналитико-синтетической деятельности сохраняется, хотя диапазон, уровень, степень и путь анализа суживаются.
Например, при тотальной слепоте очень часто наблюдается высокая тактильная чувствительность. «Видеть руками» – есть такой термин, относительной данной категории людей.
Принцип структурности заключается в приуроченности функции головного мозга к его структуре, то есть определенные функции локализуются в определенных центрах. В этом отношении кора больших полушарий головного мозга представляет собой, по выражению И.П. Павлова, «мозаику», в которой пространственно локализуются раздражители. Однако строгая локализация функций в коре головного мозга представляет собой в то же время целостную динамическую систему, в которой каждое местное воздействие влечет за собой изменение во всей системе. Именно благодаря динамической системности коры больших полушарий возможны иррадиация, концентрация и взаимная индукция процессов возбуждения и торможения и образование на этой основе новых временных связей.
В результате взамен утраченного способа образования временных нервных связей в нервной системе проторяются новые, обходные пути, формируются новые условно-рефлекторные нервные связи, восстанавливающие нарушившееся равновесие во взаимоотношениях организма и среды.
Таким образом, физиологический механизм компенсации основывается на нормальном функционировании сохранных систем. При этом включение механизмов компенсации происходит, безусловно-рефлекторным путем, автоматически, а дальнейшее развитие компенсаторных приспособлений есть деятельность условно рефлекторная.
Свойства ЦНС, обеспечивающие механизмы компенсации:
Полифункциональность и полисенсорность каждого из элементов нервной системы. Основная функция нервной системы заключается в сборе, переработке, хранении, воспроизведении и передаче информации с целью организации интеллектуальной, поведенческой деятельности, регуляции функционирования органов, систем органов и обеспечения их взаимодействия. Многие из перечисленных функций реализуются уже на нейронном уровне. Нейроны обладают способностью выполнять все информационные функции нервной системы: восприятие, обработку, хранение, многократное воспроизведение и передачу информации. В этом и заключается основной принцип функционирования нервной системы – принцип полифункциональности.
Полифункциональность присуща большинству структур ЦНС. Например, сенсомоторная кора способна воспринимать сигналы кожной, зрительной, слуховой и других видов рецепции. В ответ на эти сигналы в сенсомоторной коре формируются реакции, которые обычно возникают при нормальной деятельности коркового конца зрительного, слухового или других анализаторов. Следовательно, благодаря полифункциональности одна и та же функция может быть выполнена разными структурами мозга. Этот принципиальный момент свидетельствует о практически безграничных возможностях компенсации функции в ЦНС.
Свойства полифункциональности нервных центров тесно связаны со свойством полисенсорности нейронов. Полисенсорность – это способность одного нейрона реагировать на сигналы разных афферентных систем. Нейрофизиологи выделяют нейроны моносенсорные, реагирующие только на один вид сигналов, бисенсорные – реагирующие на два разных сигнала, например, некоторые нейроны зрительной коры могут реагировать на зрительные и слуховые раздражения. Наконец, в коре мозга имеются нейроны, которые реагируют на три и более вида сигналов. Эти нейроны называются полисенсорными.
Относительная специализация нейронов отдельных областей мозга и локализация функций в коре. Нейроны отдельных областей мозга способны реагировать только на одну характеристику сенсорного раздражения, например, на определенную частоту звука или только на один цвет. Такие нейроны называются мономодальными (моносенсорными). Они обладают высокой избирательностью и высокой чувствительностью к определенным видам раздражений, т.е. являются специализированными. Локализуются специализированные нейроны в зонах первичных проекций анализаторов. Такими зонами являются первичные области зрительной, слуховой, кожной и других зон коры.
Локализация функций в коре определяется, прежде всего, моносенсорными нейронами, имеющими наименьшие пороги чувствительности на свои адекватные раздражения. Однако рядом с этими нейронами всегда имеются полисенсорные нейроны, которые обеспечивают взаимодействие локальной структуры с другими структурами мозга, а тем самым – возможность образования временной связи, компенсацию нарушений функций своей структуры и структур, с нею связанных. Полимодальные нейроны обеспечивают внутрисистемную компенсацию нарушенных функций.
Параллельная (одновременная) обработка разно сенсорной информации. В коре мозга нет такой зоны, которая была бы связана с реализацией только одной функции. В разных отделах мозга имеется разное количество полисенсорных и полимодальных нейронов. Наибольшее количество таких нейронов находится в ассоциативных и во вторичных, третичных зонах коркового конца анализаторов. Значительная часть нейронов моторной коры (около 40 %) также является полисенсорной, они реагируют на раздражения кожи, на звук, свет.
Число полисенсорных нейронов в структурах мозга меняется в зависимости от функционального состояния нервной системы и от выполняемой в данный момент времени задачи. Так, в период обучения с участием зрительного и моторного анализаторов число полисенсорных нейронов в этих зонах коры возрастает. Следовательно, направленное обучение создает условия увеличения полисенсорных нейронов и, тем самым, компенсаторные возможности нервной системы возрастают.
Важно также, что некоторые нейроны коры мозга в результате обучения способны становиться полисенсорными, т.е. если до применения сочетания условного и безусловного стимулов нейрон реагировал только на безусловный стимул, то после ряда сочетаний этот нейрон становится способным реагировать и на условный стимул.
Полимодальность и полисенсорность позволяют нейрону одновременно воспринимать раздражения от разных анализаторов или, если от одного анализатора, то воспринимать одновременно сигналы с разными его характеристиками.
Структурная избыточность и функциональная надежность. Полифункциональность и полисенсорность связаны с другим свойством функционирования мозга – его надежностью. Надежность также обеспечивается такими механизмами, как избыточность, модульность, кооперативность.
Избыточность достигается разными способами. Наиболее распространенным является резервирование элементов. У человека в коре постоянно активны только доли процента нейронов, но их достаточно для поддержания тонуса коры, необходимого для реализации ее деятельности. При нарушении функционирования коры количество фоновоактивных нейронов в ней значительно увеличивается. Избыточность элементов в ЦНС обеспечивает сохранение функций ее структур даже при повреждении значительной их части.
Например, удаление значительной части зрительной коры не приводит к нарушениям зрения. Одно полушарное повреждение структур лимбической системы не вызывает специфических для нее клинических симптомов. Доказательством того, что нервная система имеет большие резервы, являются следующие примеры. Глазодвигательный нерв нормально реализует свои функции регуляции движений глазного яблока при сохранности в его ядре всего 45 % нейронов. Отводящий нерв нормально иннервирует свою мышцу при сохранности 38 % нейронов его ядра, а лицевой нерв выполняет свои функции всего при 10 %-ной сохранности числа нейронов, расположенных в ядре этого нерва.
Высокая надежность в нервной системе обусловлена также множеством связей ее структур, большим количеством синапсов на нейронах. Так, нейроны мозжечка имеют на своем теле и дендритах до 60 тыс. синапсов, пирамидные нейроны двигательной коры – до 10 тыс., альфа-мотонейроны спинного мозга – до 6 тыс. синапсов.
Резервирование проявляется множеством путей реализации сигнала; так, дублирующийся двигательный сигнал, идущий из коры к мотонейронам спинного мозга, может достигнуть их не только от пирамидных нейронов 4 поля коры, но и от добавочной моторной зоны, из других проекционных полей, из базальных ганглиев, красного ядра, ретикулярной формации и других структур. Следовательно, повреждение моторной коры не должно приводить к полному выпадению двигательной информации к мотонейронам спинного мозга.
Следовательно, помимо резервирования, надежность нервной системы достигается дублированием, что позволяет оперативно вводить, по мере надобности, дополнительные элементы, чтобы реализовать ту или иную функцию. Примером такого дублирования может служить многоканальная передача информации, например, в зрительном анализаторе.
Модульность – это принцип структурно-функциональной организации коры мозга, который заключается в том, что в одном нейронном модуле осуществляется локальная переработка информации от рецепторов одной модальности. Между дендритами этого пучка имеют место не только синаптические связи, но и электротонические контакты. Последние обеспечивают синхронность работы нейронов микромодуля, что повышает надежность передачи информации.
В зрительной коре имеет место чередование колонок, нейроны которых реагируют на зрительные стимулы либо только правого, либо только левого глаза. Следовательно, в зрительной коре обоих полушарий мозга имеются глазодоминантные колонки, т.е. колонки, реагирующие на стимуляцию одного глаза (А.Г. Литвак, 2017).
В слуховой коре выделяются колонки, способные дифференцировать сигналы, идущие от обоих ушей, и колонки, не способные к такой дифференциации.
В сенсомоторной коре рядом расположенные колонки выполняют разнонаправленные реакции: например, одни из них возбуждают мотонейроны спинного мозга, другие – тормозят их.
Модульный принцип структурно-функциональной организации работы мозга является проявлением кооперативного характера функционирования нейронов мозга.
Кооперативность создает возможность относительной взаимозаменяемости нейронов, и, тем самым, повышает надежность нервной деятельности. В результате функционирование системы становится мало зависящим от состояния отдельной нервной клетки.
Кооперативность дает возможность структуре выполнять функции, не присущие отдельным ее элементам. Так, отдельный нейрон мозга не способен к обучению, но, находясь в сети нейронов, он приобретает такую способность.
Способность к саморегуляции и самоорганизации. Саморегуляция – свойство структур нервной системы автоматически устанавливать и поддерживать на определенном уровне свое функционирование. Основным механизмом саморегуляции является механизм обратной связи. Обратная связь упорядочивает, суживает множество вариантов прохождения сигнала, создавая тормозное окружение пути возбуждения из неактивных нейронов.
Тесно связан с саморегуляцией нервной системы механизм ее самоорганизации. Самоорганизующиеся системы вообще имеют ряд особенностей, которые присущи и ЦНС: множество входов и выходов; высокий уровень сложности взаимодействия своих элементов; большое количество функционирующих элементов и т.д. Благодаря принципу самоорганизации компенсация функций в нервной системе обеспечивается формированием новых связей на основе включения в активность потенциальных синапсов, использованием накопленного опыта данного индивида.
Развитие нервной системы в онтогенезе приводит к непрерывному усложнению взаимодействия ее систем. Чем больше форм, видов, число условных рефлексов, организуемых в онтогенезе, тем больше связей устанавливается между структурами нервной системы.
Увеличение количества функциональных связей между структурами нервной системы имеет решающее значение, так как в этом случае возрастает число вариантов прохождения сигналов, значительно расширяются возможности компенсации нарушенных функции.
В функции самоорганизации немаловажно то, что нервная система, помимо возможности большого выбора путей для достижения цели, способна избирательно усиливать или ослаблять сигналы.
Так, при усилении сигнала, обеспечивается надежная передача информации при частичной морфологической сохранности структуры, а при ослаблении сигнала – появляется возможность снизить помеху, идущую от других источников. Так как нервная система способна к избирательной фильтрации нужного сигнала, то это позволяет ей, выделив нужный, но слабый сигнал, во-первых, прямо усилить его, а во-вторых, дать ему преимущество при прохождении к воспринимающей структуре за счет снижения силы ненужных, мешающих сигналов.
Принципы иерархичности, иррадиации и концентрация активности. Структурная локализация функций предполагает, что мозг имеет детерминированные пути, системы, реализующие проведение сигнала, организацию той или иной реакции и т.д. Однако помимо жестко детерминированных связей в мозгу реализуются функциональные связи, развивающиеся в онтогенезе. Чем более упрочены, закреплены связи между структурами мозга в процессе индивидуального развития, тем труднее использование компенсаторных возможностей при патологиях.
На основе принципа структурности реализуется механизм иерархичности. Он заключается не столько в соподчинении, сколько в организации компенсаторных процессов. Каждая вышележащая структура участвует в реализации функций нижележащей, но делает это тогда, когда нижележащая структура затрудняется в выполнении своих функций.
Структуры мозга при обучении, при дисфункции одной из них не локализуют возбуждение в своих границах, а позволяют ему широко распространяться по мозгу – принцип иррадиации.
Иррадиация состояния активности распространяется в другие структуры мозга как по прямым связям, так и по опосредованным путям. Возникновение иррадиации при гипофункции структуры, участвующей в реализации того или иного процесса, позволяет найти пути компенсации гипофункции и реализовать нужную реакцию.
Нахождение нового пути закрепляется по рефлекторному принципу и заканчивается концентрацией активности в определенных структурах, заинтересованных в выполнении реакции.
Принцип общего конечного пути. С концентрацией активности в определенных структурах мозга тесно связаны конвергентность и принцип общего конечного пути. Этот принцип реализуется на отдельном нейроне и на системном уровне. В первом случае информация в нейроне собирается на дендритах, соме нейрона, а передается преимущественно через аксон в нейроны других структур мозга. Через синапсы дендритов информация передается только на соседние нейроны.
Наличие общего конечного пути позволяет нервной системе иметь разные варианты достижения нужного эффекта через разные структуры, имеющие выход на один и тот же конечный путь.
Трудности компенсаций, отмечаемые в более старших возрастах, обусловлены не тем, что резервы мозга исчерпаны, а тем, что сформировано большое количество оптимальных путей реализации функций, которые хотя и задействуются в случае патологии, но из-за нее же и не могут быть реализованы. Чаще при патологии требуется формирование новых путей реализации той или иной функции.
Пластичность нервных центров и отдельных нейронов. В основе формирования новых путей, новых функций структуры мозга лежит принцип пластичности. Пластичность позволяет нервной системе под воздействием различных стимулов осуществлять реорганизацию связей для целей сохранения основной функции или для реализации новой функции.
Пластичность позволяет нервным центрам реализовать функции, которые ранее им не были присущи, но благодаря имеющимся и потенциальным связям эти центры становятся способными участвовать в компенсации нарушенных в других структурах функций. Полифункциональные структуры обладают большими возможностями пластичности. В связи с этим неспецифические системы мозга, ассоциативные структуры, вторичные зоны проекций анализаторов, как имеющие значительное число полифункциональных элементов, более способны к пластичности, чем зоны первичных проекций анализаторов. Четким примером пластичности нервных центров является классический опыт П.К. Анохина с изменением связей центров диафрагмального и плечевого нервов.
В этом опыте были перерезаны диафрагмальный и плечевой нервы и центральный конец диафрагмального нерва был присоединен к периферическому концу плечевого, и, наоборот, центральный конец плечевого нерва к периферическому диафрагмального. По истечении некоторого времени после операции у животного восстанавливались правильная регуляция дыхания и правильная последовательность произвольных движений. Следовательно, нервные центры перестроили свою функцию таким образом, как этого требовала периферическая мышечная система, с которой была установлена новая связь. На ранних этапах онтогенеза перестройки такого типа более совершенны и динамичны.
Рефлекторный принцип функционирования. Наиболее существенную роль в компенсации дисфункций структур мозга играет рефлекторный принцип его функционирования. Каждая новая рефлекторная связь между структурами мозга является новым его состоянием, позволяющим реализовывать требуемую в данный момент функцию.
В настоящее время взаимодействие полушарий головного мозга понимается как взаимодополняющее, взаимно компенсирующее в реализации различных функций центральной нервной системы. Несмотря на то, что каждое полушарие выполняет ряд специфичных для него функций, нужно иметь в виду, что любая функция мозга, выполняемая левым полушарием, может быть выполнена и правым полушарием. Речь идет только о том, насколько успешно, быстро, надежно, полно формируются рефлексы.
PsyAndNeuro.ru
Все дороги ведут к моторной коре: психомоторные функции
Моторные vs. психомоторные функции
История изучения психомоторных нарушений с момента своего начала в первых годах XIX-го века представляет собой сложную и запутанную последовательность сменявших друг друга парадигм и концепций. Все началось с Wilhelm Griesinger, впервые представившего концепцию «психомоторных нарушений». Однако его последователи объединяли под этим термином немного разное: Emil Kraepelin – сенсомоторные нарушения, Karl Kahlbaum и August Hoch – психомоторную концепцию кататонии, Gilles de la Tourette – непроизвольные движения, Jean-Martine Charcot и Pierre Marie – двигательные симптомы истерического паралича. Затем Carl Wernicke и Karl Kleist описали так называемые «двигательные» и «циклоидные» психозы как два обособленных эпизодических состояния со своими психомоторными проявлениями. Однако за удивительно малое время – с появлением первых антипсихотиков в 1950-х – концепция подлинно психомоторных нарушений была практически забыта, и «все дороги стали вести» к исключительно моторным нарушениям. Только в 1960-х Karl Leonhard (ученик Karl Kleist) начал возвращать внимание к собственно психомоторным нарушениям.
Несмотря на то, что психомоторные нарушения являются одними из ключевых особенностей таких состояний, как большое депрессивное расстройство (БДР), биполярное аффективное расстройство (БАР) и шизофрения, в общепринятых современных диагностических классификациях (МКБ-10 и DSM-5) делается упор на когнитивные, аффективные и социальные симптомы, но не на психомоторные. В дименсиональной классификации RDoC двигательные симптомы психических заболеваний все же рассматриваются, однако в ней все же делается упор на связанные исключительно с двигательной функцией изменения дофаминергических кортико-стриато-паллидо-таламо-кортикальных моторных путей. В отличие от данных подходов, в нашей работе мы поставили цель возродить концепцию по-настоящему «психо-моторного» в буквальном смысле этого слова, показав специфические психомоторные (а не просто моторные) механизмы.
Что конкретно мы понимаем под термином «психомоторный»? Очевидно, что данное слово состоит из двух частей: «психо» и «моторный». В отличии от редуцирования первого компонента, т.е. «психики», в угоду второму, т.е. «моторному», как это часто происходит, мы постарались непосредственно оценить прямую связь между психическими и двигательными функциями и рассмотреть лежащие в основе данной связи нейробиологические механизмы. На нейрональном уровне психомоторные механизмы обуславливают то, как первичные моторные функции (т.е. дофаминергические субкортикально-кортикальные пути) модулируются немоторными функциями, то есть когнитивными и эмоциональными системами. С психологической точки зрения психомоторные механизмы обуславливают движения тела как результат некой психической активности, что необходимо для взаимодействия с окружением и объектами. Этот взгляд соотносится с первоначальным пониманием «психомоторного», подчеркивающим само взаимодействие аффективных, когнитивных и моторных функций. Как указано в названии нашей работы, мы покажем патофизиологические механизмы, посредством которых аффективные и когнитивные изменения, не связанные с двигательными зонами тем или иным образом (т.е., разными дорогами) приводят к дисфункции моторной коры и, соответственно, к появлению психомоторной симптоматики.
Цель данного обзора
В нашей работе мы стремились возродить традиционное понимание психомоторных феноменов как чего-то большего, чем просто двигательные нарушения. Ведь согласно данным последних исследований, нейрональные и биохимические механизмы, лежащие в основе психомторных нарушений, затрагивают гораздо большее число систем головного мозга, чем одна лишь дофаминергическая базально-таламо-кортикальная моторная петля. Мы построили свой обзор не по традиционной схеме, отталкиваясь от нозологий, а, скорее следуя концепции RDoC, сгруппировали информацию по различным психомоторным синдромам.
В данной работе мы приводим результаты МРТ-исследований БДР, БАР и шизофрении, посвященных поиску нейробиологических коррелятов психомоторных феноменов. В начале мы фокусируемся на том, как именно дофаминергическая субкортикально-кортикальная моторная система модулируется другими нейромедиаторными системами, в частности, серотониновыми путями (субкортикально-кортикальная модуляция). Затем мы описываем, как сенсомоторная сеть (sensorimotor network, SMN) и соответствующие двигательные функции модулируются другими, немоторными, сетями, в частности, сетью пассивного режима работы мозга (default mode network, DMN). Также мы описываем, как общая активность коры влияет на локальную активность моторных отделов коры (т.е. кортико-кортикальную модуляцию).
Субкортикальная модуляция моторной коры
Изменения в ядре шва модулируют активность субкортикально-кортикальных моторных путей
Одним из важных отделов ствола мозга, влияющих на дофаминергическую моторную сеть, является серотонинергическое ядро шва (raphe nucleus, RN). Так как в настоящее время опубликовано достаточно небольшое число работ, посвященных прямому влиянию ядра шва на моторную кору, в данном разделе мы также приводим данные фМРТ исследований самого ядра шва.
Han et al. в своем исследовании изучали функциональную связность в состоянии покоя (resting-state functional connectivity, rsFC (под этим термином понимают временную корреляцию изменения активности различных зон головного мозга; то есть, две зоны считаются более функционально связанными, если паттерны их возбуждения более синхронизированы, при условии, что обе эти зоны являются частями одной функциональной сети – прим. пер.)) ядра шва с остальными зонами мозга у пациентов с БАР и БДР. Оказалось, что при БАР и при БДР наблюдаются противоположные паттерны rsFC ядра шва с остальными субкортикальными регионами, в частности, с таламусом и скорлупой. Кроме того, при биполярном расстройстве rsFC гипоталамуса была повышена, а при депрессии, наоборот, снижена. Эти находки были подкреплены результатами исследования Anand et al., в котором было обнаружено значимое снижение rsFC ядра шва с префронтальной корой и средней поясной извилиной при БДР. Кроме того, показатель rsFC ядра шва с гиппокампом и миндалиной коррелировал с выраженностью депрессивных симптомов. Наконец, Wohlschlager et al. пошли дальше исследования rsFC и изучили спектральные характеристики инфрамедленных колебаний (0,01-0,1 Гц) активности ядра шва и вентральной зоны покрышки (ventral tegmental area, VTA) у пациентов с БДР, не получавших терапию. Было обнаружено, что в обеих зонах происходит существенное усиление более низкочастотной активности, что также прямо коррелировало с выраженностью депрессивной симптоматики.
Все эти данные свидетельствуют, что при депрессии имеют место определенные изменения в самом ядре шва, а также в его связях с субкортикальными моторными зонами (таламусом и базальными ганглиями) и различными немоторными зонами коры. Однако в настоящее время крайне мало исследований, посвященных возможным функциональным изменениям ядра шва и его rsFC, а также серотонинергической дисфункции, при шизофрении. Тем не менее, в указанных выше исследованиях предполагалось, что аномалии функциональных связей ядра шва (как центральной структуры серотонинергической системы) с другими субкортикальными и кортикальными регионами могут являться трансдиагностическими феноменами. Все это оставляет открытым вопрос о связи этих аномалий с моторной функцией и особенно с психомоторными симптомами.
Модуляция дофаминовых субкортикально-кортикальных моторных путей ядром шва и серотонином в здоровом мозге
Влияет ли серотониновое ядро шва на дофаминергические субкортикально-кортикальные пути и моторные функции? Conio et al. на основе данных фармакологических, структурных и функциональных МРТ-исследований продемонстрировали наличие сложных взаимодействий между серотонином и дофамином, а также влияние этих взаимодействий на активность головного мозга. В частности, было показано, что дофаминергическая черная субстанция соединена, в основном, с сенсомоторной сетью (а VTA – с сетью салиентности (salience network, SAN). Однако серотонинергическое ядро шва имеет связи как с сенсомоторной сетью, так и с сетью пассивного режима работы мозга. Помимо различных связей дофаминовых и серотониновых ядер ствола мозга, активность дофаминовых путей приводит к усилению активности SMN, а активность серотонинергических путей, наоборот, к уменьшению активности SMN и усилению активности DMN. Более того, rsFC черной субстанции прямо коррелировали с активностью SMN, а rsFC ядра шва коррелировали с активностью SMN обратным образом. Martino et al. в своем исследовании показали, что у здоровых испытуемых rsFC между таламусом и SMN модулируются функциональными связями как от ядра шва, так и от черной субстанции, но противоположным образом. Иными словами, связи от черной субстанции способствуют большей синхронизации активности между таламусом и SMN, а связи от ядра шва, наоборот, уменьшают эту синхронизацию. Таким образом, на основании этих данных можно утверждать, что серотонин ядра шва и дофамин черной субстанции диаметрально противоположным образом влияют на активность моторных зон коры, в частности, на SMN. Дофаминовые сигналы усиливают активность SMN и ее синхронизацию с активностью таламуса, а серотониновые сигналы, наоборот, приводят к «антикорреляции» SMN и таламуса и снижению активности SMN.
Таким образом, отвечая на вопрос, поставленный в начале раздела, можно утверждать, что ядро шва и серотонин действительно модулируют дофаминовые субкортикально-кортикальные пути. Соответственно, дофаминовые пути от черной субстанции и серотониновые пути от ядра шва можно расценивать не как первично моторные пути сами по себе, а скорее как модуляторы психомоторных функций.
Модуляция дофаминовых субкортикально-кортикальных моторных путей ядром шва и серотонином при депрессии, БАР и шизофрении
Основываясь на данных, полученных при исследовании здоровых испытуемых, можно предположить, что психомоторное торможение, в основе которого лежит сниженная активность SMN, должно быть обусловлено уменьшением rsFC черной субстанции и/или увеличением rsFC ядра шва. Подобные феномены действительно наблюдаются у пациентов с психомоторным торможением в депрессивной фазе БАР. Для таких пациентов характерно уменьшение rsFC таламуса и SMN и черной субстанции с таламусом/базальными ганглиями, а также конкурентное уменьшение rsFC ядра шва с базальными ганглиями/таламусом. Вместе эти паттерны способствуют «отсоединению», то есть, рассинхронизации активности таламуса и SMN, с последующим торможением активности SMN и возникновением психомоторного торможения. Эти находки согласуются с результатами исследования Yin et al., в котором было продемонстрировано снижение кровотока в моторной коре при психомоторном торможении у пациентов с БДР.
Для пациентов с манией, наоборот, характерны практически диаметрально противоположные изменения. У данных пациентов наблюдалось уменьшение rsFC ядра шва с таламусом/базальными ганглиями, а также, в отличие от пациентов с депрессией, rsFC черной субстанции была сохранна. Все вместе это приводит к увеличению rsFC таламуса с SMN, усилению активности SMN и последующей психомоторной ажитации.
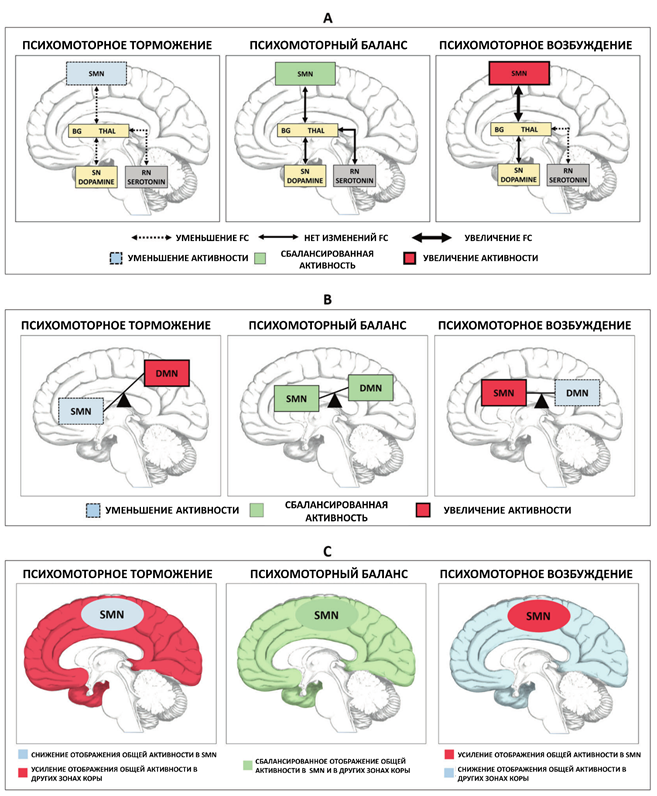
Таким образом, данные этих исследований свидетельствуют о наличии реципрокного баланса между дофаминергическими связями базальных ганглиев/таламуса с SMN с одной стороны и серотонинегической модуляцией этих связей ядром шва с другой стороны. Уменьшение активности серотонинергических путей от ядра шва до базальных ганглиев приводит к большей «связанности» талаумса c SMN, что приводит к психомоторному возбуждению. Уменьшение же активности дофаминергических путей от черной субстанции до базальных ганглиев, напротив, уменьшает «связанность» таламуса с SMN и приводит к возникновению психомоторного торможения. Если эти два плеча модуляции связей таламус-SMN, дофаминергическое и серотонинергическое, уравновешены, то психомоторная функция «нормальная», то есть, не ускорена и не замедлена. Если же этот баланс нарушается, то таламус и SMN становятся либо чрезмерно, либо недостаточно функционально связанны, что приводит либо к психомоторному возбуждению (например, при мании), либо к психомоторному торможению (при депрессии). Подробнее см. Рис. 1А.
Рис. 1. Биохимическая и нейрональная модуляция субкортикально-кортикальных и кортико-кортикальных механизмов психомоторных феноменов. А. Модуляция дофаминергической субкортикально-кортикальной моторной цепи ядром шва и серотонином. B. Модуляция сенсомоторной сети (SMN) сетью пассивного режима работы мозга (DMN). С. Модуляция отображения общей активности в SMN. SN – черная субстанция, RN – ядро шва, Thal – таламус.
Модуляция дофаминовой субкортикально-кортикальной моторной петли ядром шва/серотонином и другими нейромедиаторными системами – дименсиональный и транснозологический подход
Следующий вопрос, на который необходимо ответить, звучит следующим образом: можно ли соотнести серотониновую модуляцию моторной петли с различными диагностическими категориями, или, формулируя иначе, можно ли ее соотнести с различными степенями психомоторных нарушений? Своеобразной «лакмусовой бумажкой», способной помочь ответить на данные вопросы, является феномен психомоторного возбуждения при депрессии. Martino et al. отдельно исследовали пациентов в депрессивной фазе БАР с психомоторным возбуждением и сравнивали их с соответствующими пациентами с психомоторным торможением. Оказалось, что у депрессивных пациентов с психомоторным возбуждением наблюдается паттерн, схожий с тем, что имеет место при мании: при обоих состояниях наблюдается усиление rsFC таламуса с SMN, что, соответственно, приводит к усилению активности SMN и психомоторному возбуждению.
Еще одно доказательство дименсиональной и транснозологической природы двусторонней «от ядра шва и от черной субстанции) модуляции активности субкортикально-кортикальной моторной петли следует из результатов недавнего исследования шизофрении. Авторы изучали две группы пациентов с шизофренией – с психомоторным возбуждением и с психомоторным торможением – и сравнивали их соответственно с группами пациентов с БАР в фазе мании (и с психомоторным возбуждением) и в фазе депрессии (с сопутствующим психомоторным торможением). Оказалось, что для пациентов, страдающих шизофренией с психомоторным торможением, характерен почти тот же паттерн изменений таламо-сенсомоторной rsFC, что и для пациентов, страдающих депрессией с психомоторным торможением, то есть, снижение rsFC таламуса с SMN и сопутствующее уменьшение rsFC ядра шва и черной субстанции с базальными ганглиями и таламусом. Аналогичное совпадение наблюдалось и у пациентов, страдающих шизофренией с психомоторным возбуждением. Наблюдаемые у таких пациентов усиление rsFC таламуса c SMN и уменьшение rsFC только ядра шва с базальными ганглиями и таламусом аналогичны соответствующим изменениям у пациентов в маниакальной фазе БАР с психомоторным возбуждением.
Хрестомайтиным примером психомоторного синдрома является кататония, являющаяся по-настоящему трансдиагностическим феноменом. Кататония может встречаться при шизофрении, БАР, БДР и при других заболеваниях. Развитие кататонии является результатом дисфункции сразу нескольких нейромедиаторных систем. Действительно, кататония, в первую очередь, проявляется двигательными нарушениями, связанными с изменениями активности сенсомоторных субкортикально-кортикальных зон. Однако кататония также характеризуется аффективными нарушениями, связанными с изменениями в немоторных зонах коры (например, с нарушениями функционирования лобно-теменных связей), что подчеркивает истинно психомоторную природу этого феномена. Соответственно, наряду с гипоактивацией дофаминергических рецепторов, при кататонии наблюдаются нарушения в других нейромедиаторных системах: гипоактивация серотониновых (5-HT2A) рецепторов, дисбаланс между активностью ГАМКА (гипоактивация) и ГАМКВ (гиперактивация) рецепторов и, вероятно, также гиперактивация глутаматных NMDA-рецепторов. С одной стороны, лоразепам и золпидем (аллостерические модуляторы ГАМКА-рецепторов) усиливают возбудимость ГАМК-ергических ингибиторных сетей в моторной коре и, таким образом, способствуют облегчению симптомов кататонии. С другой стороны, баклофен и вальпроевая кислота могут усиливать активность ГАМКв- и NMDA-рецепторов и, наоборот, усилить выраженность кататонии. Тем не менее, все же существуют некоторые данные о положительном влиянии вальпроевой кислоты, топирамата и карбамазепина на аффективные кататонические симптомы (предположительно, усиливая восприимчивость ГАМК и NMDA). Наконец, клозапин (антагонист 5-HT2A-рецепторов и агонист ГАМКB-рецепторов) компенсирует серотонинергическую гипоактивацию дисбаланс активности ГАМКA-B и, таким образом, согласно некоторым исследованиям, может уменьшать выраженность кататонии.
Другим примером транснозологического психомоторного синдрома служит паркинсонизм (сочетание тремора, ригидности и брадикинезии), являющийся, главным образом, следствием болезни Паркинсона, первично нейродегенеративной по своей природе. Однако явления паркинсонизма могут быть ассоциированы и с другими заболеваниями (например, паркинсонизм может наблюдаться у больных шизофренией). Болезнь Паркинсона, в первую очередь, характеризуется дегенерацией дофаминергических клеток черной субстанции и стриатума, однако было обнаружено, что при данном заболевании также нарушается активность серотонинергической системы. Так, при болезни Паркинсона имеет место снижение количества серотониновых транспортеров в ядре шва, что прямым образом ассоциировано с тяжестью тремора. Кроме того, при болезни Паркинсона затронуты также другие нейромедиаторные системы. Известно, что модуляторы ГАМКергической системы (золпидем и клоназепам), амантадин, антихолинергические препараты и клозапин могут улучшать двигательную симптоматику болезни Паркинсона. У пациентов с шизофренией, страдающих паркинсонизмом, наблюдаются характерные изменения объема серого вещества и активности фронто-таламических/мозжечковых и кортикальных соматосенсорных сетей, не свойственные пациентам без паркинсонизма. Эти факты дают возможность предположить существование восходящей модуляции моторных отделов коры как центрального нейронального механизма возникновения паркинсонизма при шизофрении.
Наконец, психомоторные нарушения могут наблюдаться и при других заболеваниях, в частности, при аутизме. Стоит отметить, что имеются данные об ассоциированных с данным расстройством изменениях активности дофаминергической, серотонинергической (повышенный синтез серотонина), ГАМКергической и глутаматергической систем в моторной и соматосенсорной коре, а также в стриатуме. Соответственно, блокаторы дофаминовых рецепторов, ингибиторы обратного захвата серотонина, мемантин, вальпроевая кислота, арбаклофен и акампросат в некоторых исследованиях демонстрируют эффективность в уменьшении выраженности таких психомоторных симптомов аутизма, как стереотипии, импульсивность и раздражительность.
Все эти результаты ясно демонстрируют, что модуляция ядром шва и серотонином субкортикально-кортикальной моторной петли представляют собой явление, простирающееся за рамки каких-то конкретных нозологических категорий. Она соответствует скорее направленности и выраженности психомоторных нарушений, а не какому-то конкретному диагнозу, являясь, таким образом, по-настоящему дименсиональным и транснозологическим феноменом.
Кортикальная модуляция моторной петли
Модуляция моторной петли другими корковыми сетями
Кора головного мозга включает в себя различные нейронные сети: сеть пассивного режима работы мозга (DMN), сенсорные сети (зрительная, слуховая, соматосенсорная), сенсомоторная сеть (SMN), фронтопариетальная сеть, сеть салиентности, сети внимания и многие другие. Недавние исследования показали, что все эти сети функционально взаимосвязанны. К примеру, DMN и фронтопариетальная сеть противоположности по своей активности: функциональное усиление активности одной прямо приводит к угнетению активности другой и наоборот. Что особенно интересно, SMN также, по-видимому, находится в реципрокных отношениях с другими сетями, в частности, с DMN и сенсорными сетями. В исследовании Martino et al. было продемонстрировано, что увеличение нейрональной вариабельности (вариабельность амплитуды сигнала от определенной популяции нейронов; считается, что чем выше нейрональная вариабельность, тем более активна данная популяция нейронов – прим пер.) в DMN ассоциировано с уменьшением этого параметра в SMN даже у здоровых людей.
Так же, как и в случае с субкортикальной модуляцией, это реципрокное взаимодействие в крайней степени выражено у пациентов с БАР в фазе депрессии и мании. У пациентов в депрессивной фазе наблюдается аномально высокая нейрональная вариабельность в DMN, что, следуя реципрокному механизму, сопровождалось снижением нейрональной вариабельности в SMN. Изменение этих параметров коррелировало с выраженностью симптоматики: чем больше была нейрональная вариабельность в DMN по сравнению с SMN, тем более выраженными были депрессивные симптомы. Интересно, что у пациентов в маниакальной фазе, наоборот, была снижена нейрональная вариабельность в DMN и, соответственно, повышена в SMN. Это также коррелировало с маниакальной симптоматикой: чем больше была вариабельность SMN по сравнению с DMN, тем более выраженные симптомы мании наблюдались у пациента. Стоит подчеркнуть, что именно отношение вариабельностей DMN/SMN коррелировало с тяжестью симптомов, но не абсолютные значения данных показателей сами по себе.
В другом исследовании Northoff et al. исследовали нейрональую вариабельность в SMN и в зрительной сети у пациентов с БАР. Авторы обнаружили, что при мании увеличение вариабельности в SMN сопровождалось уменьшением таковой в зрительной сети. Обратная картина наблюдалась при депрессии: снижение вариабельности в SMN и увеличение таковой в зрительной сети. Авторы связывали этот баланс с «внутренним» и «внешним» восприятием скорости времени. «Внутреннее» восприятие определялось активностью SMN и субкортикально-кортикальной моторной петли, в то время как «внешнее» – сенсорными областями, в том числе, зрительной сетью. Если взять степень нейрональной вариабельности в качестве показателя, отражающего восприятие времени (увеличенная вариабельность свидетельствует о большем изменении активности нейронов за единицу времени и, соответственно, об «ускорении» времени на нейрональном уровне), то можно сказать, что для пациентов с депрессией свойственно замедление «внутреннего» времени, то есть, аномальное «внутреннее замедление» (являющееся следствием уменьшения нейрональной вариабельности в SMN). Для пациентов же с манией, наоборот, характерно субъективное «ускорение» вследствие увеличенной вариабельности в SMN. Вопрос о том, каким образом эти аномалии «внутреннего времени» трансформируются в психомоторные нарушения и трансформируются ли вообще, пока остается открытым.
Данные исследования наглядно демонстрируют, что нейрональная активность в моторной коре и SMN зависит не только от субкортикальных влияний ядра шва и черной субстанции, но и от активности других, немоторных сетей коры. Самым ярким доказательством этого является реципрокное взаимодействие между DMN и SMN, а также модуляция SMN сенсорными сетями. Тем не менее, механизмы, посредством которых подобная реципрокная кортико-кортикальная модуляция ассоциирована с психомоторными функциями, еще только предстоит исследовать.
Модуляция локально-региональной активности моторной коры общей корковой активностью
Традиционно мы измеряем нейрональную активность локально, то есть, в какой-то конкретной области (амплитуда сигнала от области), либо в какой-то конкретной сети (синхронизация между собой различных отделов сети, оцениваемая при помощи rsFC). Однако в дополнение к этим локальным методам существуют также методы, позволяющие оценить активность мозга в общем. Одним из таких методов является определение rsFC между целыми нейронными сетями, например, между DMN и SMN. Кроме того, если взять вместе все межрегиональные и межсетевые связи, можно получить так называемый «глобальный сигнал», оцениваемый при помощи фМРТ. Глобальный сигнал вычисляется как среднее от всех rsFC по всему головному мозгу и отражает степень, в которой синхронизированы между собой различные области и сети, то есть глобальную синхронизацию мозга. Исследования демонстрируют, что степень, в которой та или иная область или сеть синхронизирована с остальными частями мозга, различается у разных отделов. Например, нейрональная активность в SMN более синхронизирована с общей активностью мозга (и, соответственно, демонстрирует больший глобальный сигнал на фМРТ), чем DMN, чьи отделы, по-видимому, работают более обособленно, то есть десинхронизированно (что выражается более низким глобальным сигналом на фМРТ).
В настоящее время имеются сообщения об изменениях глобального сигнала при различных психических расстройствах. Yang et al. продемонстрировали, что у пациентов с шизофренией значимо выше глобальный сигнал по сравнению с пациентами с БАР и здоровыми испытуемыми. Это означает, что общая синхронизация активности между отдельными зонами/сетями мозга аномально высокая у пациентов с шизофренией (однако в другом исследовании Argyelan et al., наоборот, продемонстрировали снижение глобальной синхронизации у пациентов с шизофренией). Более того, было обнаружено, что при шизофрении глобальная активность становится менее синхронизированной с активностью отделов/сетей низкого порядка, особенно сенсорных зон. Напротив, глобальная активность становится более синхронизированной с активностью зон высокого порядка. Wang et al. дополнили эти данные, показав, что синхронизация отдельных сетей с общей активностью мозга является динамическим, изменяющимся во времени, процессом: сначала глобальная активность синхронизируется с сенсорными сетями, затем с DMN, а после уже и с остальными сетями. Эта последовательность синхронизации глобальной активности мозга с отдельными зонами/сетями, по-видимому, нарушается при шизофрении.
В другом исследовании Zhang et al. изучали глобальный сигнал у биполярных пациентов в маниакальной, депрессивной и в эутимной фазах. Было обнаружено, что у пациентов с БАР в депрессивной фазе усилена синхронизация глобальной активности мозга с гиппокампом, что может быть ассоциировано с более частым «вызовом из памяти» автобиографических воспоминаний. Кроме того, оказалось, что у пациентов в мании глобальная активность сильно синхронизирована с активностью моторной коры, что отражает характерную для данных пациентов большую психомоторную активность. Последняя находка особенно подчеркивает, что синхронизация глобальной активности является настоящим психомоторным механизмом: изменения в моторной коре вызывают не связанные с субкортикально-кортикальной моторной петлей изменения общей активности мозга.
Ограничения
У данного обзора имеются следующие важные ограничения. Во-первых, обозреваемые работы сильно отличаются друг от друга по диагностическим группам, подходам к определению психомоторных нарушений и нейровизуализационным техникам. Во-вторых, разнообразие подходов и методик вкупе с небольшим количеством исследований не дали нам возможность провести полноценный ALE-мета-анализ (activation likelihood estimation – подход к мета-анализу нейровизуализационных исследований, заключающийся в определении вероятности того, что выявляемые в однородных экспериментах зоны высокой активности коры действительно совпадают – прим. пер.). В-третьих, в силу разнообразия терминологии, относящейся к концепции «психомоторного», мы могли пропустить часть важных исследований. Исходя из перечисленных выше причин, мы считаем необходимым проведение дальнейших трансдиагностических лонгитудинальных нейровизуализационных исследований психомоторных нарушений с использованием стандартизированных методов.
Заключение
В данном обзоре были показаны различные нейрональные механизмы, лежащие в основе психомоторных симптомов при различных психических заболеваниях. Это является своего рода продолжением классического взгляда на психомоторные синдромы, актуальным в настоящее время, так как было продемонстрировано, что нейрональные и биохимические механизмы возникновения психомоторных нарушений не ограничиваются дофаминовой субкортикально-кортикальной моторной петлей. Мы выявили три трансдиагностических нейробиологических механизма, лежащих в основе психомоторных функций. 1) модуляция серотонином и ядром шва дофаминергической субкортикально-кортикальной моторной петли; 2) реципрокный баланс между сетью пассивного режима работы мозга, сенсомоторной и сенсорными сетями; 3) локальная синхронизация сенсомоторной сети c глобальной активностью головного мозга.
Эти механизмы в основе своей довольно похожи. Во-первых, все три механизма зависит не от каких-то абсолютных значений, а от относительных показателей, то есть, от баланса между какими-либо параметрами. Мы столкнулись с тремя видами нейронного баланса, относящимися к различным уровням проявления психомоторных функций: 1) баланс между rsFC ядра шва и черной субстанции; 2) баланс между активностью сети пассивного режима работы мозга и соматосенсорной сети; 3) баланс между глобальной активностью мозга и локальной активностью соматосенсорной сети. Кроме того, мы выявили различные виды биохимического баланса, например, между дофамином и серотонином, формирующие психомоторные функции посредством модуляции субкортикально-кортикальных и кортико-кортикальных нейронных балансов.
Во-вторых, разобранные нами данные свидетельствуют о дименсиональной и транснозологической природе психомоторных механизмов, имеющих место не только при различных заболеваниях (например, при шизофрении, БАР или депрессии), но и в норме. Соответственно, психомоторные механизмы являются иллюстрацией преимуществ применения дименсионального транснозологического синдромного подхода (как это сделано, в частности, авторами RDoc)
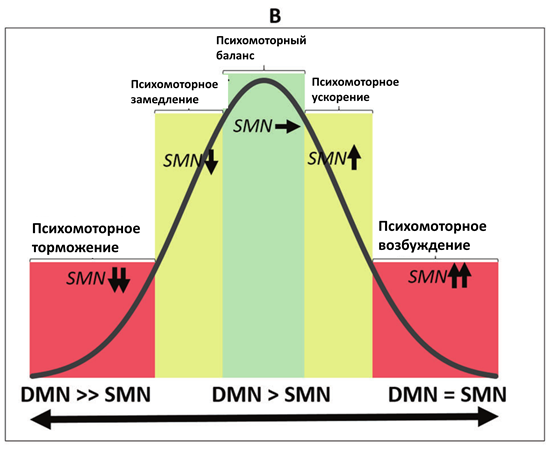
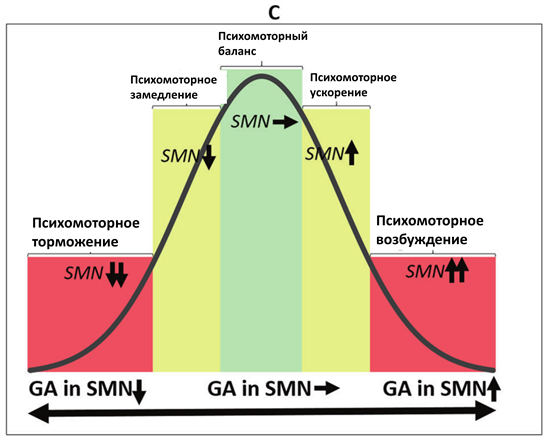
В-третьих, данные примеры демонстрируют континуум здоровых и патологических психомоторных состояний, в которых задействован один и тот же механизм, но проявляющийся в различной степени. В рамках данного континуума норма соответствует средним значениям, в то время как патологические состояния расположены на противоположных концах, что, таким образом, формирует кривую в форме перевернутой буквы U (см. Рис.2)
Рис.2. Перевернутые U-образные кривые континуума различных нейробиологических механизмов психомоторной активности. А. Континуум различных видов баланса между функциональной связностью ядра шва (RN) и черной субстанции (SN) с таламусом (Thal) и его связи с сенсомоторной сетью (SMN), определяющей ее активность. B. Континуум различных видов баланса между активностью SMN и сетью пассивного режима работы мозга (DMN), определяющего уровень активности SMN. C. Континуум различных видов баланса между глобальной активностью мозга (GA) и уровнем активности SMN.
В-четвертых, первернутая U-образная кривая демонстрирует, что именно средние показатели различных видов нейробиологического баланса являются наиболее оптимальными. В отличие от них, крайние формы смещения баланса являются дисфункциональными, приводящими к нарушению психомоторных функций.
В-пятых, с клинической точки зрения психомоторные нарушения могут быть охарактеризованы специфическим набором симптомов, то есть, сочетанием определенных двигательных, аффективных и когнитивных нарушений. Например, психомоторное возбуждение может сопровождаться эмоциональными нарушениями (например, повышенными аффектом) и когнитивными нарушениями (в частности, нарушениями внимания). В то же время психомоторное торможение часто сопровождается негативными эмоциями и усилением внимания на самом себе. Подобные конструкции симптомов позволяют предположить наличие связей между субкортикально-кортикальной моторной системой и немоторными, аффективными и когнитивными, нейронными системами, что подтверждается, например, существованием реципрокных взаимодействий между SMN, DMN и сенсорными сетями.
Наконец, все перечисленные механизмы имеют потенциальное диагностическое и терапевтическое значение. Они могут применяться для ранней диагностики пограничных состояний и манифеста психических заболеваний, служить потенциальными биомаркерами терапевтического ответа и быть мишенями неинвазивных методов стимуляции головного мозга (транскраниальной магнитной стимуляции и др.) Несмотря на то, что при помощи этих методов может проводиться стимуляция разных отделов мозга, все они тем или иным образом повлияют на активность субкортикально-кортикальной моторной петли и уменьшать выраженность психомоторных нарушений. Как и в случае с Римом, все дороги, в конечном счете, ведут к моторной коре.
Автор перевода: Кибитов А.А.