Талидомидовая трагедия 60 лет назад. Ошибка фармацевтов сделала инвалидами тысячи детей
25 декабря 1956-го, г. Штольберг. У сотрудника фармацевтической компании Chemie Grünenthal большой праздник — его жена рожает. Однако скоро радость сменяется ужасом. Младенец родился без ушей и носа. Спустя шесть лет в 52 странах будет зарегистрировано ещё 12 000 похожих случаев. По всему миру дети появляются на свет с мутациями. Позже выяснится, что их матери принимали один и тот же препарат. Историки назвали этот случай «талидомидовой трагедией» — в честь, как казалось поначалу, безобидного лекарства.
Отмотаем время назад. Как и многие другие ужасы XX в., история талидомида берёт своё начало в нацистской Германии. До войны Герман Виртц производил мыло, духи и другую бытовую химию. На бизнесе немец сколотил капитал. После войны — в 1946 г. — Виртц нанимает полдюжины технических специалистов и учёных, с которыми открывает фармацевтическую компанию Chemie Grünenthal.
В конце концов в команду Chemie Grünenthal вступил Мартин Штеммлер, один из самых рьяных последователей идеи расовой гигиены и евгеники в Третьем рейхе. Штеммлер возглавил патологическое отделение в новоиспечённой фирме Германа Виртца.
Секс любой ценой. Чем пользовались мужчины до изобретения виагры
Несмотря на своё прошлое, смертоносное трио собралось не ради продолжения своих злодеяний. Объединившись под вывеской Chemie Grünenthal, учёные приступили к созданию недорогих антибиотиков. Иии… не преуспели. Зато команда синтезировала талидомид.
Фото © Getty Images
Изначально свойство препарата определялось как противосудорожное. Но опыты на животных этого не подтвердили. Впрочем, одно полезное свойство за талидомидом всё же было замечено — лошадиные дозы микстуры не убивали даже лабораторных мышей.
Фото © Getty Images
Оба эти аргумента фармацевтическая компания использовала при лицензировании продукта. В 1957 г. препарат начал свободно распространяться в ФРГ. Он позиционировался как «чудо-средство» от бессонницы, головной боли, кашля, тошноты и даже простуды. Уже в 1958 г. талидомид в чистом виде и в составе других лекарств (от астмы, повышенного давления и т.д.) появился в 45 других странах Европы, Азии, Африки и в Южной Америке. В некоторых регионах, в том числе и в ФРГ, новинка по популярности уступала только аспирину. Люди упивались чудо-пилюлями. При этом дополнительные исследования не проводились.
Однажды в офис Chemie Grünenthal бог весть от какого врача пришёл отзыв о новом лекарстве. В нём говорилось, что талидомид — лучшее средство для беременных, поскольку подавляет тошноту, снижает раздражительность и вызывает здоровый сон. Британский дистрибьютор лекарства тотчас начал использовать тезис в рекламе. Случился новый бум популярности. Это была трагедия, с последствиями которой людям только предстояло столкнуться.
Фото © Getty Images
Изомерия — это явление, при котором химические соединения могут иметь одинаковый атомный состав, но различаться по расположению тех же самых атомов. Видов изомерии бывает несколько. Сейчас нужно разобраться только с одной — оптической.
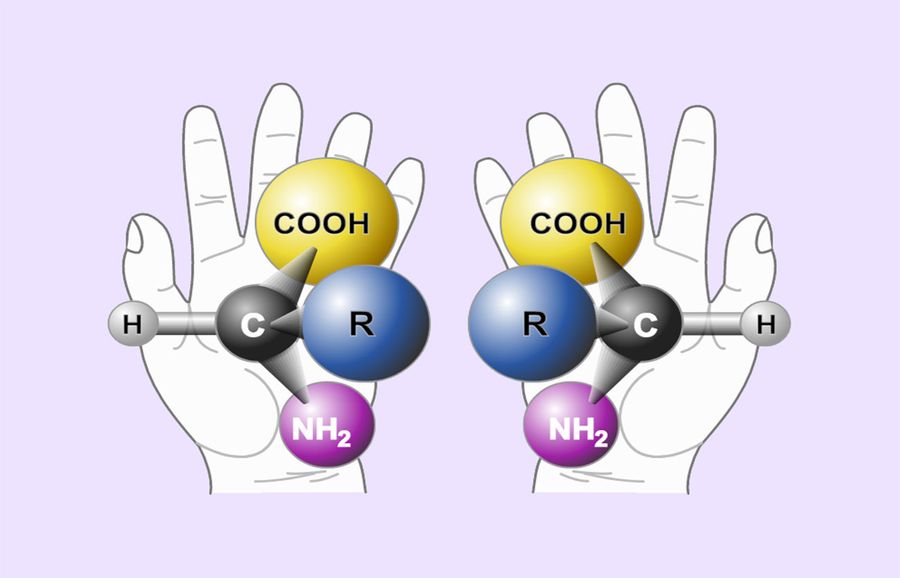
При оптической изомерии две молекулы одного и того же вещества обладают одинаковыми свойствами, но их строение несимметрично относительно левой и правой стороны. Чтобы лучше это представить, нужно взглянуть на кисти рук. Их строение одинаково, но асимметрично относительно сторон. В противном случае у людей было бы две левые или правые руки.
Так вот, молекула талидомида может состоять из двух оптических изомеров. Один из которых вращается вправо, а другой — влево. Только один изомер из этой пары оказывает успокаивающий эффект. Тогда как второй вклинивается в ДНК эмбриона и нарушает естественное деление клеток. Последнее и приводит к всевозможным уродствам.
Обстрел из космоса. Что стало с людьми, на которых упал метеорит: 3 реальные истории
Описанное свойство называется тератогенным действием. Как несложно догадаться, открыто оно было только после «талидомидовой трагедии». До неё влияние лекарств на плод не изучалось. На момент разработки талидомида учёные попросту не верили, что лекарство может пройти через плацентарный барьер.
В действительности же чудо-таблетка чхала на убеждения учёных. Применение талидомида на 20-й день беременности приводит к поражению мозга у плода. На 21-й день препарат нарушает формирование глаз. На 22-й день — страдают уши и лицо. С 24-го по 28-й дни — руки и ноги. Использование талидомида после 42-го дня беременности плоду вроде как уже не вредит.
Сглупили родители — расплатились дети
Фото © Getty Images
Дети-мутанты начали появляться ещё до разрешения талидомида в ФРГ. Как мы отметили в самом начале, первой по иронии судьбы пострадала семья сотрудника Chemie Grünenthal. Не подозревая о пагубных последствиях, он рекомендовал своей супруге пить экспериментальные пилюли перед сном. Впрочем, в 1956 г. никому и в голову не пришло провести связь между лекарством и уродствами ребёнка.
В Европе на корреляцию обратили внимание только несколько лет спустя. В конце 1961 г. «эпидемию» уродств, вызванную успокаивающим средством, подсветили педиатры в Германии, Австралии и Великобритании. Публикации в СМИ вызвали скандал. На тот момент талидомид присутствовал уже на рынках 52 стран. Со всех его начали отзывать. Но было поздно.
По разным данным, с 1956 по 1961 г. из-за талидомида на свет появилось от 8 до 12 тыс. младенцев с мутациями. За всё время изобретение Chemie Grünenthal сгубило десятки тысяч невинных. «Талидомидовая трагедия» считается одной из крупнейших антропогенных катастроф в истории. Важно подчеркнуть, что до своего первого дня рождения не доживало 40% детей с мутациями.
Невероятная история. Малоизвестные факты из прошлого
Атомный апокалипсис. Как возродилась Хиросима после бомбардировки 75 лет назад — фотогалерея
6 августа 2020, 14:30
2 августа 2020, 17:00
Как и за что на Руси и в средневековой Европе наказывали женщин
1 августа 2020, 14:00
Ведь деформация конечностей, дефекты глаз и мимической мускулатуры — это только внешние проявления последствий талидомида. Но внутренние органы тоже страдают: сердце, печень, почки, пищеварительная и мочеполовая системы.
Никто не виноват — так получилось
Параллельно отзыву лекарства (конец 1961 г.) на Chemie Grünenthal, само собой, посыпались судебные иски. Как гражданские, так и уголовные. Материалов было настолько много, что суд начался только в 1968 г. Папки с делом насчитывали 972 страницы. И это только в ФРГ. Процесс длился до 1970 г.
Фото © ТАСС / Picture alliance / Horst Ossinge
В ходе расследования выяснилось, что в Chemie Grünenthal знали о некоторых побочных эффектах задолго до скандала. Но в ответ на опасения дистрибьюторов и некоторых врачей фармацевтическая компания преуменьшала проблему.
— Более миллиона людей в одной только Западной Германии принимают Contergan (название талидомида в ФРГ) каждый день. Мы слышали о случайных реакциях, которые, скорее всего, являются аллергией. Все негативные последствия исчезают у пациентов сразу после прекращения приёма, — гласит ответ Chemie Grünenthal пациентам, у которых на фоне регулярного применения талидомида развивался периферический неврит, ещё один побочный эффект.
Стало известно и то, что фармацевты покупали позитивные отзывы о препарате и платили тем, кто критиковал недовольных. После отзыва пилюль в одних странах Chemie Grünenthal до последнего оттягивала такое же решение в других. В некоторых источниках даже утверждается, что компания изначально знала о влиянии вещества на беременных. Мол, талидомид синтезировали ещё в нацистской Германии и планировали использовать в качестве антидота для зарина. Косвенно это подтверждают только воспоминания солдат, которые видели изуродованных детей во время освобождения узников концлагерей.
Талидомид
формула
группа
(по состоянию на 17.01.08) [1]
Талидомид — седативное снотворное лекарственное средство, получившее широкую известность из-за своей тератогенности, после того, как было установлено, что в период с 1956 по 1962 годы в ряде стран мира родилось по разным подсчётам от 8000 до 12 000 детей с врождёнными уродствами, обусловленными тем, что матери принимали препараты талидомида во время беременности. Талидомидовая трагедия заставила многие страны пересмотреть существующую практику лицензирования лекарственных средств, ужесточив требования к лицензируемым препаратам.
В настоящее время талидомид применяется для лечения проказы, а также множественной миеломы и других тяжёлых онкозаболеваний.
Содержание
История
Разработка и появление на рынке
В 1954 году немецкая фармацевтическая компания Chemie Grünenthal проводила исследования с целью разработать недорогой способ производства антибиотиков из пептидов. В ходе исследований работникам компании был получен препарат, названный ими талидомид (thalidomide), после чего начались изучения его свойств для определения сферы его применения.
Изначально талидомид предполагалось использовать как противосудорожное средство, однако первые опыты на животных показали, что подобными свойствами новый препарат не обладает. Однако было обнаружено, что передозировка препарата не убивала подопытных животных, что дало основание считать препарат безвредным.
В 1955 году Chemie Grünenthal неофициально выслала бесплатные образцы препарата разным докторам Германии и Швейцарии.
Люди, принимавшие препарат, отметили, что, хоть он и не проявляет противосудорожных свойств, он оказывает успокаивающий и снотворный эффект. Принимавшие препарат люди рассказывали, что они испытали глубокий «естественный» сон, длящийся всю ночь. [2]
Действие препарата впечатлило многих терапевтов, безопасное успокаивающее и снотворное средство выделялось на фоне существующих снотворных препаратов. Безопасность передозировки (случайной или при попытке суицида) препарата особо отмечалась в дальнейшем при продвижении этого продукта на рынке.
Несмотря на то, что препарат оказывал на людей подобное воздействие, для его лицензирования необходимо было показать эффективность его действия. Однако, на животных препарат седативного воздействия не оказывал, поэтому представителям компании Chemie Grünenthal для демонстрации пришлось изготовить особую клетку, которая служила для измерения малейших движений подопытных животных. Таким образом представители Chemie Grünenthal сумели убедить комиссию, что, несмотря на то, что мыши после приёма препарата бодрствовали, их движения замедлялись в большей степени, чем у животных, которым ввели другие седативные средства. Основной акцент при демонстрации представители компании делали на то, что препарат абсолютно безопасен, что и позволило получить лицензию на производство и распространение препарата. [2]
В 1957 году препарат был официально выпущен в продажу в Германии под названием Contergan, в апреле 1958 года в Великобритании его выпустила фирма Distillers Company под названием Distaval. Кроме того, талидомид поставлялся на рынок в составе лекарственных средств для самых разных случаев, например, Asmaval — против астмы, Tensival — против повышенного кровяного давления, Valgraine — против мигрени. Всего Талидомид поступил в продажу в 46 странах Европы, Скандинавии, Азии, Африки, Южной Америки, где он выпускался под 37 разными названиями. Никаких дополнительных независимых исследований препарата ни в одной стране не проводилось.
В августе 1958 года от компании Grünenthal поступило письмо, в котором отмечалось, что «талидомид — лучшее лекарство для беременных и кормящих матерей». Этот пункт почти сразу же был отражён в рекламе средства в Великобритании компанией Distiller, несмотря на то, что исследования влияния препарата на плод не проводились ни немецкой компанией Grünenthal, ни английской Distiller. Талидомид стал успешно применяться для устранения неприятных симптомов, связанных с беременностью, таких, как бессонница, беспокойство, утренняя тошнота. [2] [3]
Начиная с 1959 года, компания Grünenthal начала получать письма с сообщениями о периферическом неврите и других побочных эффектах от применения препарата. Появились мнения о том, что препарат следует продавать только по назначению врача. Несмотря на это, талидомид продолжал держать лидирующие позиции по продажам и в некоторых странах отставал по уровню продаж только от аспирина. Политика компании заключалась в отрицании связи препарата Contergan с периферическим невритом, и Grünenthal упорно сопротивлялась попыткам ограничить продажи препарата.
8 сентября 1960 года в США Richardson-Merrell Company представила талидомид на рассмотрение Управления контроля качества продуктов и лекарств США под названием Kevadon. Американские законы того времени для лицензирования лекарственного препарата требовали только безопасности его применения. Эти же законы допускали клиническое пробное применение лекарственного препарата до его лицензирования, что позволило компании Richardson-Merrell распространить более 2 500 000 таблеток 20 тысячам пациентов посредством 1267 терапевтов. Препарат был одобрен большинством врачей, которые сочли его безопасным и полезным, что они отразили в своих отчётах. Однако доктор Фрэнсис О. Келси, назначенная FDA для контроля над лицензированием препарата, оказалась не впечатлена результатами этого теста. Одним из основных факторов, повлиявших на решение Келси, было то, что компания Richardson-Merrell знала о риске развития невритов, но умолчала об этом в рапорте для FDA. Фрэнсис О. Келси, несмотря на серьёзное давление со стороны Richardson-Merrell, не одобрила препарат Kevadon, и он не поступил на рынок США.
К 1961 году талидомид стал самым продаваемым седативным средством в Германии. [2]
Трагедия
В конце 1961 года, почти в одно время, профессор Ленц (нем. W. Lenz ) в Германии и доктор Макбрайд (англ. McBride ) в Австралии выявили связь между возросшим числом врождённых пороков у новорожденных и тем фактом, что матери этих детей принимали талидомид на ранних сроках беременности.
16 ноября 1961 года Ленц сообщил о своих подозрениях в компанию Chemie Grünenthal по телефону. 18 ноября в газете Welt am Sonntag было опубликовано его письмо, в котором он описал более 150 случаев врождённых пороков у новорождённых и связал их с приёмом матерями талидомида на ранних стадиях. 26 ноября под давлением прессы и немецких властей Chemie Grünenthal начала отзыв талидомида с рынка Германии, уведомив Richardson-Merrell, продукция которой успела распространиться на территории Южной Америки. При этом компания Chemie Grünenthal продолжала отрицать связь эпидемии с выпускаемым ей препаратом.
2 декабря Distillers объявила об отзыве препарата с рынков в открытом письме, опубликованном в английских журналах The Lancet и the British Medical Journal.
В декабре 1961 года в журнале The Lancet было опубликовано письмо Уильяма Макбрайда, в котором он также описал свои наблюдения относительно связи талидомида с врождёнными пороками у младенцев. После этого препарат начали убирать с прилавков в остальных странах. Подтверждения словам Ленца и Макбрайда стали поступать из разных стран, ситуация получила широкую огласку в газетах, по радио и на телевидении, однако, несмотря на это, препарат был доступен для покупки в некоторых аптеках и спустя полгода после первых сообщений. В Италии и Японии препарат продавался и спустя 9 месяцев после огласки.
Судебное разбирательство
Германия
Начиная с конца 1961 года, в прокуратуру Ахена начали поступать первые обвинения в адрес Chemie Grünenthal, и только к 1968 году были окончательно подготовлены материалы дела на 972 страницах. 27 мая 1968 года начался судебный процесс, ответчиками в котором являлись семь представителей компании Chemie Grünenthal, которые обвинялись в том, что допустили на рынок опасный медицинский препарат, не прошедший должной проверки и повлёкший за собой телесный ущерб у значительного числа детей. Также компания обвинялась в том, что не только не отреагировала должным образом на поступающие негативные отзывы о препарате, но и прилагала усилия к замалчиванию этой информации.
18 декабря 1970 года состоялось последнее заседание суда по этому делу, на котором было принято решение о закрытии дела в связи с предложенным 10 апреля 1970 года компанией Chemie Grünenthal обязательством выплатить компенсацию в 100 000 000 немецких марок детям, пострадавшим от действия талидомида. Суд постановил, что, учитывая всю систему производства и распространения лекарственных препаратов, подобное могло произойти с любой фармацевтической компанией, и первоочередной задачей является изменение существующей системы, а не сваливание вины за трагедию на нескольких человек.
17 декабря 1971 года Министерство здравоохранения Германии основало фонд Hilfswerk für behinderte Kinder, в задачу которого входила выплата компенсаций пострадавшим от действия талидомида. Выплаты начались в 1972 году и поначалу были достаточно малы — порядка 10 000 немецких марок, однако позже они увеличились, достигнув размера 100 000—180 000 немецких марок. Размер выплаты конкретному ребёнку зависел от степени нанесённого препаратом ущерба. Ежемесячные выплаты на ребёнка составляли 100—450 немецких марок, позже сумма ежемесячного платежа пересчитывалась и увеличивалась несколько раз (в 1976, 1977, 1980 и 1991 году). Всего к началу 1992 года в качестве компенсации из фонда было выплачено порядка 538 000 000 немецких марок, компенсацию получили 2866 человек. Эти выплаты, в отличие от выплат Chemie Grünenthal, касались только жителей Германии.
Великобритания
В период с 1962 по 1966 год 70 родителей и опекунов детей, пострадавших от талидомида, подали исковые заявления против Distillers с обвинениями в халатности и выдвинули требования о возмещении ущерба. Кроме того, был подан ряд исков от людей, утверждавших, что получили периферический неврит, являющийся побочным эффектом от действия талидомида. Компания начала переговоры с целью разрешить вопросы по исковым заявлениям без доведения дел до суда. В 1968 году было урегулировано, в частности, 65 дел из 70, касающихся детей. Родителям или опекунам детей предлагалось отозвать иск о небрежности, в обмен на получение 40 % от суммы, которую они могли получить в случае успешного завершения судебного процесса. Таким образом, в 1968 году было отозвано 58 исков, за которые компания выплатила 1 000 000 фунтов стерлингов. После того, как суд разрешил подачу исков по этому делу, в том числе и по истечении определяемого законодательством трёхлетнего срока, начали поступать новые иски, из которых к 1971 году неурегулированными осталось 389. По всем этим искам компания Distillers пыталась договориться с истцами, не доводя дело до суда. Кроме того, было создано два списка истцов: список X — те, кто мог доказать, что являются жертвой талидомида, и список Y — те, кто не смог привести убедительных доказательств.
В 1971 году Distillers объявила решение об учреждении трастового фонда для помощи детям с врождёнными физическими недостатками, и к сентябрю проект фонда размером 3 250 000 фунтов стерлингов был готов. Проект предусматривал выплату этой суммы в качестве компенсации в течение десяти лет (не считая той компенсации, которая была выплачена по искам в пользу детей категории X отдельно).
24 сентября 1972 года в газете «Санди Таймс» (англ. The Sunday Times ) появилась статья «Наши талидомидные дети — причина национального позора», в которой рассматривались предпринимаемые компанией Distillers шаги по урегулированию ситуации, и указывалось на то, что предлагаемая компенсация не может быть сопоставима с ущербом, нанесенным английским семьям. Кроме того, в статье было указано, что размер компенсации в 3 250 000 фунтов стерлингов, по сравнению с годовым оборотом компании 64,8 миллионов фунтов стерлингов и активами в 421 миллион, ничтожно мал. Статья вызвала широкий резонанс, в СМИ поднялась волна интереса к этой теме, в связи с чем Distillers увеличила предполагаемый размер фонда до 5 000 000 фунтов стерлингов. [3]
10 августа 1973 года был основан фонд Thalidomide Children’s Trust, в задачу которого входила поддержка детей-инвалидов, чьи матери принимали талидомид на ранних сроках беременности. Правительство Великобритании освободило выплаты детям-жертвам талидомидовой трагедии от налогообложения.
Так как значительная часть исков была отозвана в связи с договорённостью о выплате компенсаций, уголовного дела не возбуждалось и ответственности за случившееся никто из представителей Distillers не понёс.
Другие страны
В других странах были организованы аналогичные фонды. Единственная страна, где такого фонда не было — Италия.
В США история с талидомидом также стала поводом для пересмотра и ужесточения требований к лицензированию лекарственных препаратов, в результате чего в закон «О продуктах питания, лекарствах и косметических средствах» (англ. Federal Food, Drug, and Cosmetic Act ) в 1962 году было добавлено требование предъявления доказательств эффективности лицензируемого товара. [9] [10]
Возвращение на рынок
В 1964 году в Иерусалимском госпитале Хадасса Яков Шескин искал препарат, способный помочь смертельно больному пациенту, страдающему от тяжёлых воспалительных процессов, вызванных проказой. Среди больничных запасов он обнаружил талидомид. Доктор знал о том, что препарат запрещён, но, поскольку больной страдал от невыносимой боли, не мог нормально спать несколько недель и был фактически обречён, Шескин решил дать этот препарат больному. После 20 часов сна больной смог впервые сам встать на ноги, а после последующего приёма талидомида его здоровье начало улучшаться. Такой же эффект от приема препарата наблюдался и у шести других пациентов со сходными симптомами. Позже доктор провёл ряд исследований в Венесуэле, результаты которых показали, что из 173 пациентов, принимавших препарат, полностью излечились 92 %. Дальнейшие исследования Всемирной организации здравоохранения на 4552 больных проказой пациентов показали 99 % улучшений состояния здоровья. Таким образом, появились предпосылки для возвращения препарата на рынок.
Негативное воздействие талидомида на организм
Тератогенное воздействие
Талидомид представляет наибольшую опасность на ранних стадиях беременности. Критический период для плода — 34—50 дней после последней менструации у женщины (от 20 до 36 дней после зачатия). Вероятность появления ребёнка с физическими деформациями появляется после приёма всего одной таблетки талидомида в этот промежуток времени.
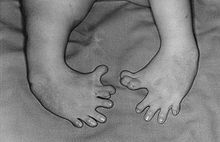
Повреждения плода, вызванные талидомидом, касаются самых разнообразных частей тела. Среди наиболее распространённых внешних проявления выделяются дефекты или отсутствие верхних или нижних конечностей, отсутствие ушных раковин, дефекты глаз и мимической мускулатуры. Кроме того, талидомид влияет на формирование внутренних органов, разрушительным образом действуя на сердце, печень, почки, пищеварительную и мочеполовую системы, а также может приводить в отдельных случаях к рождению детей с отклонениями в умственном развитии, эпилепсией, аутизмом. Дефекты конечностей носят названия фокомелия и амелия (дословный перевод с латинского языка это «тюленья конечность» и «отсутствие конечности» соответственно), которые проявляются в виде некоего подобия тюленьих ласт вместо конечности или практически полного их отсутствия.
Согласно собранным Ленцем данным, около 40 % новорождённых, подвергшихся воздействию препарата на стадии развития плода, умерли до своего первого дня рождения. Некоторые разрушительные воздействия (в частности, касающиеся половой системы ребёнка) могут проявиться только через много лет после рождения и могут быть выявлены только в результате тщательного анализа.
Механизм тератогенного воздействия
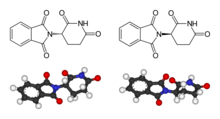
Молекула талидомида может существовать в виде двух оптических изомеров — право- и левовращающего. [18] Один из них обеспечивает терапевтический эффект препарата, в то время как второй является причиной его тератогенного воздействия. Этот изомер вклинивается в клеточную ДНК на участках, богатых G-C связями, и препятствует нормальному процессу репликации ДНК, необходимому для деления клеток и развития зародыша.
Поскольку в организме энантиомеры талидомида способны переходить друг в друга, препарат, состоящий из одного очищенного изомера, не решает проблему тератогенного воздействия.
Другие побочные эффекты
Применение в современной медицине
Отражение в культуре
Трагические последствия употребления талидомида беременными женщинами стали широко известны и были отражены во многих произведениях: