Узи печени эхогенность повышена что это значит у женщин
Саркоидоз:
• Выраженное огрубение эхо-структуры паренхимы.
• Гипоэхогенные мелкоузловые инфильтраты.
Мелкоузловые абсцессы или метастазы:
• Грубая зернистая гипоэхогенная структура.
• Сосуды визуализируются с трудом либо вовсе не определяются (компрессия со стороны сосудов ворот печени, печеночных вен).
Токсический жировой гепатоз, хронический токсический гепатит (индуцированный лекарственными препаратами или алкоголем): при увеличении тяжести заболевания и фиброзной трансформации печени формируются ее структурные изменения:
• В целом повышенная эхогенность. отдельные грубые эхо-сигналы.
• Акустическая тень имеется даже при минимальной глубине поражения.
• Беспорядочные изменения диаметра и невозможность визуализации печеночных вен и мелких венозных ветвей воротной вены.
• Появление дольчатости и зернистости контуров печени.
• Прогрессирующее увеличение диаметра воротной вены.
Тяжелый хронический гепатит со структурными изменениями или циррозом:
На заметку: эхо-структура и характер контуров печени зависят от протяженности изменений, степени фиброзной трансформации и этиологии цирроза. Вид сосудов ворот печени, присутствие асцита и размеры селезенки определяются тяжестью портальной гипертензии и активностью воспалительного процесса.
Диффузные метастазы или метастазы в печень на фоне химиотерапии, системные гематологические заболевания:
• Повышение эхогенности паренхимы.
• Дистальная акустическая тень (как при жировом гепатозе).
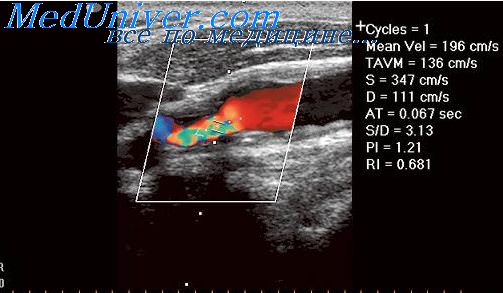
Результаты УЗИ исследования печени.
Роль ультразвукового исследования: ультразвуковое исследование не может заменить гистологического исследования, однако позволяет:
• Получить достоверные, ранее неизвестные данные.
• Сузить диапазон поиска при дифференциальном диагнозе
• При клинически заподозренном заболевании печени классифицировать его как диффузное или локальное, что нередко позволяет поставить более конкретный диагноз.
• Уменьшить или устранить потребность в проведении инвазивных эндоскопических процедур (лапароскопии).
• Поставить диагноз цирроза печени с точностью почти 80%.
Показания для гистологического исследования:
• Диагностика гепатита и оценка активности воспалительного процесса.
• Дифференциальный диагноз цирроза печени и сидероцирроза, алкогольного жирового гепатоза, диабетического или токсического лекарственного жирового гепатоза и болезней накопления.
Последующие исследования зависят от результатов ультразвукового и гистологического исследования:
• Данные, указывающие на жировой гепатоз:
— В случае, если клинические данные не противоречат результатам ультразвукового исследования, дополнительные тесты не требуются. В противном случае показана чрескожная биопсия печени под контролем УЗИ с целью дифференцирования с другими состояниями, характеризующимися аналогичной ульгразвуковой картиной: хроническим гепатитом, болезнью Гоше, токсическим гепатитом, неалкогольным стеатогепатитом (NASH), диффузной злокачественной инфильтрацией.
Лишь в отдельных случаях для подтверждения диагноза требуется слепая биопсия печени (после определения места для пункции при УЗИ) или лапароскопическое исследование.
• Подозрение на метастазы или необъяснимый асцит:
— Лапароскопия и гистологическое исследование.
— Ультразвуковое исследование: используются ЦДЭ, эхосонография с контрастированием и ТГВ.
— Другие методы диагностической визуализации, такие как КТ-ангиография и МРТ.
• Симптомы холестаза (например, склерозирующий холангит): выполняется ЭРХ.
Что значит повышенная эхогенность печени на УЗИ?
В современных подходах к диагностике заболеваний паренхиматозных (плотных) органов брюшной полости важную роль играет УЗИ: ультразвуковое исследование. Термины, которыми оперируют врачи функциональной диагностики, самим больным тоже хочется понимать, чтобы уметь оценить своё состояние.
Что означает повышенная эхогенность печени?
Эхогенность — это способность тканей и органов поглощать либо пропускать сигнал (волну). Аппарат УЗИ — это и приёмник, и передатчик одновременно. Он посылает ультразвуковые волны, а затем ловит то, что отразилось, обратно.
Эхогенность — это плотность органа при УЗИ, соотношение поглощения и отражения волны от органа или ткани. Уровень разницы величин отправленного и вернувшегося сигнала отображает картинку на экране. Степень поглощения волны зависит от плотности, упругости, влажности среды, через которую проходят ультразвуковые волны.
Повышенная эхогенность печени на УЗИ может быть по разным причинам. Обратитесь к врачу для выяснения.
позволяет увидеть много показателей, нужных для оценки состояния печени и окружающих органов:
Если в печёночной ткани обнаружены объёмные образования, то по снимку можно предположить их характер, структуру, состояние клеток. Именно в оценке состояния тканей, то есть структуры печени, и помогает оценка эхогенности. На картинке уровни эхогенности, если сравнивать с видеоизображением, представляют собой разницу по контрасту. Картинка УЗИ рисуется тёмными и светлыми тенями. И разница цветов — это разная эхогенность.
Для любого заключения нужен эталон. При исследовании эталоном средней эхогенности является корковое вещество почки. Плотность (и, соответственно, эхогенность) здоровой печени близка к эталону. Паренхима печени представлена гепатоцитами, именно они дают практически равное соотношение между поглощением и отражением ультразвуковых волн. На картинке УЗИ это выглядит как ровная серая масса. Но в органе есть сосуды, желчные протоки, оболочки долей и долек — и все они отличаются эхогенностью от печёночной паренхимы (ткани) на снимке.
Для примера: кость отражает практически 100% сигнала, который был направлен. В жидкостях, наоборот, сигнал полностью поглощается. Паренхиматозные органы (то есть органы, состоящие из клеточной ткани, в том числе печень) обычно поглощают и отражают 50% на 50% ультразвуковых волн.
Эксперт сайта Похмелье.рф, врач-гастроэнтеролог Даниэла Пургина предупреждает от совершения распространённой ошибки.
Не занимайтесь самолечением. Это неэффективно. И иногда, пытаясь лечиться самостоятельно, пациент может упустить драгоценное время, не достигнув желаемого результата.
Как выглядит на УЗИ патология
При патологических изменениях паренхима печени становится неоднородной. При повышении эхогенности (гиперэхогенности) печени картинка становится более светлой. Увидев в заключении УЗИ фразу об гиперэхогенности печёночной ткани, врач может сделать косвенный вывод о наличии патологии.
Изменение картины на снимке означает изменение ткани органа. Гепатоциты (рабочие клетки печени, составляющие основную массу органа) могут быть заменены всего двумя видами ткани:
И при том, и при другом результате оттенок на снимке УЗИ будет отличаться от нормального состояния, то есть от средней эхогенности печёночной ткани. В любом случае, причиной страдания печёночных клеток всегда являются процессы, которые происходят в организме. Расскажем о них подробнее.
чего бывает повышенная эхогенность печени
Причины, при наличии которых выявляют диффузное (разлитое) повышение эхогенности печёночной ткани:
Совет заболевшему от врача-гастроэнтеролога Даниэлы Пургиной, эксперта сайта Похмелье.рф.
Если вам выставлен диагноз жировой гепатоз (а это одна из самых частых причин диффузных изменений печени) то основное лечение — это снижение массы тела. Это самое простое и самое сложное одновременно. Увы, никакие препараты жир из печени не уберут, поэтому придётся приложить усилия ради собственного здоровья.
Повышение эхогенности может быть как диффузным, разлитым, охватывающим ткань полностью — так и локальным, то есть ограниченным. Причём ограниченные участки (отдельные образования повышенной либо пониженной эхогенности) могут быть с ровными или неровными контурами. Что это значит?
Под гиперэхогенными (то есть более плотными) участками могут маскироваться:
Гипоэхогенными участками (с пониженной плотностью) бывают обычно:
Когда врач видит отдельный участок с изменённым оттенком на снимке, то речь идёт об очаге. При существует масса тонкостей, которые позволяют предположить характер образования, например:
Это разделение условно. Есть характерные для каждого объёмного образования черты, которые смотрит и описывает специалист. Для уточнения диагноза врач может назначить компьютерную томографию или МРТ. Послойные снимки с введением контраста в орган в данном случае хорошо помогают в уточнении характера образования. О том, как выглядят участки аномальной плотности на КТ и МРТ при разных заболеваниях, читайте в статье про гиподенсные образования в печени.
Печень — очень терпеливый орган. Если нет изменений в желчевыводящей системе, то она может долго никак не заявлять о себе клинически. Однако со временем патологические процессы, при которых эхогенность печени повышена, могут привести к циррозу печени. Поэтому нужно обязательно знать, как именно орган говорит о своём недомогании, чтобы не пропустить опасные симптомы.
Какие симптомы должны насторожить
Когда вы ещё чувствуете себя хорошо, но возникают нижеперечисленные признаки — не оставляйте их без внимания. Обратившись к врачу прямо сейчас и вовремя начав лечение, вы сможете избежать массы проблем. Вот наиболее частые ранние симптомы печёночного поражения:
Далее рассмотрим симптомы, которые развиваются, когда печень уже сильно пострадала:
Случай из практики врача-гастроэнтеролога Даниэлы Пургиной, эксперта сайта Похмелье.рф.
В этом случае нет ничего особенного, но он мне запомнился именно реакции самой пациентки. На приём пришла женщина 54 лет, которая не переставая плакала. Как оказалось, накануне она пошла делать УЗИ по поводу тупых болей в правом боку. На УЗИ были выявлены диффузные изменения печени, и врач сказала ей, что это признаки цирроза печени. На самом деле у женщины не было никакого цирроза печени: все показатели крови у неё были в норме, маркёры вирусных гепатитов в норме, признаков цирроза у неё не было. Единственное что было у женщины — это избыточная масса тела и повышение уровня холестерина. И диффузные изменения в печени были ничем иным как жировой болезнью печени. Пациентке было рекомендовано снижение массы тела и препараты, нормализующие уровень холестерина.
Как врач выявляет причину такой картины на УЗИ
При наличии патологии в анализах и повышенной эхогенности печени на УЗИ доктор должен заподозрить и искать процесс, который способствует разрушению ткани органа. Если требуется уточнение диагноза, пациента направят на КТ или МРТ печени с введением контраста.
Также в России становится все более доступной такая диагностическая процедура, как эластометрия печени на аппарате Фиброскан. Этот метод позволяет уточнить плотность печени и дать прогноз заболевания, но имеет свои ограничения. Так, при повышении трансаминаз в 3 раза и более он может дать недостоверные результаты.
В редких случаях требуется проведение такого исследования, как биопсия. Оно инвазивно, то есть требует нарушения целостности печёночной ткани для исследования, поэтому несёт в себе некоторые риски и выполняется строго по показаниям.
Как лечиться
Основа лечения печёночных заболеваний — это прекращение действия повреждающего фактора:
Печень обладает потрясающей способностью к регенерации. Если вовремя определить повреждающий фактор и устранить его, то оставшиеся печёночные клетки возьмут на себя функции погибших. Если при этом начать вести здоровый образ жизни, то орган справится с возникшими трудностями.
Несмотря на широко распространённое мнение о наличии «помощников печени» — гепатопротекторов, которые якобы способствуют восстановлению ткани печени, — убедительных научных подтверждений пока нет. Однако надежды на появление средства, помогающего регенерации печени, не покидают учёных и врачей.
Эксперт сайта Похмелье.рф, врач-гастроэнтеролог Даниэла Пургина развеивает распространённое заблуждение.
Как только пациенту выявляют диффузные изменения в печени, он сразу бежит в аптеку за препаратами для защиты печени, которые так активно рекламируются по телевизору. Но с вами уже знаем, что нам нужно найти причину этих диффузных изменений — и воздействовать на неё уже вполне понятными лекарственными препаратами. Не тратьте деньги на бесполезные гепатопротекторы, обратитесь к специалисту.
Для каждой болезни печени врач подбирает определённое лечение. Главное — вовремя обратиться за медицинской помощью.
Вы можете задать вопрос врачу-гепатологу в комментариях. Спрашивайте, не стесняйтесь!
Статья опубликована: 2019-09-09
Статья обновлялась в последний раз: 17.12.2021
Не нашли то, что искали?
Попробуйте воспользоваться поиском
Бесплатный путеводитель по знаниям
Подпишитесь на рассылку. Мы будем вам рассказывать, как пить и закусывать, чтобы не навредить здоровью. Лучшие советы от экспертов сайта, который читают больше 200 000 человек каждый месяц. Прекращайте портить здоровье и присоединяйтесь!

Думаете, что умеете пить?
Пройдите тест, проверьте себя!
268973 человек прошли опрос, но только 2% ответили на все вопросы верно. Какая оценка будет у вас?
Эхогенность – что это такое и при каких болезнях изменяются эхографические признаки
Для выявления заболеваний внутренних органов в медицине используется ультразвуковая диагностика. Для понимания этого метода нужно знать, что такое показатели эхогенности и другие ультразвуковые признаки нормального или измененного органа.
Понятие об эхогенности
УЗ-диагностика строится на способности ультразвука отражаться от внутренних органов. Датчик улавливает отраженные волны и передает их на компьютер. Врач на экране видит изображение внутренних органов в виде черных, темно-серых и белых пятен.
Процедура абсолютно безопасна для организма человека. Диагностику проводят новорожденным детям и беременным женщинам без ограничений.
Чтобы получить достоверные результаты, обследование нужно проводить правильно. Перед УЗИ брюшной полости рекомендуется придерживаться специальной диеты на протяжении трех дней. При выраженном запоре или метеоризме назначают слабительные и ветрогонные препараты.
Для обследования других органов специальной подготовки не требуется. Для проведения УЗИ на кожу наносят звукопроводящий гель. Это снижает вероятность ошибок.
Для расшифровки результатов обследования существуют эхографические признаки:
Различия между нормальной и измененной структурой органов определяются с помощью эхогенности. Это понятие обозначает степень отражения ультразвука от органов разной плотности.
Основные критерии
Выделяют три основных типа эхоструктуры органов.
Эхогенность
Также существуют анэхогенные структуры. Они поглощают ультразвук полностью. На снимке видно только черное пятно. Иногда встречается смешанная эхогенность — она представлена гипоэхогенными и гиперэхогенными структурами.
Каждое эхогенное образование имеет параметры для определения его характера:
Образования могут быть плотными или иметь полость. В последнем случае их называют кистами. В полости содержится воздух или жидкость. Кисты бывают однокамерными, когда содержат одну полость. Если их несколько, образование называют многокамерным.
Причины патологических образований
Нормой считается эхогенность средняя, или изоэхогенность. Повышенной эхогенностью обладают кости и хрящи. Пониженная эхогенность характерна для фолликулов в яичнике. Остальные случаи являются патологией.
Гиперэхогенные
Эхопозитивное образование, то есть с повышенной эхогенностью, имеет плотность, близкую к костям. Таким критериям отвечают опухоли и разрастания рубцовой ткани.
Повышенная эхогенность возникает в печени при циррозе. В норме она обладает изоэхогенной структурой, но цирроз — это замещение здоровой ткани рубцовой, которая отражает ультразвук сильнее.
Высокая эхогенность характерна для некоторых злокачественных опухолей. Они поражают печень и почки, реже поджелудочную железу.
Гиперэхогенные образования округлой формы в желчном пузыре или почках — камни. Они образуются из-за скопления желчи или солей.
Если эхогенность повышена умеренно в стенке матки, это признак миомы. Доброкачественная опухоль, образованная мышцами, растет медленно.
Гиперэхогенные новообразования отличаются четкими контурами, форма их обычно овальная. Цвет на снимке зависит от плотности. Чем плотнее новообразование, тем светлее оно выглядит.
Гипоэхогенные
Эхонегативное образование имеет плотность ниже, чем здоровый орган. Такой признак наблюдается при воспалениях, появлениях полостей.
Эхогенность снижена при воспалении любого органа. При этом он увеличивается в размере. Такой признак наблюдается при гепатите, панкреатите, простатите.
Низкой эхогенностью обладают полости, содержащие воздух или жидкость. Они называются кистами, у них есть стенка, которая на снимке выглядит светлой. Внутри же обнаруживается темное пятно, потому что воздух или жидкость плохо отражают ультразвук.
Сниженная эхогенность типична для большинства злокачественных и доброкачественных опухолей. На снимке они имеют цвет более темный, чем окружающие ткани.
Низкой эхогенностью характеризуются фиброзные мастопатии. Доброкачественные опухоли молочной железы развиваются на фоне гормональных нарушений.
Равномерно низкая эхогенность внутри полости матки — признак эндометрита. Так называют воспаление слизистой матки.
Новообразования с низкой эхогенностью имеют различные формы, их контуры чаще расплывчатые. Гипоэхогенная эхоструктура бывает диффузной, когда поражается весь орган. При опухолях и кистах гипоэхогенность имеет локальный характер.
Смешанные
Некоторые патологические образования имеют смешанную эхогенность. Так выглядит начальная стадия цирроза печени, когда еще не вся здоровая ткань превратилась в рубцовую.
Гиперэхогенные включения в гипоэхогенной опухоли — это кальцинаты. Признак характерен для рака щитовидной железы или туберкулеза. Подобные изменения наблюдаются в поджелудочной железе при сахарном диабете.
Смешанная эхогенность наблюдается при гломерулонефрите — заболевании почек. Воспалительный процесс развивается только в части органа, а часть его остается здоровой.
Анэхогенные
Новообразования, которые поглощают ультразвук, называются анэхогенными. Такими свойствами обладают кисты, содержащие много жидкости. Чаще всего это паразитарные поражения печени. Они аваскулярные, то есть к ним не подходят кровеносные сосуды.
Тонкостенные анэхогенные образования, до половины заполненные жидкостью — абсцессы. Они появляются в результате гнойного воспаления органа. Абсцессы образуются в любом органе, чаще страдает печень или почка. На снимке абсцесс выглядит как темное пятно со светлой каемкой.
Анэхогенное содержимое появляется в щитовидной железе при диффузном зобе. Заболевание характеризуется разрастанием железистой ткани.
Зная о существующих типах эхогенных образований, что это такое и какими признаками они обладают, можно диагностировать заболевание у человека. Ультразвуковая диагностика обнаруживает даже малейшие изменения, что позволяет своевременно поставить диагноз. Благодаря этому, возможно провести лечение как можно раньше.
Неалкогольная жировая болезнь печени: клиника, диагностика и лечение
В настоящее время неалкогольная жировая болезнь печени (НЖБП) является одним из самых распространенных заболеваний в гепатологии, приводящим к ухудшению качества жизни, инвалидизации и смерти. В первую очередь, это обусловлено высоким риском прогрессирова
В настоящее время неалкогольная жировая болезнь печени (НЖБП) является одним из самых распространенных заболеваний в гепатологии, приводящим к ухудшению качества жизни, инвалидизации и смерти. В первую очередь, это обусловлено высоким риском прогрессирования НЖБП с развитием неалкогольного стеатогепатита (НАСГ), печеночной недостаточности и гепатоцеллюлярной карциномы. Общая распространенность НЖБП в популяции колеблется от 10 до 40%, тогда как частота НАСГ составляет 2–4% [1, 2, 3].
Эпидемиология и патогенез НЖБП
Понятие НЖБП объединяет спектр клинико-морфологических изменений печени, представленных стеатозом, НАСГ, фиброзом и циррозом, развивающихся у пациентов, не употребляющих алкоголь в гепатотоксичных дозах (не более 40 г этанола в сутки для мужчин и не более 20 г — для женщин). НЖБП встречается во всех возрастных группах, но наибольшему риску ее развития подвержены женщины в возрасте 40–60 лет с признаками метаболического синдрома (МС) [4, 5].
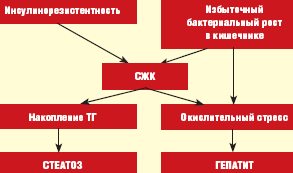
Патогенез НЖБП тесно связан с синдромом инсулинорезистентности (ИР), вследствие которого в печени накапливаются триглицериды (ТГ) и формируется жировой гепатоз (ЖГ) — первый этап или «толчок» заболевания. В последующем происходит высвобождение из жировой ткани и синтез de novo в гепатоцитах свободных жирных кислот (СЖК), способствующих возникновению окислительного стресса, являющегося вторым «толчком» заболевания и приводящего к развитию воспалительно-деструктивных изменений в печени в виде стеатогепатита [6].
Максимальный риск развития НЖБП отмечен в группе лиц с МС — это пациенты с сахарным диабетом (СД) 2 типа, ожирением, гипертриглицеридемией. Частота НЖБП у больных СД 2 типа и ожирением по данным различных исследований варьирует от 70 до 100%. При этом СД 2 типа или нарушение толерантности к глюкозе (НТГ) отмечаются у 10–75%, ожирение — у 30–100%, гипертриглицеридемия — у 20–92% пациентов с НЖБП [1, 4, 7, 8]. В то же время признаки НЖБП обнаруживаются у 10–15% людей без клинических проявлений МС, что может быть обусловлено другими патогенетическими механизмами формирования НЖБП, например, синдромом избыточной пролиферации бактерий в кишечнике или дисбиозом, как это принято формулировать в отечественной литературе [5, 10].
Основные механизмы развития НЖБП при кишечном дисбиозе связаны с нарушением синтеза апо-липопротеидов классов А и С, являющихся транспортной формой для ТГ в процессе образования липопротеидов очень низкой плотности (ЛПОНП), а также кишечным эндотоксикозом, что позволяет рассматривать это состояние в качестве дополнительного источника окислительного стресса (рис.) [11, 12].
Взаимосвязь патогенеза НЖБП с ИР позволяет считать это заболевание одним из независимых компонентов МС, клиническая значимость которого заключается в значительном прогрессировании атеросклеротического поражения сосудов.
В ряде работ показано, что НЖБП повышает риск возникновения сердечно-сосудистых заболеваний (ССЗ) независимо от других предикторов и проявлений МС [13]. Это подтверждается несколькими фактами, к которым относится связь НЖБП с концентрацией адипонектина в плазме. Известно, что адипонектин обладает антиатерогенным действием и по данным многих проспективных исследований снижение его уровня является ранним предиктором ССЗ и МС. У пациентов с НЖБП была отмечена более низкая концентрация адипонектина в плазме, чем у здоровых лиц [13].
Кроме этого, у указанной категории больных по сравнению с контрольной группой отмечается значительное увеличение толщины интимы (ТИ) сонной артерии, которое также признано достоверным субклиническим признаком атеросклероза. Доказано, что величина ТИ менее 0,86 мм связана с низким риском ССЗ, а более 1,1 — с высоким. У пациентов с НЖБП ее значение составляет в среднем 1,14 мм [14–18].
Другим субклиническим признаком атеросклероза, обнаруженным у больных НЖБП, служит выявление эндотелиальной дисфункции, что подтверждается снижением эндотелийзависимой вазодилатации плечевой артерии у пациентов с НЖБП. При этом уменьшение этого показателя коррелирует со степенью морфологических изменений в печени независимо от пола, возраста, ИР и других компонентов МС [19, 20].
Таким образом, патогенез НЖБП неразрывно связан с МС, а сам факт развития указанной патологии изменяет прогноз для этих пациентов, как в виде прогрессирования печеночной недостаточности, так и в виде значительного увеличения частоты осложнений ССЗ.
Клиника и диагностика
В целом для НЖБП характерно бессимптомное течение, поэтому наиболее часто в практике врач сталкивается со случайно обнаруженным при биохимическом исследовании синдромом цитолиза. При этом пациент с НЖБП, как правило, либо не предъявляет жалоб, либо они являются неспецифичными в виде астеновегетативного синдрома (слабость, утомляемость) и дискомфорта в правом подреберье. Наличие кожного зуда, диспепсического синдрома, наряду с развитием желтухи и портальной гипертензии, свидетельствует о далеко зашедшей стадии НЖБП [2, 3].
При объективном осмотре больных НЖБП обращают на себя внимание гепатомегалия, которая встречается у 50–75%, и спленомегалия, выявляемая у 25% пациентов [4].
При лабораторном исследовании для НЖБП характерны следующие изменения:
Основным дифференциальным отличием ЖГ от НАСГ, доступным в клинической практике, может быть выраженность биохимического синдрома цитолиза.
Следует отметить, однако, что отсутствие изменений лабораторных показателей, характеризующих функциональное состояние печени (АЛТ, АСТ, ЩФ, ГГТП), не исключает наличия воспалительно-деструктивного процесса и фиброза [10].
Как указывалось выше, диагностический поиск проводится в связи с выявлением у больного синдрома цитолиза, при этом наличие у него СД 2 типа, абдоминального ожирения, артериальной гипертензии и нарушения липидного обмена свидетельствует о высокой вероятности НЖБП. Постановка этого диагноза достаточно сложна ввиду необходимости исключения всех других причин, вызывающих цитолиз, макровезикулярный стеатоз и воспалительно-деструктивные изменения в печени. Следует исключить вторичный характер поражения печени (табл. 1) [2].
Для уточнения диагноза могут использоваться инструментальные методы (ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ)), которые позволяют верифицировать гепатомегалию, косвенно оценить степень стеатоза печени и зарегистрировать формирование портальной гипертензии.
УЗИ является недорогим и, по мнению некоторых авторов, достаточно информативным инструментальным методом диагностики стеатоза печени. Выделяют 4 основных ультразвуковых признака стеатоза печени:
К преимуществам УЗИ относится также возможность регистрировать динамику признаков стеатоза, в том числе на фоне лечения [20].
При проведении КТ печени основными признаками, свидетельствующими о наличии стеатоза, являются:
В целом КТ менее информативна, чем УЗИ при диффузных поражениях печени, однако она является методом выбора при очаговых заболеваниях [23].
Преимуществами современной высокопольной МРТ по сравнению с другими методами визуализации являются: высокая тканевая контрастность изображения за счет выгодного соотношения сигнал–шум, возможность получения целостного изображения органа в любой проекции, а также большие ресурсы программного обеспечения, используемые для дифференциальной диагностики.
Однако все визуализационные методы диагностики, несмотря на достаточно высокую информативность, не позволяют оценить наличие признаков стеатогепатита, степень его активности и стадию фиброзных изменений в печени [24, 25]. Поэтому с целью верификации диагноза необходимо проведение пункционной биопсии.
Значение пункционной биопсии печени в клинической практике неоднозначно. С одной стороны, только биопсия печени позволяет провести дифференциальный диагноз между стеатозом и стеатогепатитом, оценить стадию фиброза и на основании гистологических данных прогнозировать дальнейшее течение заболевания, а также исключить другие причины поражения печени. Однако отсутствие информированности врачей о целесообразности, а пациентов о безопасности метода сдерживают активное внедрение пункционной биопсии в практику.
Помимо этого, до сих пор активно обсуждаются морфологические критерии НЖБП. До настоящего времени в практике широко использовалась классификация, предложенная Brunt Е. (1999, 2001), которая подразделяет НЖБП в зависимости от степеней стеатоза, активности воспаления и стадии фиброза печени:
I. Степени крупнокапельного стеатоза:
0 степень: нет стеатоза;
1 степень: стеатоз до 33% гепатоцитов;
2 степень: стеатоз 33–66% гепатоцитов;
3 степень: стеатоз более 66%.
II. Степени НАСГ:
1 степень (мягкий НАСГ) — стеатоз 1–2 степени, минимальная баллонная дистрофия в 3 зоне ацинуса, лобулярное воспаление — рассеянная или минимальная лимфоплазмоцитарная инфильтрация, портальное воспаление отсутствует или минимальное;
2 степень (умеренный НАСГ) — стеатоз любой степени (крупно- и мелкокапельный), умеренная баллонная дистрофия в 3 зоне ацинуса, мягкое или умеренное портальное и лобулярное воспаление в 3 зоне ацинуса, может быть перисинусоидальный фиброз;
3 степень НАСГ (тяжелый НАСГ) — панацинарный стеатоз (смешанный), выраженная баллонная дистрофия, выраженное лобулярное воспаление, мягкое или умеренное портальное воспаление.
III. Стадии фиброза:
1 стадия — перисинусоидальный/перицеллюлярный фиброз в 3 зоне ацинуса, очаговый или распространенный;
2 стадия — перисинусоидальный/перицеллюлярный фиброз в 3 зоне ацинуса, очаговый или распространенный перипортальный фиброз;
3 стадия — очаговый или распространенный мостовидный фиброз;
4 стадия — цирроз печени [26].
Однако, по мнению ряда авторов, эта классификация не отражает целый спектр морфологических признаков, выявляемых у больных НЖБП при гистологическом исследовании. Недавно на основе существующей классификации была разработана и предложена Шкала активности НЖБП (NAFLD activity score — NAS), представляющая комплексную оценку морфологических изменений в баллах и объединяющая такие критерии, как стеатоз (0–3), лобулярное воспаление (0–2) и баллонную дистрофию гепатоцитов (0–2). Сумма баллов менее 3 позволяет исключить НАСГ, а более 5 свидетельствует о наличии у пациента гепатита. Данная шкала используется преимущественно для оценки эффективности лечения НЖБП, поскольку позволяет определить достоверность динамики морфологических изменений на фоне терапии за относительно короткий период времени [27].
В тех случаях, когда выполнение пункционной биопсии невозможно, диагноз НЖБП устанавливается в соответствии с алгоритмом, позволяющим пошагово исключить другие заболевания печени (табл. 2).
В связи с тем, что все пациенты с МС относятся к группе риска развития НЖБП, то больные с ожирением, СД 2 типа или НТГ, нарушением липидного обмена нуждаются в дополнительном обследовании, включающем клинические, лабораторные и инструментальные методы диагностики НЖБП и, в особенности, НАСГ. Однако до настоящего времени НЖБП и ее проявления не входят ни в критерии постановки диагноза МС, ни в алгоритм обследования больных с подозрением на его наличие (табл. 3).
Скрининг больных на стадии доклинических проявлений МС включает:
С учетом частоты, роли и значения НЖБП, в алгоритм обследования больных с МС должны входить клинико-лабораторные и инструментальные методы, позволяющие оценить морфофункциональное состояние печени:
Обязательными показаниями для биопсии являются:
Оценивать течение НЖБП возможно на основании данных гистологического исследования печени. Однако когда выполнение биопсии недоступно, существуют предикторы, позволяющие предположить высокий риск прогрессирования НЖБП с развитием гепатита и фиброза, которые были установлены при проведении статистической обработки результатов большого количества наблюдений [28–30].
Выявление более 2 критериев свидетельствует о высоком риске фиброза печени.
Для формулировки полноценного клинического диагноза необходимо учитывать данные клинико-лабораторного и инструментального обследования, выявление факторов неблагоприятного течения заболевания и других компонентов МС. Поскольку диагноз «неалкогольная жировая болезнь печени» в МКБ-10 (ВОЗ, 1998) пока отсутствует, его формулировка практическими врачами может производиться с учетом правил диагностики алкогольной болезни печени и вирусных гепатитов. В диагнозе на первом месте лучше указывать ту нозологическую единицу, на фоне которой развилась НЖБП, далее идет форма заболевания (гепатоз или НАСГ), степень стеатоза (по данным УЗИ), активность гепатита и стадия фиброзных изменений в печени в случае проведения гепатобиопсии. Если морфологическое исследование не выполнялось, допустимым, как и при других заболеваниях печени, является заключение: неустановленный фиброз. Примеры диагностических заключений:
Лечение НЖБП
В связи с высокой вероятностью неблагоприятного течения НЖБП, особенно в сочетании с другими проявлениями МС, все больные независимо от тяжести заболевания нуждаются в динамическом наблюдении и лечении. Однако до сих пор не разработаны стандартизированные терапевтические подходы к ведению пациентов с НЖБП.
Используемые направления терапии больных НЖБП основываются на механизмах развития заболевания, к которым в первую очередь относятся синдром ИР и окислительный стресс, поэтому наиболее важными задачами у данной категории пациентов являются:
Диета. С учетом современных представлений об этиологии, патогенезе и факторах прогрессирования НЖБП больным рекомендуются следующие диетические принципы:
Для пациентов с избыточной массой тела и ожирением — снижение общей энергетической ценности пищевого рациона. Суточная калорийность подбирается индивидуально в зависимости от массы тела, возраста, пола, уровня физической активности с использованием специальных формул. Сначала рассчитывают количество калорий, необходимых для основного обмена:
18–30 лет: (0,06 × вес в кг + 2,037) × 240
31–60 лет: (0,034 × вес в кг + 3,54) × 240
старше 60 лет: (0,04 × вес в кг + 2,76) × 240
18–30 лет: (0,06 × вес в кг + 2,9) × 240
31–60 лет: (0,05 × вес в кг + 3,65) × 240
старше 60 лет: (0,05 × вес в кг + 2,46) × 240.
Полученное значение умножают на коэффициент физической активности (1,1 — низкая активность, 1,3 — умеренная, 1,5 — тяжелая физическая работа или активное занятие спортом) и получают калорийность суточного рациона. Для снижения массы тела из рассчитанной величины суточных энергозатрат вычитают 500–700 ккал. Однако минимальное потребление калорий в сутки должно быть не менее 1200 ккал для женщин и не менее 1500 для мужчин. Доказано, что снижение массы тела на 5–10% сопровождается уменьшением гепатоспленомегалии, активности АЛТ, АСТ и коррелирует с регрессированием стеатоза печени [4]. Следует учесть, что быстрая потеря веса может привести к развитию «острого» НАСГ с формированием портального фиброза, центральных некрозов на фоне значительного повышения воспалительной активности вследствие увеличения поступления СЖК в печень на фоне периферического липолиза [5, 31]. Для больных ожирением и НЖБП безопасным и эффективным является снижение массы тела на 500 г в неделю для детей и на 1600 г в неделю для взрослых [31].
Кроме этого, всем пациентам с НЖБП рекомендуется:
Физическая нагрузка. Обязательным условием лечения больных НЖБП является физическая нагрузка. Она оказывает положительный эффект на снижение массы тела и чувствительность к инсулину, при этом увеличивается поступление СЖК в мышечную ткань, где происходит их окисление, тем самым уменьшается ИР [4]. Степень снижения ИР, как правило, коррелирует с интенсивностью физических упражнений, которые рекомендуется проводить не менее 3–4 раз в неделю, продолжительностью 30–40 минут.
Повышение чувствительности клеточных рецепторов к инсулину. К базисным медикаментозным средствам лечения синдрома ИР у больных НЖБП могут быть отнесены инсулиновые сенситайзеры — бигуаниды (метформин) и тиазолидиндионы (пиоглитазон, росиглитазон) — препараты, повышающие чувствительность клеточных рецепторов к инсулину. Опыт применения данных лекарственных средств свидетельствует о положительном влиянии на клинико-морфологические проявления НЖБП в виде уменьшения активности показателей цитолитического синдрома, степени стеатоза и воспаления. Но в целом вопрос применения этих препаратов у больных НЖБП требует проведения дальнейших исследований, что обусловлено отсутствием адекватных методов контроля эффективности лечения (гепатобиопсия) в выполненных работах [32].
Гиполипидемические средства. Учитывая патогенез заболевания, у пациентов с НЖБП эффективным может оказаться применение гиполипидемических средств из группы фибратов. Однако результаты исследования с назначением клофибрата больным НЖБП показали его неэффективность [33]. Не следует забывать и о возможности развития фибрат-индуцированных гепатитов. В отношении статинов также существует ряд противопоказаний, связанных с их гепатотоксическим действием. В целом данные выполненных работ противоречивы и указывают на необходимость дальнейшего изучения возможности использования этих препаратов у пациентов с НЖБП.
Пентоксифиллин. Снижение концентрации тумор-некротизирующего фактора-a (TNFa) имеет значение для прогрессирования НЖБП. Обладая высокой биологической активностью, TNFa усиливает ИР и приводит к развитию окислительного стресса. Уменьшение его уровня в крови связано с регрессом клинических и морфологических проявлений НЖБП. Подобный эффект был обнаружен у пентоксифиллина. Назначение этого препарата у пациентов с НАСГ в суточной дозе 1200 мг на протяжении 12 месяцев было связано со снижением показателей цитолитического синдрома и достоверным улучшением гистологических показателей у 67% больных [34].
Антагонисты рецепторов ангиотензина II. Формирование данного подхода обусловлено ролью ангиотензина в прогрессировании НАСГ. Установлено, что он, способствуя пролиферации миофибробластов, клеточной миграции, синтезу коллагена и провоспалительных цитокинов, активирует процессы фиброгенеза в печени. Поэтому в настоящее время исследуется возможность применения блокаторов ангиотензиновых рецепторов у пациентов с НЖБП. Так, прием лозартана у пациентов с НАСГ и артериальной гипертензией в суточной дозе 50 мг в течение 38 недель приводил к достоверному снижению АЛТ и ГГТП, что сочеталось с уменьшением степени стеатоза и воспалительной активности [35].
Антиоксиданты. Применение антиоксидантов у больных НЖБП оправдано наличием окислительного стресса, что подтверждается повышением в плазме у больных НАСГ маркера окислительного стресса — тиоредоксина и снижением концентрации антиоксидантных факторов. В настоящее время активно изучается возможность использования витамина Е, эффективность которого была продемонстрирована в ряде исследований [36]. Также имеется ряд зарубежных и отечественных работ, посвященных оценке влияния УДК на морфофункциональное состояние печени. Механизмы действия этой гидрофильной кислоты связаны с тем, что, нормализуя гепатоэнтеральную циркуляцию желчных кислот и целого ряда биологически активных веществ, вытесняя токсичные желчные кислоты, она способствует ликвидации избытка холестерина в гепатоцитах, путем уменьшения его синтеза и всасывания из кишечника. УДК также обладает цитопротективным и антиапоптотическим действием, препятствуя развитию окислительного стресса, что позволяет применять ее на обоих этапах НЖБП [33].
В отношении АЛК установлено, что она обладает плейотропным действием на весь организм, оказывая положительное влияние на энергетический, липидный (тормозит синтез холестерина, подавляя высвобождение СЖК из жировой ткани, что предупреждает развитие стеатоза гепатоцитов) и углеводный (снижает ИР, усиливает захват и утилизацию глюкозы клеткой, повышает чувствительность клеточных рецепторов к инсулину) виды обменов.
Кроме этого, АЛК, имея низкий оксислительно-восстановительный потенциал, обладает мощным антиоксидантным эффектом, действуя непосредственно на печень, способствует повышению детоксицирующих субстанций в гепатоцитах (восстанавливает глутатион) и улучшению морфологических изменений [36].
Восстановление микробиоценоза кишечника. К сожалению, большинство работ, подтверждающих патогенетическую роль дисбиоза кишечника в формировании НЖБП и эффективность антибактериальных препаратов в лечении указанной нозологии, относится к 80–90-м годам прошлого столетия.
Поэтому вопрос проведения санации кишечника антибактериальными препаратами остается открытым. Антибиотики рекомендуются только при наличии верифицированной чувствительной условно-патогенной флоры в кишечнике или формировании заболевания после оперативного лечения на брюшной полости, например «синдрома приводящей петли». Преимуществом выбора при этом принадлежит препаратам, обладающим способностью хорошо накапливаться в желчи с эффектом вторичного прохождения через желудочно-кишечный тракт, к которым относятся фторхинолоны первого поколения (ципрофлоксацин). Также могут использоваться кишечные антисептики, типа метронидазола или нифуроксазид, и невсасывающиеся в кишечнике препараты, например рифаксимин.
Во всех остальных случаях, когда нет показаний для применения антибиотиков, кишечную санацию у больных НЖБП следует проводить пребиотиками, а препаратом выбора в данном случае является Эубикор. Его преимуществом является сбалансированный состав, куда входят пищевые волокна и винные дрожжи (S. vini). Кроме мощного пребиотического эффекта, Эубикор обладает хорошими сорбционными свойствами, что позволяет не только восстанавливать нормальную микрофлору, но и проводить дезинтоксикацию. По результатам исследований, прием Эубикора у данной категории пациентов способствовал дополнительному уменьшению дислипопротеидемии и повышению чувствительности к инсулину [37, 38].
Лечение неалкогольного ЖГ
В целом требования, предъявляемые к лекарственным средствам, используемым в лечении НЖБП, достаточно высоки. В первую очередь, они должны быть максимально безопасны с точки зрения гепатотоксичности, также желательно их позитивное действие на улучшение клинико-лабораторных и морфологических изменений в печени.
Собственный опыт лечения больных НЖБП на стадии гепатоза состоит в использовании комбинации АЛК с Эубикором. АЛК (препарат «Берлитион», производитель — Берлин-Хеми, Германия) назначалась по 600 ЕД внутривенно в течение 14 дней, с переходом на пероральный прием в той же суточной дозе, однократно в течение 6 месяцев. Эубикор назначался по 2 пакетика 3 раза в день во время еды. Результаты работы показали положительное влияние Берлитион и Эубикора не только на показатели липидного и углеводного обменов, но и на степень жировой дистрофии в печени по результатам ультразвукового и морфологического исследований. Положительная динамика указанных изменений имеет значение как для формирования системной ИР, являющейся основной причиной развития МС, так и для течения собственно НЖБП и развития НАСГ. Поэтому данные препараты, наряду с немедикаментозной терапией, могут рассматриваться как средства базисной терапии первой стадии НЖБП — ЖГ.
Лечение НАСГ
При развитии у пациентов НАСГ терапия заболевания усиливалась дополнительной комбинацией метформина (препарат «Сиофор», производитель — Берлин-Хеми, Германия) в дозе 1500 мг в сутки с УДК (препарат «Урсосан» фирмы PRO.MED.CS Praha a.s.) в дозе 15 мг на 1 кг массы тела, с однократным приемом через час после ужина. Длительность лечения подбиралась индивидуально, как правило, она составляла не менее 6 месяцев, иногда достигая 12 и более месяцев. Продолжительность курса зависела от выраженности клинических проявлений, комплайнса и динамики лабораторно-инструментальных показателей на фоне лечения. Назначение этих препаратов сопровождалось уменьшением не только клинико-лабораторных проявлений заболевания, но и достоверно способствовало улучшению гистологической картины печени. При этом комбинированная терапия у данной категории пациентов являлась методом выбора, поскольку именно в группе, получавшей одновременно Сиофор, Берлитион и Урсосан, динамика показателей синдромов цитолиза, холестаза, а также жирового и углеводного обменов была более значимой. На фоне лечения у больных НАСГ также отмечалось обратное развитие жировой дистрофии, достоверно уменьшилась выраженность воспалительных изменений и отсутствовало прогрессирование стадии фиброза в печени. Таким образом, комбинированная терапия воздействует на основные этиопатогенетические механизмы формирования метаболических нарушений, приводит к улучшению показателей липидного и углеводного обменов в виде нормализации уровней ЛПВП, ТГ и индекса ИР у пациентов с НАСГ.
Предложенная схема лечения НЖБП не является стандартизированной, но она патогенетически обоснована, а ее рабочий вариант может рассматриваться как применение:
На практике рациональный выбор того или иного препарата может определяться сочетанием НЖБП с другими компонентами МС.
Рекомендуемые алгоритмы выбора терапии пациентов с НЖБП и ожирением:
ИМТ менее 40 кг/м 2 :