герпес влияние на мозг
Герпетический энцефалит
Сезонные колебания герпетическому энцефалиту не свойственны. Два пика заболеваемости приходятся на 5-30 лет и возраст старше 50 лет. Более чем в 95% случаев возбудителем герпетического энцефалита служит вирус простого герпеса типа 1.
Что провоцирует / Причины Герпетического энцефалита :
Возбудитель относится к семейству герпеса (Herpes viridae).E это семейство входят также вирусы ветряной оспы, опоясывающего лишая, цитомегаловирусы и возбудитель инфекционного мононуклеоза. Содержит ДНК, размеры вириона 100-160 нм. Вирусный геном упакован в капсид правильной формы, состоящий из 162 капсомеров. Вирус покрыт липидсодержащей оболочкой. Размножается внутриклеточно, образуя внутриядерные включения. Проникновение вируса в некоторые клетки (например, в нейроны) не сопровождается репликацией вируса и гибелью клетки. Наоборот, клетка оказывает угнетающее влияние и вирус переходит в состояние латенции. Через некоторое время может происходить реактивация, что обусловливает переход латентных форм инфекции в манифестные. По антигенной структуре вирусы простого герпеса подразделяются на два типа. Геномы вирусов 1 и 2-го типа на 50% гомологичны. Вирус 1-го типа обусловливает преимущественно поражение респираторных органов. С вирусом простого герпеса 2-го типа связано возникновение генитального герпеса и генерализованная инфекция новорожденных.
Эпидемиология. Герпетический энцефалит составляет 11,5% среди острых энцефалитов. Заболевают чаще дети младшего возраста. Заболеваемость спорадическая, некоторые исследователи указывают на увеличение ее весной. Инфекция может передаваться капельным и контактным путем.
Патогенез (что происходит?) во время Герпетического энцефалита :
Патогенез заболевания герпетическим энцефалитом неоднороден. У детей и молодых людей в форме энцефалита может протекать первичный герпес. При этом вирус герпетического энцефалита, по- видимому, попадает в ЦНС со слизистой носа, транспортируясь по аксонам обонятельных нейронов в обонятельную луковицу. Однако большинство взрослых больных, страдающих герпетическим энцефалитом, либо имеют герпес в анамнезе, либо серопозитивны в отношении вируса простого герпеса типа 1. Приблизительно у 25% больных герпетическим энцефалитом в слизистой ротоглотки и ткани головного мозга обнаруживают разные штаммы вируса. В этих случаях энцефалит обусловлен повторным заражением иным штаммом вируса простого герпеса типа 1 с проникновением возбудителя в ЦНС.
Для объяснения причин энцефалита в тех случаях, когда в слизистой ротоглотки и ткани головного мозга обнаруживают один и тот же штамм вируса, предложено две гипотезы.
Согласно первой, реактивация вируса герпетического энцефалита в тройничном или вегетативных ганглиях сопровождается его распространением в ЦНС по нервам, иннервирующим среднюю черепную ямку. Согласно второй, вирус длительное время покоится в латентном состоянии непосредственно в ЦНС, где и реактивируется. Во всяком случае, с помощью олигонуклеотидных зондов ДНК вируса простого герпеса была обнаружена в ткани головного мозга взрослых людей, умерших не от герпеса.
Симптомы Герпетического энцефалита :
Кроме типичного некротического энцефалита выделяют псевдотуморозную и стволовую форму. Описаны также энцефаломиелиты и генерализованная герпетическая инфекция с преимущественным поражением ЦНС.
Диагностика Герпетического энцефалита :
Лечение Герпетического энцефалита :
Профилактика Герпетического энцефалита :
К каким докторам следует обращаться если у Вас Герпетический энцефалит :
Ученые связали вирус герпеса с развитием нейродегенеративных болезней
Герпесвирусы — обширное семейство, насчитывающее почти 90 видов вирусов, поражающих млекопитающих, птиц, рыб, рептилий и земноводных. Человек уязвим лишь для восьми из них. При этом после заражения, например, вирусами простого герпеса I и II типа, избавиться от инфекции в организме уже невозможно. Вирус сохраняется в латентной форме, напоминая о себе в среднем несколько раз в год высыпаниями, преимущественно в районе губ или половых органов. Вирусом простого герпеса I типа, по разным оценкам, заражено до 90% населения планеты.
Ранее вирус простого герпеса I типа уже связывали с болезнью Альцгеймера — у людей с HSV-1 заболевание возникает чаще, а вирусная ДНК определяется в амилоидных бляшках.
Однако достаточно подробных исследований, посвященных связи вирусов герпеса с нейродегенеративными заболеваниями и поиску возможных механизмов, повышающих риски, не проводилось.
Заняться поиском факторов, с помощью которых вирусы делают мозг более предрасположенным к дегенерации нервных клеток, решили специалисты Иллинойсского университета в Чикаго. Свои выводы они изложили в статье в журнале Nature Communications.
Исследователи хотели выяснить, почему HSV-1 может стать смертельным для людей с ослабленным иммунитетом, но не наносит серьезного вреда здоровым людям. Герпесвирусы инфицируют центральную нервную систему и могут приводить к энцефалиту и прочим поражениям мозга. Однако в большинстве случаев организм подавляет первичную инфекцию прежде, чем она успевает нанести ЦНС серьезный ущерб.
В механизме защиты может играть роль белок оптиневрин, предположили ученые. Оптиневрин — рецептор, способный склонить белки вируса к аутофагии.
«Оптиневрин останавливает рост вируса, это происходит путем аутофагии — захвата частиц вируса внутри крошечных везикул, называемых аутофагосомами. Происходящая аутофагия очень избирательна. Это может быть важно для понимания того, как организм борется и с другими вирусами», — говорит доктор Дипак Шукла, один из авторов работы.
Чтобы проверить эту версию, исследователи использовали линию генетически модифицированных мышей, у которых не синтезировался оптиневрин. Их и обычных мышей ученые заразили HSV-1. У мышей без оптиневрина вирус беспрепятственно размножался в мозге, уничтожая нейроны и, в конечном итоге, приводя к смерти грызунов.
Ген, регулирующий выработку оптиневрина, может мутировать и естественным образом, отмечают авторы работы.
«Если у вас есть и мутировавший оптиневрин, и герпес, это катастрофа с точки зрения нейродегенерации», — говорит Шукла.
«Исследование также показывает, что при дефиците оптиневрина нарушается иммунный ответ, — добавляет Чандрашекхар Патил, соавтор исследования. — Оптиневрин необходим для подачи сигнала о притоке соответствующих иммунных клеток в место инфекции. Когда у вас его нет, возникают проблемы».
Поскольку вирус герпеса остается в нервных клетках, исследователи полагают, что он может быть фактором, повышающим риск развития нейродегенеративных заболеваний. Чтобы постоянно бороться с вирусом, иммунной системе приходится запускать воспалительные процессы, и это сказывается на состоянии нейронов не лучшим образом.
Мыши без оптиневрина, зараженные HSV-1, через 30 дней теряли способность распознавать объекты. По словам Шуклы, это может свидетельствовать, что наличие вируса вкупе с мутацией способно ускорить повреждение нейронов привести к когнитивным нарушениям.
По мнению авторов работы, результаты могут касаться всех видов герпесвирусов, поражающих человека. Хотя исследование проводилось на мышах, у ученых нет сомнений, что и в человеческом мозге отсутствие оптиневрина приведет к тем же последствиям — ускоренной дегенерации нервных клеток. Исследователи планируют дополнительно изучить возникающие естественным образом мутации гена, регулирующего выработку оптиневрина — так, известно, что они наблюдаются у людей с глаукомой. Теперь же предстоит выяснить, как они влияют на здоровье при наличии в организме HSV-1 и других вирусов герпеса.
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
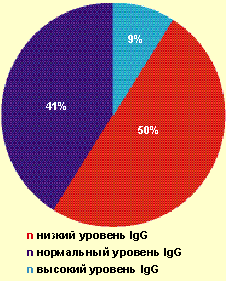 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
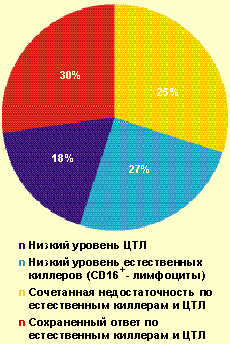 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва
Вирус простого герпеса нарушил процесс развития нервной ткани
South Park / Comedy Central, 1997-2020
Вирус простого герпеса первого типа нарушает процессы дифференцировки стволовых нервных клеток и формирования коры головного мозга. Такие результаты удалось получить с помощью, в том числе, трехмерной органоидной модели головного мозга человека. Кроме того, ученым удалось показать, что вирус способствует аномальной активации микроглии, которая сопровождается выработкой воспалительных медиаторов. Она также может нарушать процесс развития нервной ткани. Исследование опубликовано в журнале PLoS Pathogens.
Вирус простого герпеса (ВПГ) — один из наиболее распространенных патогенов человека во всем мире. ВПГ первого типа (ВПГ-1) в основном передается при оральном контакте и вызывает герпес на губах и во рту, в то время как ВПГ второго типа передается половым путем и вызывает генитальный герпес. Оба типа вируса способны вызывать пожизненную инфекцию и иногда способны вызывать и тяжелые заболевания, например, энцефалит. Ряд исследований показали, что внутриутробные инфекции ВПГ-1 связаны с риском нарушений развития центральной нервной системы плода, что приводит к долгосрочным неврологическим последствиям, включая когнитивную дисфункцию, неспособность к обучению и деменцию у взрослых. Однако патогенетические звенья этого процесса остаются неясными.
Современное понимание того, как инфекция ВПГ-1 влияет на мозг плода, в значительной степени известно по животным моделям. Однако человеческий мозг содержит намного больше нервных и глиальных клеток, которые формируют сложные морфологические и функциональные связи. Из-за этой сложности полноценно перенести результаты с животных моделей на человека нельзя. Поэтому группа ученых из Уханьского университета под руководством Хаовэнь Цяо (Haowen Qiao) изучила патогенное действие вируса простого герпеса первого типа на нервных клетках разной степени дифференцировки и трехмерных органоидах головного мозга, которые были максимально приближены морфологически и функционально к развивающемуся головному мозгу плода.
Чтобы понять, какие клетки поражает ВПГ-1, ученые попытались заразить вирусом плюрипотентные стволовые клетки, нервные стволовые клетки и зрелые нейроны разным количеством вирусных частиц. Через восемь дней при количественном определении уровня инфицирования клеток (с помощью иммунофлюоресцентного окрашивания антител против антигенов ВПГ-1 на оболочке клетки) выяснилось, что наиболее восприимчивыми к ВПГ-1 оказались нервные стволовые клетки (p
Многоликий и коварный герпес
– Давайте разберемся с этим «семейством».

– А может, предположим, человек не знать, что страдает герпесом, обусловленным вирусами этих двух типов?
– Может. Например, мы часто видим в уголках губ так называемые заеды – трещинки. Исследования показывают, что у 20% таких пациентов есть вирус простого герпеса 1-го типа. То же самое и с генитальным герпесом: не обязательно будет сыпь и зуд, вполне возможно образуется просто трещинка.
– Я слышала, что вирус ветрянки – тоже герпес.
– Это 3-й тип – герпес Зостера, или ветрянки, который может поражать и после 40 лет. Считается, что у 40% детей, которые перенесли ветрянку, вирус ветряной оспы остается существовать дальше в ганглиях нервной системы (нервном узле – скоплении нервных клеток).
В пожилом возрасте, когда меняется гормональный фон и происходит естественное угнетение иммунологических реакций, создаются условия для реактивации вируса. Клинически это проявляется в виде опоясывающего герпеса – высыпаний на торсе, образующих сплошную ленту по ходу межреберных нервов. Больных беспокоит зуд и невралгические боли. Как вы видите, вирусы герпеса могут долгие годы ждать удобного случая, «укрываясь» в клетках нервной и иммунной систем.
– Почему вирусы герпеса облюбовали именно эти клетки?
– На этот вопрос сложно ответить. Вирусы появились на земле миллиарды лет назад, а человек как биологическое существо – относительно недавно (как считают специалисты, сотни тысяч лет назад). Поэтому вирусы «хитрее» организма человека. Вирус погружается внутрь клетки, сбрасывает свою защитную оболочку – и процесс пошел. ДНК вируса может встраиваться в ДНК клетки хозяина, и с этого момента он живет и размножается. Но инфицирование – не значит болезнь, и не всегда носитель вируса страдает его проявлениями. 10% населения не болеют вообще или болеют редко и в мягкой стертой форме. Ну а остальным везет меньше. Герпесом могут поражаться печень, легкие, органы зрения, половые органы, железистая ткань, стенки сосудов различных органов. Все это – на фоне гибели или снижения функциональной активности клеток иммунной системы и развития вторичных иммунодефицитных состояний.
– Но основным-то источником заражения являются инфицированные люди?
– Да, а механизмы инфицирования – воздушно-капельный, оральный (через рот), контактный (через микротравмы на коже и слизистых оболочках) и гемоконтактный (через кровь). Факторами передачи инфекции могут быть инфицированные слюной или содержимым пузырьков детские игрушки, предметы обихода – полотенце, посуда, дверные ручки. Вирусы герпеса могут содержаться в слюне, крови, слезной жидкости, содержимом везикул, сперме, секрете влагалища и шейки матки, моче, грудном молоке, различных органах и тканях, используемых для пересадки.
– А если в семье кто-то болеет, значит ли это, что и другие больны или заболеют?
– Риск инфицирования внутри семьи гораздо выше, но это не означает, что все будут болеть одинаково. Бывает, у пациента два или три разных вируса герпеса одновременно, а у членов его семьи – другие комбинации. Поэтому каждого пациента надо обследовать и лечить отдельно.
– Мы поговорили лишь о наиболее распространенных вирусах этого семейства. Сколько же их всего?
– Известно восемь разновидностей вируса. Вирус герпеса 4го типа (вирус Эпштейна – Барр, ВЭБ) – единственный онкогенный среди своего семейства. Живет преимущественно в лимфоидной ткани и вызывает воспаление и боль в лимфоузлах шеи, подмышечных, паховых областях. У детей и взрослых острая форма инфекции называется инфекционным мононуклеозом. Как и в случае ветрянки, 30–40% детей, перенесших это заболевание, становятся пожизненными носителями ВЭБ. На долгий срок даже могут забыть о нем. Но в определенный момент наступает сбой в работе иммунной системы, и пациент начинает болеть. Первая реакция – недоумение. Почему? 10–15 лет не болел, а тут – частые ОРЗ, ангины, фарингиты, немотивированная слабость, повышение температуры. И длиться это может годами. Начинаются поиски причины. Пациенту делают мазки из зева, носа, выделяют, к примеру, стрептококки, назначают антибиотики, и на какое-то время эффект есть. А через три недели все повторяется снова: боли, налеты в горле, слабость, увеличение шейных лимфоузлов. В такой ситуации следует задуматься о герпетической природе такого недомогания и сдать анализы на ВЭБ. А поскольку схожую симптоматику дают еще цитомегаловирус и вирус герпеса 6го типа, то лучше подойти к решению проблемы комплексно.
– Цитомегаловирус имеет какие-то свои особенности?
– Это 5-й тип вируса герпеса, который живет в клетках иммунной системы и поражает в основном внутренние органы: щитовидную, поджелудочную, половые железы. Известны случаи аутоиммунного тиреоидита, тяжелого панкреатита вирусной природы. Особенно это опасно у беременных, так как беременность протекает на фоне физиологического подавления иммунитета (чтобы не было конфликта между матерью и развивающимся плодом) и снижения выработки гормонов. Это идеальные условия для его активации. Цитомегаловирус сильнее других вирусов поражает плод и приводит к нарушениям нервной системы, печени, легких.
– А как ведут себя в нашем организме менее известные вирусы герпеса?
– Вирусы герпеса человека 6-го и 7-го типов менее изучены. Вирус герпеса 6-го типа в чем-то похож на цитомегаловирус, вызывает чаще всего внезапную экзантему (острое инфекционное заболевание детей раннего возраста, протекающее с повышенной температурой и кожными высыпаниями). Герпес 6го типа у детей и взрослых вызывает первичную герпетическую инфекцию, проявляющуюся менингоэнцефалитом разной степени тяжести, поражением печени, воспалительными процессами в легких, бронхах и сердечной мышце.
Вирус герпеса 7-го типа относится к лимфотропным, он пагубно влияет на лимфоциты. Поражает их и вирус герпеса 8-го типа. Но для человека с нормальным иммунитетом опасности он не представляет. И обычно не влияет на здоровье. А проявляет себя лишь у людей со стойким снижением иммунитета, что бывает при СПИДе, пересадке органов, лучевой терапии. Изучение данного вируса продолжается. Однако уже сейчас известно, что он способен вызвать развитие, например, саркомы Капоши – системного заболевания, при котором на коже, слизистых оболочках, в лимфатических узлах и внутренних органах образуются множественные опухоли, разрастающиеся из стенки кровеносных сосудов.
– Герпес так многолик. С ним сталкиваются врачи многих специальностей: гинекологи, урологи, офтальмологи, неврологи, оториноларингологи, педиатры, дерматологи, иммунологи. У кого и как лечиться?
– Надо помнить, что герпесвирусы поражают весь организм в целом. И если необходим результат, нужно выявить причину и пройти комплексное лечение с участием врача-иммунолога, инфекциониста. И уж никак нельзя относиться к этому заболеванию легкомысленно. Герпесвирусы могут быть причиной бесплодия, мертворождения и выкидышей, инициируют процессы атеросклероза и развитие злокачественных новообразований, они могут свести на нет безупречно проведенное хирургическое вмешательство. Например, при протезировании клапанов сердца. Более того, Всемирная организация здравоохранения на ближайшее время поставила проблему борьбы с герпесвирусными инфекциями на первое место. Не ВИЧ и СПИД, не вирусные гепатиты и не грипп. Это такая же реальная опасность.
Поэтому нами создан Кабинет терапии герпесвирусных инфекций и иммунореабилитации. Здесь работают врачи-специалисты доктора и кандидаты медицинских наук: акушеры-гинекологи, инфекционисты, иммунолог, аллерголог. Консультируют терапевт, невролог, оториноларинголог, дерматовенеролог, офтальмолог. Лечение пациента проводится комплексно, применяются новые эффективные технологии с использованием современных противовирусных, иммуномодулирующих и антибактериальных препаратов, вакцин.
– Насколько эффективны эти препараты?
– Полностью уничтожить вирус невозможно. Но можно добиться длительной ремиссии и уменьшить концентрацию вируса во всех биологических жидкостях: слюне, крови, моче. Для этого используются противовирусные препараты последнего поколения, которые обладают «игольчатым» механизмом действия: они менее токсичны и могут применяться годами без негативного воздействия на организм. Также назначается иммуностимулирующая терапия в комплексе с другими местными средствами.
Материал предоставлен газетой «Панацея» (№ 2 (103) февраль 2015 г.)
Записаться на прием к специалисту