Фиброз у детей что это
Врожденный фиброз печени
Врожденный фиброз печени (ВФП) – это генетически детерминированная патология, которая характеризуется портальным фиброзом, нарушением морфогенеза внутрипеченочных ветвей портальной вены и желчных ходов. Клинически она может проявляться портальной гипертензией с желудочно-кишечными кровотечениями и/или холангитом с характерными симптомами. При диагностике наиболее информативными являются лабораторные маркеры фиброза, УЗИ, холангиография, портальная венография и биопсия печени. Лечение симптоматическое. При выраженной гипертензии в системе воротной вены и массивных кровотечениях проводится венозное шунтирование.
Общие сведения
Врожденный фиброз или фиброхолангиокистоз печени у детей – это аутосомно-доминантная наследственная патология, которая характеризуется фиброзными изменениями печени и кистозными аномалиями внутрипеченочных желчных путей. ВФП очень редкое заболевание – распространенность составляет 1:20 000 новорожденных. Часто сопровождается поражением почек – дисплазией, поликистозом или нефронофтизом. Изменение частоты заболеваемости врожденным фиброзом печени в зависимости от пола не прослеживается. Исход патологии зависит от формы, при портальной гипертензии на фоне своевременно проводимых лечебных мероприятий, как правило, прогноз благоприятный, при сочетании с холангитом – сомнительный. В некоторых случаях может наблюдаться прогрессирующая почечная недостаточность или малигнизация участков фиброза с формированием холангиокарциномы.
Причины
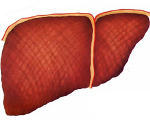
Врожденный фиброз печени – это генетически детерминированная патология, которая передается по аутосомно-доминантному типу. Крайне редко наблюдаются спорадические случаи. Патогенетически ВФП обусловлен аномалией эмбриогенеза протоковой пластинки междолевых желчных ходов. Морфологические изменения включают в себя четко отделенный от печеночной дольки портальный фиброз с сохраненным периферическим слоем нормальных гепатоцитов. Паренхима приобретает характерный вид «географической карты». Внутри развившегося фиброза образовывается большое количество деформированных или дилатированных желчных протоков. Архитектура печеночных ацинусов не нарушена. Артерии, кровоснабжающие печень, как правило, нормальны, вены могут иметь меньший диаметр по сравнению с нормой. Признаков воспаления или холестаза не возникает.
Классификация
Выделяют три основные клинические формы врожденного фиброза печени:
Симптомы ВФП
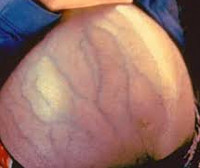
Выраженная клиническая картина врожденного фиброза печени формируется у детей от 3 до 13 лет, редко – во взрослом возрасте. Симптомы варьируют в зависимости от формы патологии. ВФП с портальной гипертензией проявляется гепатоспленомегалией и желудочно-кишечными кровотечениями разной интенсивности из расширенных вен пищевода или прямой кишки. До 5 лет данная форма врожденного фиброза печени, как правило, не обнаруживается. Первичный симптом – гепатоспленомегалия, которая у детей может проявляться увеличением живота.
При небольших кровотечениях постепенно формируется клиника хронической постгеморрагической анемии: слабость, бледность кожных покровов, головокружение, потеря аппетита, сухость кожи, нарушения со стороны ногтей и волос, стабильная тахикардия. Через некоторое время может возникнуть массивное желудочно-кишечноее кровотечение. Помимо острого геморрагического синдрома наблюдаются характерные симптомы: при разрыве вен пищевода — рвота кровью, при кровотечении из прямой кишки – примесь неизмененной крови или мелена.
Врожденный фиброз печени с холангитом может диагностироваться уже с трехлетнего возраста. Он характеризуется острыми болями в правой подреберной области, повышением температуры тела до 38,5-39°С. Реже возникает желтуха, проявляющаяся пожелтением склер, слизистых оболочек рта, затем — кожных покровов. Часто данная форма сопровождается холелитиазом с соответствующей для педиатрии клиникой. Изолированный ВФП с холангитом встречается редко, обычно наблюдается сочетание с портальной гипертензией.
Комбинированная форма врожденного фиброза печени сочетает в себе портальную гипертензию и холангит. Как правило, особенно при позднем проявлении (после 7-10 лет и во взрослом возрасте), первично возникает гипертензия в системе воротной вены, которая позже дополняется холангитом. Также ВФП часто сопровождается поражением почек в виде почечной дисплазии, поликистоза почек и нефронофтиза с клиникой почечной недостаточности и другими симптомами данных патологий.
Диагностика
Диагностика врожденного фиброза печени основывается на данных анамнеза, объективном осмотре ребенка, лабораторных и инструментальных методах исследования. Анамнестические данные, как правило, дают возможность выявить данное заболевание аналогичной или иной формы у родителей или других родственников. При физикальном осмотре педиатром определяются неспецифические симптомы: гепатоспленомегалия, анемический синдром, клинические проявления холангита и холелитиаза.
Лабораторная диагностика при врожденном фиброзе печени позволяет обнаружить небольшое повышение уровня щелочной фосфатазы в плазме, наличие скрытой крови в кале. Могут определяться признаки железодефицитной анемии, а при обострении холангита – лейкоцитоз со смещением формулы влево, повышение СОЭ. Печеночные ферменты (АлТ, АсТ), протеинограмма, билирубин, как правило, в пределах нормы. Также существуют маркеры фиброза: гиалуроновая кислота, проколлаген III, ламинин, коллаген IV типа и другие.
Ведущую роль в диагностике врожденного фиброза печени играют инструментальные методы диагностики – УЗИ, КТ, холангиография, портография и биопсия печени. При ультразвуковом исследовании и компьютерной томографии определяются высокоэхогенные очаги, которые соответствуют фиброзным тяжам. Также могут быть обнаружены камни в желчных путях и сопутствующие поражения почек.
При трансдермальной или эндоскопической холангиографии можно выявить стенозирование внутрипеченочных желчных протоков. Портальная венография дает возможность визуализировать усиленное кровенаполнение венозных коллатералей, возможные аномалии внутрипеченочных ветвей воротной вены. Диагноз врожденного фиброза печени у детей в 35-50% случаев удается подтвердить путем пункционной биопсии. При гистологическом анализе полученного фрагмента определяются характерные для данной патологии морфологические изменения.
Дифференциальный диагноз врожденного фиброза печени проводится с инфантильным гепаторенальным поликистозом и поликистозом печени взрослого типа, а также с приобретенными патологиями, которые сопровождаются портальной гипертензией и/или поражением желчевыводящих путей.
Лечение при ВФП
Лечение врожденного фиброза печени проводится педиатром, детским гастроэнтерологом и гепатологом, заключается в предупреждении желудочно-кишечных кровотечений и острых холангитов. При небольших и редких кровотечениях из расширенных эзофагеальных вен проводится их эндоскопическое склерозирование. При выраженной портальной гипертензии показано венозное шунтирование. Чаще всего соединяют воротную и нижнюю полую, селезеночную и почечную вены или накладывают илеомезентерикокавальный анастомоз. Данные оперативные вмешательства проводятся после эпизодов массивных кровотечений с целью профилактики рецидива, редко – только при наличии признаков портальной гипертензии. Профилактика обострений холангита при врожденном фиброзе печени включает регулярное полноценное питание, раннюю диагностику и лечение любых заболеваний ЖКТ. При формировании больших камней желчевыводящих путей осуществляется их хирургическое удаление.
Прогноз и профилактика
Профилактика врожденного фиброза печени подразумевает медико-генетическое консультирование семейных пар. В центрах планирования семьи составляется родословная с целью оценки вероятности возникновения данной патологии у будущего ребенка.
Фиброз легких
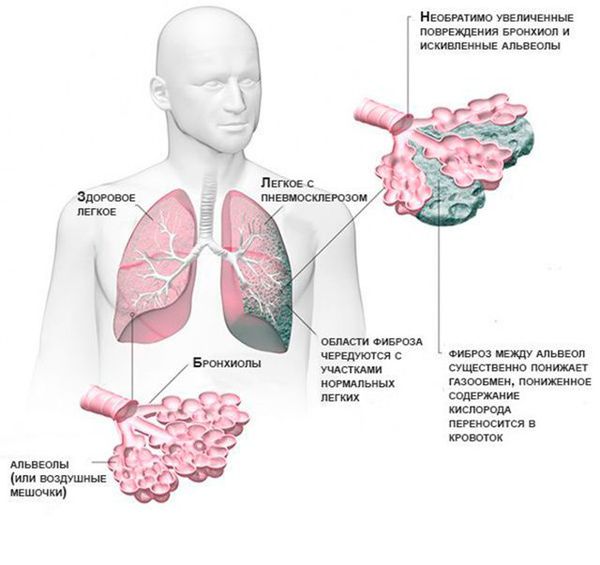
Патологический процесс разрастания в легких фиброзной (соединительной или рубцовой) ткани с постепенным замещением ею легочной альвеолярной ткани называют фиброзом. Процесс характеризуется постепенным снижением дыхательной функции вплоть до критического уровня. Ткань, образующая легкие, становится все менее эластичной и растяжимой. Уплотнение затрудняет газовый обмен: кислороду и углекислому газу становится сложнее проникать через стенки альвеол, способность легких к расширению постепенно теряется. В зависимости от локализации образования фиброзных участков и причин их появления зависит общее течение болезни.
Почему происходит разрастание рубцовой ткани
Часто причиной развития фиброза легких становится заболевание, поражающее легочную ткань:
В тех случаях, когда установить заболевание, вызвавшее рост соединительной ткани в легких, не удается, медики говорят об идиопатическом легочном фиброзе.
Как распознать заболевание
На ранней стадии процесс замещения легочной ткани рубцовыми образованиями заметить практически невозможно, поскольку этот процесс протекает бессимптомно и до определенного момента не доставляет пациенту дискомфорта. Характерные симптомы фиброза легких появляются после того, как процесс охватывает существенную часть легких, из-за чего становится заметным снижение дыхательной функции, выражающееся в:
Перечисленные признаки могут говорить и о других, не менее серьезных заболеваниях, поэтому при их появлении необходимо обратиться к врачу и пройти обследование своего состояния.
Диагностические методы
Чтобы выявить легочный фиброз, врач назначает ряд исследований:
При необходимости может быть проведена биопсия легочной ткани.
Современные методы лечения
В настоящее время не существует методов лечения фиброза легких, которые приводили бы к восстановлению легочной ткани в полном либо даже частичном объеме. Задачей врача становится определение причины, вызывающей разрастание соединительной ткани, и прекращение этого процесса. Определенные успехи в этом направлении уже достигнуты. В случаях, когда фиброз является следствием воспалительного либо аутоиммунного процесса, терапия устраняет воспалительный процесс, и разрастание фиброзной ткани прекращается.
В целом, лечение фиброза включает:
При сильном поражении легочной ткани пациенту в молодом возрасте назначают трансплантацию легких либо хирургическое удаление очага разрастания фиброзной ткани.
В специальном питании при фиброзе легких нет необходимости. Рацион больного должен быть здоровым и разнообразным, желательно с повышенным содержанием белковых продуктов. Рекомендовано деление суточного количества пищи на небольшие порции, употребляемые через небольшие промежутки времени. Категорически запрещено курение, в том числе пассивное. Пациенту необходимо избегать стрессов и освоить приемы, улучшающие дыхательную функцию.
Часто задаваемые вопросы
Чем опасен фиброз легких для человека?
Разрастание фиброзной ткани приводит к уменьшению рабочего объема легких и снижению количества воздуха, поступающего в организм при вдохе. Человеку недостает кислорода, он начинает задыхаться при ходьбе, а впоследствии и в спокойном состоянии. Легочная недостаточность приводит к развитию легочной гипертензии, эмфиземе легких, кровотечению, пневмотораксу, разрыву легкого. Существенно повышается риск перерождения легочной ткани в злокачественную опухоль.
Как остановить фиброз легких народными средствами?
Рецепты народной медицины во многих случаях превосходно дополняют основной курс лечения фиброза, однако использовать их можно лишь после консультации с лечащим врачом. Среди наиболее популярных средств – отвар анисовых семян (столовую ложку семян заливают стаканом кипятка) и чай из смеси измельченных ягод шиповника с корнем девясила.
Как понять, что у тебя фиброз легких?
Если вы постоянно ощущаете одышку, нехватку воздуха и дискомфорт в груди, необходимо обратиться к пульмонологу (врачу, специализирующемуся в лечении болезней легких) или вашему участковому терапевту, который направит вас на консультацию к специалисту. Диагностировать фиброз можно лишь после проведения рентгеновского исследования.
Не нашли ответа на свой вопрос?
Наши специалисты готовы проконсультировать вас по телефону:
Что такое муковисцидоз (кистозный фиброз)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Кольцова Е. В., пульмонолога со стажем в 6 лет.
Определение болезни. Причины заболевания
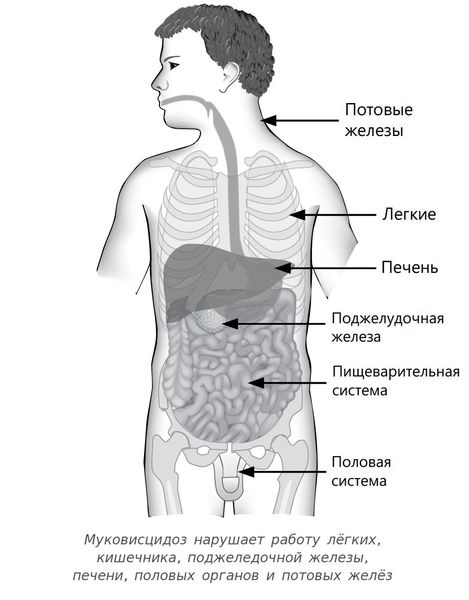
Муковисцидоз — это наследственное заболевание, при котором нарушаются функции желёз внешней секреции. Болезнь поражает весь организм, но сильнее всего страдает дыхательная система и поджелудочная железа.
Заболевание также называется кистозным фиброзом, синдромом Фанкони. Характеризуется системным поражением экзокринных желез: слизеообразующих (респираторных, кишечника, поджелудочной) и серозных (слюнных, потовых, слезных).
В некоторых случаях симптомы болезни проявляются не сразу. Это связано с тем, что тяжесть и форма заболевания у разных больных отличаются. Кроме того, признаки муковисцидоза могут напоминать симптомы других болезней, что затрудняет диагностику. Без лечения подавляющее большинство больных умирает в детском возрасте, но благодаря современным лекарственным препаратам и другим методам лечения продолжительность жизни пациентов постоянно растёт.
Чаще всего без адекватного лечения болезнь протекает тяжело и имеет плохой прогноз, на который во многом влияет развитие хронической инфекции в нижних дыхательных путях. Бактериальные агенты при муковисцидозе специфичны, например, для раннего возраста характерно развитие инфекции, вызванной золотистым стафилококком, в дальнейшем к нему присоединяются синегнойная и гемофильная палочки. Данные возбудители устойчивы к лекарственным препаратам, что осложняет лечение, поэтому важно своевременно идентифицировать возбудителя и подобрать подходящие антибактериальные средства.
Симптомы муковисцидоза
При муковисцидозе симптомы болезни зачастую видны сразу после рождения ребёнка и проявляются признаками непроходимости кишечника (мекониальным илеусом):
В возрасте одного года у ребёнка с муковисцидозом может наблюдаться обильный, зловонный стул непереваренной пищей, частый сухой кашель, отставание в физическом развитии и длительная желтуха.
Иногда признаки заболевания проявляются только в школьном возрасте. Дети с муковисцидозом из-за нехватки питательных веществ страдают дефицитом массы тела и отстают в росте.
Для заболевания также характерны:
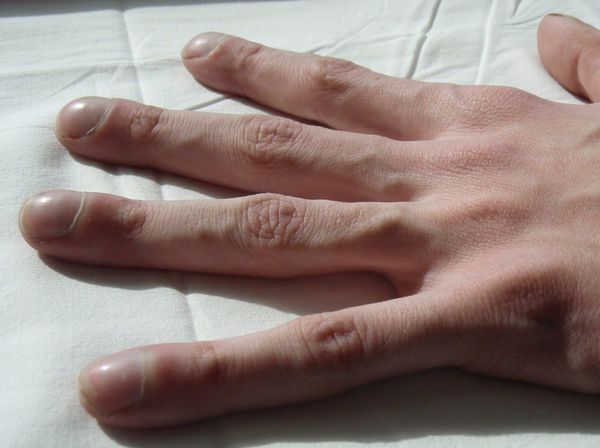
У заболевших в раннем детстве и доживших до взрослого возраста отмечаются постоянный сухой кашель, вне обострения чаще наблюдается постоянное отделение мокроты от 5-10 мл до 200 мл и более. Характер мокроты — от слизистой до гнойной. О дышка, которая в начале болезни может возникать только при небольшой нагрузке, но со временем усиливается, частые респираторные заболевания и гаймориты. У пациентов выражена задержка роста, фаланги пальцев и ногти изменяются по типу «барабанных палочек» и «часовых стёкол».
Грудная клетка чаще бочкообразной формы. Появляется бледность, одутловатость лица и цианоз видимых слизистых.
У больных может наблюдаться задержка в половом развитии или отсутствие вторичных половых признаков:
Патогенез муковисцидоза
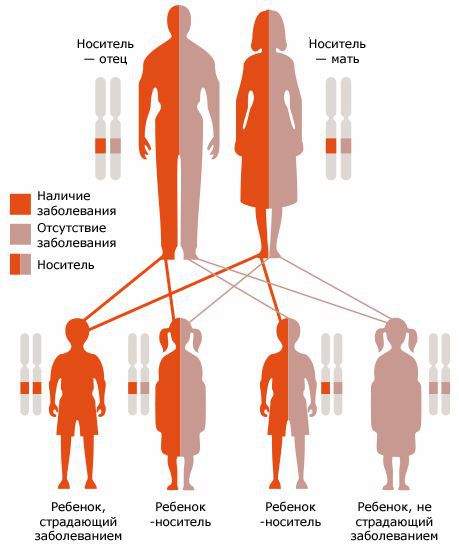
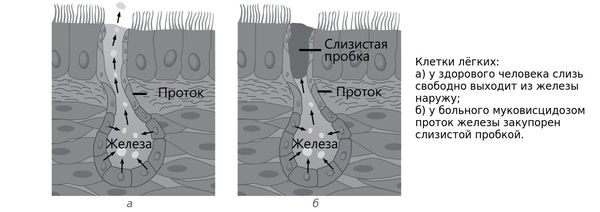
Патогенез муковисцидоза обусловлен мутацией гена CFTR (Cystic Fibrosis Transmembrane conductance Regulator) — муковисцидозного трансмембранного регулятора проводимости. Этот ген кодирует белок, который обеспечивает транспорт солей и воды в эпителиальном слое бронхолёгочной системы и в клетках, выстилающих железы, вырабатывающие секрет и выводящие его во внешнюю среду организма. Из-за дефекта структуры белка нарушается перемещение ионов натрия и хлора в клетках, что в итоге приводит к повышенной вязкости секрета экзокринных желез. Происходит увеличение всасывания ионов натрия и дефект секреции хлора, что ведёт к снижению или прекращению выделения жидкости в просвет бронхов. Из-за этого мокрота теряет свою жидкую часть, становится вязкой и густой. Впоследствии это ведёт к тому, что бронхи забиваются вязким секретом.
Таким образом, при муковисцидозе нарушаются функции желёз, которые вырабатывают пот, слизь, слёзы, слюну и пищеварительные соки. Через протоки этих желёз выделения выходят на поверхность тела или в полые органы, такие как кишечник или дыхательные пути. У пациентов с муковисцидозом в этих органах возникают серьёзные изменения, особенно они затрагивают бронхолёгочную систему — в язкий секрет закупоривает мелкие дыхательные пути.
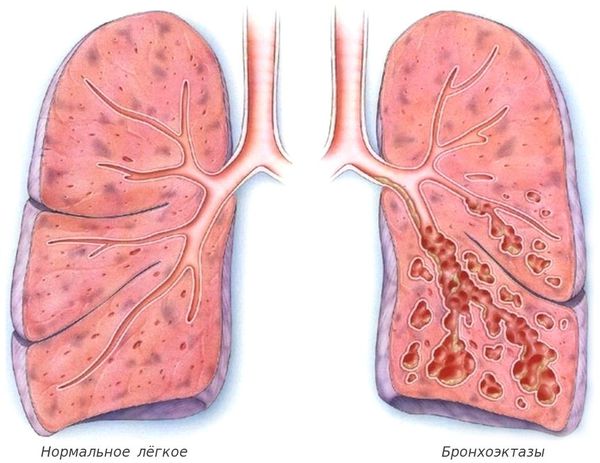
С лизь, выделяемая в дыхательных путях, необходима для удаления из них пыли и бактерий, но при муковисцидозе выработка и структура бронхиального секрета нарушаются. В результате на стенках дыхательных путей развивается хроническое воспаление, которое впоследствии приводит к формированию бронхоэктазов (расширения и деструкции бронхов) и рубцов в лёгочной ткани.
При муковисцидозе страдает не только дренажная функция дыхательных путей, но и клеточный и гуморальный иммунитет. Это происходит из-за нарушений в работе клеток и затруднённого движения ресничек мерцательного эпителия бронхов.
Помимо этого, при муковисцидозе ферменты, вырабатываемые поджелудочной железой, не поступают в кишечник. Они начинают разрушать ткань поджелудочной железы, в результате чего в ней формируются рубцы и кисты. Также необратимо нарушается весь процесс пищеварения. Это приводит к недостаточности массы тела, отставанию в росте и весе, хронической диарее и выпадению прямой кишки.
При муковисцидозе у мужчин отмечается обструкция (непроходимость) семявыносящих протоков, отсюда и высокий процент мужского бесплодия при заболевании.
Классификация и стадии развития муковисцидоза
В зависимости от преобладающих симптомов выделяют три основные клинические формы заболевания: кишечную, бронхолёгочную и смешанную.
Кишечная форма муковисцидоза. Кистозный фиброз с кишечными проявлениями Е84.1 (код по МКБ-10)
Из-за неправильной секреции ферментов нарушается работа органов желудочно-кишечного тракта. Ухудшается расщепление жиров, белков и углеводов, а также их усвоение. Не вся пища переваривается, стул становится обильным, частым и зловонным.
Бронхолёгочная форма муковисцидоза. Кистозный фиброз с лёгочными проявлениями Е84.0
Нарушения затрагивают всю бронхолёгочную систему. Вязкая мокрота скапливается в дыхательных путях и её тяжело откашлять. При инфицировании золотистым стафилококком, синегнойной и гемофильной палочками возникают тяжёлые бронхиты и пневмонии, для которых характерно осложнённое течение с развитием одышки, интоксикации и выраженной слабостью. Со временем развиваются следующие необратимые изменения:
Смешанная форма (лёгочно-кишечная)
Различают четыре стадии развития муковисцидоза:
1. Непостоянство симптомов, пациент жалуется на частый сухой кашель и небольшую одышку при физических нагрузках. Стадия может длиться до 10 лет.
2. Кашель с отделением мокроты, одышка появляется в покое и усиливается при физической нагрузке, фаланги пальцев и ногтевые пластины деформируются по типу «барабанных палочек» и «часовых стёкол». Стадия продолжается от 2 до 15 лет.
3. Бронхолёгочные симптомы прогрессируют, развиваются тяжёлые осложнения. У пациентов усиливается одышка и появляются признаки сердечной недостаточности: отёки на ногах, одышка при небольшой активности или в покое, быстрая утомляемость, непереносимость физических нагрузок. На УЗИ сердца видны признаки гипертрофии левых и правых отделов, а также снижение сердечной фракции выброса левого желудочка. На рентгенологических снимках можно обнаружить зоны пневмофиброза, бронхоэктазы и кисты. Формируется сердечная недостаточность по правожелудочковому типу, так называемое «лёгочное сердце». Длительность стадии от 3 до 5 лет.
4. Тяжёлая кардио-респираторная недостаточность. Из-за дисфункции левого желудочка нарушается работа сердца и лёгких, снижается фракция выброса левого желудочка, учащается сердцебиение, прогрессирует гипотензия. Стадия длится несколько месяцев и завершается смертью больного, вызванной развитием дыхательной недостаточности и остановкой сердечной деятельности.
Различают стадии обострения и ремиссии:
Осложнения муковисцидоза
Для муковисцидоза характерны следующие бронхолёгочные осложнения:
Пациенты жалуются на выраженную одышку, отмечаются симптомы сильной интоксикации, повышается температура и выделяется большое количество зловонной гнойной мокроты.
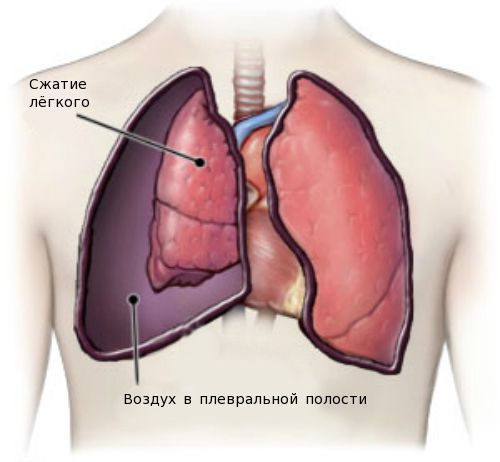
Одним из тяжёлых осложнений является спонтанный пневмоторакс — скопление воздуха в плевральной полости. Нарушение проявляется резкой колющей болью в грудной клетке, усиливающейся при дыхании, кашле и движениях. Больной начинает дышать часто и поверхностно, отмечается сильная одышка и чувство нехватки воздуха, беспокоит кашель, появляется синюшность кожных покровов лица.
У больных старше 12 лет высока вероятность развития сахарного диабета I типа, может наблюдаться остеопороз, артриты и отёки нижних конечностей.
Постоянные или частые боли в животе могут указывать на панкреатит, эзофагит или язвенную болезнь желудка и двенадцатиперстной кишки.
Диагностика муковисцидоза
Основной критерий постановки диагноза — увеличение концентрации ионов хлора в потовых железах более 60 ммоль/л вместе с одним или более из следующих критериев:
Характерные клинические проявления болезни:
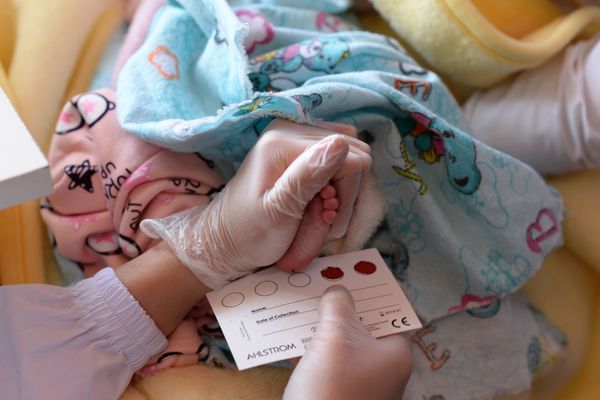
Скрининг на муковисцидоз проводится в роддоме всем новорождённым и направлен на выявление заболевания ещё до клинических проявлений. Для этого у ребёнка на 4-7 день жизни берётся кровь из пятки на фильтровальную бумагу и определяют уровень иммунореактивного трипсина (ИРТ). Если показатели ИРТ превышены (норма не более 65-70 нг/мл), то на 21-28 день анализ повторяют. Если показатели остаются повышенными, ребёнку проводится потовая проба и генетическое обследование.
Потовая проба — это один из методов диагностики муковисцидоза, с помощью которого определяется уровень хлоридов в секрете потовых желез. Анализ проводится троекратно. Положительным результатом для постановки диагноза считается показатель выше 60 ммоль/л.
Методика проведения потовой пробы: кожу правого бедра новорождённого протирают раствором натрия хлорида, дают высохнуть, после кладут салфетку, смоченную раствором пилокарпина для провоцирования гипергидроза и вторую салфетку, смоченную солёной водой. На салфетках закрепляются электроды, в течение 5 минут подаётся разряд 4 мА, после чего электроды снимаются, и кожа протирается. На простимулированном участке фиксируется кусочек фильтровальной бумаги. Выделяющийся пот собирается в течение 30 минут, после чего бумагу снимают и отсылают в лабораторию для определения концентрации электролитов хлора и натрия.
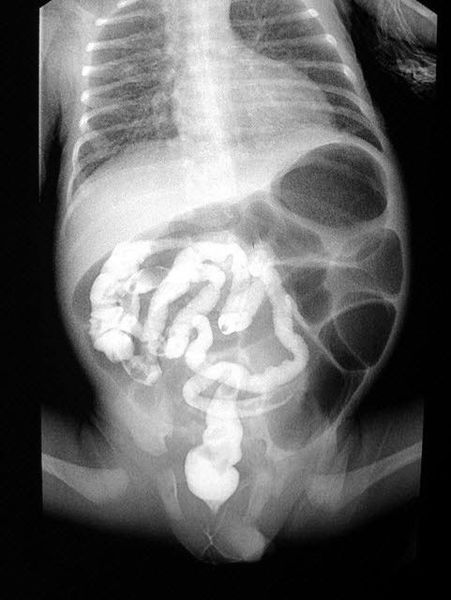
Обзорную рентгенограмму брюшной полости проводят для выявления вздутых петель кишечника и признаков кишечной непроходимости. При осмотре может быть обнаружено увеличение печени (гепатомегалия). Также у пациентов выявляют сахарный диабет I типа, который сочетается с респираторными симптомами: одышкой, частым кашлем с трудноотделяемой вязкой мокротой и панкреатитом, проявляющимся опоясывающими болями в области живота и частым стулом непереваренной пищей.
Молекулярно-генетический анализ позволяет диагностировать муковисцидоз приблизительно в 90 % случаев. Для его проведения нужна кровь из вены. Генетический метод обнаруживает в хромосомах пациента «дефектный» ген с мутацией F508del. При тестировании на муковисцидоз невозможно проверить все мутации, так как их более 1900, а большинство лабораторий выявляет только 20-30 самых частых вариантов.
Лечение муковисцидоза
Муковисцидоз носит наследственный характер, поэтому его лечение большей частью симптоматическое, оно направлено на восстановление функций дыхательного и желудочно-кишечного тракта и проводится на протяжении всей жизни пациента. Больным муковисцидозом важно соблюдать диету, выполнять специальный комплекс упражнений и принимать препараты, предотвращающие развитие инфекций.
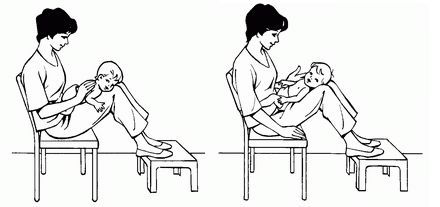
Основной целью лечения при муковисцидозе является удаление из дыхательных путей вязкой мокроты. Для этого применяют различные методики дренирования бронхиального дерева, например кинезотерапию — одну из форм лечебной физкультуры, способствующую очищению бронхов от вязкой и агрессивной слизи.
Физиотерапевтическое лечение младенцев и детей раннего возраста включает как активную, так и пассивную техники.
Пассивная техника:
• принятие телом ребёнка определённого положения на короткое время, затем его изменение;
• сопровождение и стимуляция дыхательных движений при помощи рук (контакт-дыхание) — техника, при которой рука физиотерапевта ведёт и стимулирует дыхательные движения;
• ручная вибрация на выдохе — для поддержки выдоха и помощи высвобождению мокроты потряхивается грудную клетку рукой;
• потряхивание — ритмические движения, выполняемые в одной из частей тела для возникновения реакции в грудной клетке;
• терапевтические положения тела — расположение грудной клетки в состоянии, при котором растягивается лёгочная ткань и расширяются дыхательные пути.
Активная техника:
• влияние на дыхание, например с помощью акустической стимуляции — поощряя ребёнка повторять громкие крики, которые он издаёт;
• упражнения для развития эластичности грудной клетки, позвоночника и мышечного баланса тела;
• упражнения, повышающие ловкость, выносливость и формирующие наслаждение от мышечной активности.
При муковисцидозе важно соблюдать диету — питание должно быть высококалорийным, с повышенным содержанием белков и жиров. Пищу принимают часто и небольшими порциями, дополнительно подсаливая. Из рациона исключается еда, которая тяжела для переваривания: грубая клетчатка, навары из супов, жареные блюда, шоколад, торты, пирожные. Суточный калораж должен превышать возрастную норму на 20—40 %, главным образом за счёт увеличенного количества белка (до 6 г на 1 кг массы тела в сутки). Из-за нарушенной функции поджелудочной железы у больных не усваиваются жиры и жирорастворимые витамины А, Д, Е и К, поэтому необходим их дополнительный приём.
Для облегчения отхождения мокроты применяют следующие препараты:
Для ингаляционной терапии используют бронхолитики:
Следует иметь в виду, что у трети больных бронхолитики оказывают положительный ответ, но у большей части может возникнуть коллапс мышц дыхательных путей и резкое снижение объёма выдыхаемого воздуха. В связи с этим больные, получающие такую терапию, должны находиться под наблюдением врача.
Антибактериальные препараты назначаются всем пациентам с лёгочными симптомами, при обострениях заболевания или выявлении возбудителей респираторных инфекций для подавления их роста.
Для лечения применяют эффективные комбинации антисинегнойных антибиотиков:
Парентеральные антибиотики:
Доза вводимого антибактериального препарата должна превышать среднюю терапевтическую в полтора раза. Курс антибактериальной терапии может продолжаться до 3-4 недель,в случае хронизации инфекционного процесса — до 12 недель.
Для улучшения функции пищеварения используют ферментные препараты, которые содержат липазу, протеазу и амилазу, облегчающие переваривание жиров, углеводов и белков, а также способствующие их лучшему всасыванию в тонком кишечнике. Подбор доз панкреатических ферментов проводится индивидуально исходя из клинических проявлений болезни. Применяются препараты: «Панкреатин», «Мезим», «Креон». Ферментные препараты назначаются в больших дозах, чем больным с другими заболеваниями желудочно-кишечного тракта — до 30 капсул «Креона» в сутки.
Лечение муковисцидоза пожизненное. Выбор схемы терапии зависит от вида бактерий, обнаруженных в бронхиальном секрете дыхательных путей, а также от преобладающих клинических форм заболевания.
В России оригинальные препараты для лечения муковисцидоза заменяются дженерикам отечественного производства. Дженерики сходны с оригинальными препаратами по составу действующего вещества. Многие пациенты жалуются на их плохое качество и появление побочных эффектов. В последнее время пациентами и родителями больных муковисцидозом проводятся кампании, цель которых — вернуть государственное обеспечение качественными иностранными лекарствами.
Назвать побочные эффекты дженериков на данный момент сложно, так как отсутствуют их сравнительные исследования с оригинальными препаратами.
В рамках 44-ого ФЗ закупки лекарственных препаратов идут по международному непатентованному названию. Перечень лекарственных препаратов утверждается правительством РФ. Врачам за назначение препаратов под торговыми названиями или купленными родителями и благотворительными фондами грозит ответственность. В рецептах, выписанных врачом, должны быть указаны только международные названия, а не торговые. За нарушение этого правила врачей ждет штраф.
Хотя есть одно условие: при наличии медицинских показаний (аллергия, индивидуальная непереносимость дженерика по жизненным показаниям) по решению врачебной комиссии пациент может получить лекарство под торговым названием. Поэтому возможность получить оригинальный препарат — индивидуальная непереносимость дженерика (которую нужно доказать) и решение врачебной комиссии.
Муковисцидоз — наиболее частое показание для трансплантации лёгких. Основные показания для этой операции: прогрессирующее снижение веса, ухудшение лёгочной функции, частые обострения, потребность в кислородотерапии. Противопоказания: аспергиллома ( опухолевоподобное неинвазивное новообразование шаровидной формы, состоящее в основном из клеток мицелия микроскопического плесневого гриба ), курение, психосоциальные факторы. Сахарный диабет и лечение кортикостероидами не являются препятствием для трансплантации.
Прогноз. Профилактика
Муковисцидоз — это неизлечимое хроническое заболевание, но при своевременной диагностике и адекватной постоянной терапии многие пациенты доживают до взрослого возраста.
Для больных муковисцидозом возможна полноценная жизнь, но только при условии постоянного получения необходимых препаратов. Основными причинами смертности этих пациентов являются бронхолёгочные осложнения: развитие инфекции в нижних дыхательных путях, бронхоэктазы и хроническая обструктивная болезнь легких (ХОБЛ).
Главным способом профилактики является дородовая и неонатальная диагностика. Семейным парам, планирующим рождение ребенка, рекомендуется пройти ДНК-диагностику на носительство мутаций, приводящих к муковисцидозу, с последующей консультацией врача-генетика.
Пренатальная ДНК-диагностика выполняется при заборе околоплодных вод в ранний (13-14 недель) и поздний (16-20 недель беременности) сроки. Обследование проводят для семей, в которых выявлено носительство мутации гена CFTR и имеющих ребёнка больного муковисцидозом.