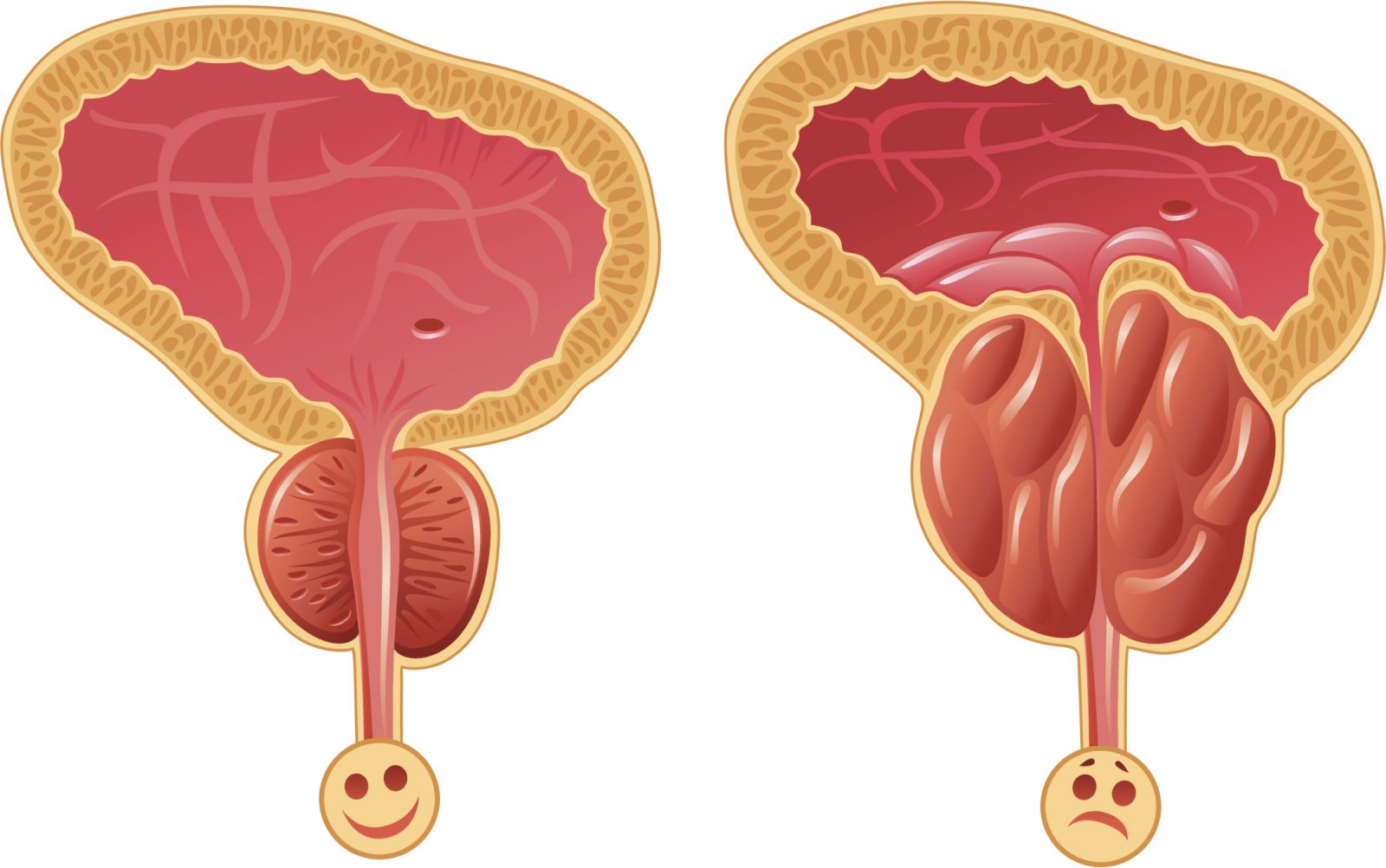
Фокусин или омник что эффективнее
Сравнительный анализ препаратов Кардура, Омник и Урорек
Каждый из рассматриваемых мною препаратов изложен в Интернете на сайтах, специально посвященных лекарствам от простатита, поэтому я не буду уделять подробного внимания ни механизму действия, ни формам выпуска, ни фармакокинетике и фармакодинамике, ни другим сложным и интересным лишь для профессионала характеристикам. Считаю важным рассматривать средства от простатита лишь с точки зрения врача уролога с опытом работы 15 лет.
На всякий случай уточняю. Я не сотрудничаю ни с какой фармфирмой и не занимаюсь ни рекламой, ни антирекламой препаратов, а так же не претендую на истину в последней инстанции. Это всего лишь мое мнение, написанное исключительно для моих пациентов.
Все три препарата относятся к классу так называемых адреноблокаторов. Точкой приложения этой группы являются адренорецепторы, отвечающие за расслабление гладкой мускулатуры. Поскольку гладкие мышцы образуют стенку органов ЖКТ, мочевой системы и сосудов первый препарат этой группы «Кардура» фирмы «Пфайзер» помимо основного, положительного, эффекта (о нем поговорим чуть ниже) вызывает два нежелательных эффекты – снижение моторики кишечника и снижение АД (вплоть до его резкого падения — коллапса). Для того, чтобы минимизировать эти нежелательные эффекты фирма производитель рекомендует работать с дозой препарата (постепенно наращивают, подбирая необходимую). Это сложно и долго и для пациента и для врача. Поэтому, по моему мнению, «Кардура» имеет право на жизнь только при аллергии на все другие альфаблокаторы.
Главный положительный эффект препаратов данной группы является быстрое и выраженное уменьшение таких нарушений мочеиспускания, как затрудненное мочеиспускание и неполное опорожнение мочевого пузыря. Т.е. мы можем рассчитывать ТОЛЬКО на быстрый локальный тактический результат (симптоматическое лечение). Ни о каком полноценном лечении простатита или аденомы не может быть и речи.
В чем разница этих двух препаратов. Окас можно разжевывать до порошка – это никак не влияет на его работу. А вот с Омником такого делать категорически нельзя. Поэтому Окас хорошо идет пациентам, у которых есть затруднения при глотании таблеток (пожилые, люди после операций на пищеводе и др.).
Урорек позиционируется фирмой «Рекодати» как еще более селективный препарат (еще меньше % побочных эффектов). Однако на практике я не заметил у него принципиальных отличий от Омника. В то же время купить его в аптечной сети гораздо труднее.
Важный нюанс. И Омник, и Урорек – это мощные, хорошие, достаточно эффективные препараты, с относительно низкой частотой побочных эффектов, но – только если правильно рассчитана доза, время и длительность приема с учетом ряда параметров. Стандартная, наиболее распространенная схема, такова — 1 таб. 1 раз в день, утром, 7-30 дней. Однако, следует помнить, что отсутствие коррекции препараты с учетом работы ССС, веса и аллергического анамнеза может привести к тому, что возникнут серьезные побочные эффекты или препараты дадут очень слабый эффект.
И последнее. Некоторые пациенты могут мне возразить: «Доктор, а вот я (или мой хороший знакомый) вот уже год или два пьем только Омник Окас и чувствуем себя хорошо». Да, некоторые симптомы нижних мочевых путей Омник действительно снимает очень хорошо (и еще поэтому я достаточно часто использую альфаблокаторы), но на основной процесс воспаления он НЕ ДЕЙСТВУЕТ. По данным обследования у таких пациентов простатит исподволь прогрессирует (в этом коварство простатита) и через некоторое время Омник, а вместе с ним ряд других лекарств, просто перестает действовать – развиваются осложнения в виде падения потенции, увеличивается риск аденомы простаты и т. д.
Резюмируя вышесказанное хочу сказать, что если у пациента по тем или иным причинам нет возможности посетить уролога в ближайшее время, а нарушения мочеиспускания резко ухудшают его качество жизни прием Омника, Омника Окаса или Урорека на короткое время вполне оправдан.
После написания этой статьи я получил от пациентов ряд писем, одно из которых хочу опубликовать.
«Дмитрий Анатольевич, принимал Кардуру. Полностью согласен с вышеописанным. Давление падало, с кишечником было не очень, да еще на фоне дисбактериоза кишечника. Но от кардуры не было ретроградной эякуляции. Пропил курс Кардуры месяц. Сейчас врач назначил мне Урорек, хотя я просил не назначать препараты с ретроградной эякуляцией. В свое время врач мне из-за этого отменял омник. Но видимо уже не помнит, назначил похоже другую марку, вместо омника и все. Другой уролог мне предлагает пропить дальфаз ретард, Который стоит в 2-3 раза дороже, почти 2 000 рублей. Говорит, что эффект от него хороший, а побочных эффектов с эякуляцией нет, или менее выражены. Подскажите, пожалуйста, как ведет себя Дальфаз ретард в сравнении с Урореком, Кардурой? Может быть есть вообще какая-то растительная замена этим всем блокаторам? Сейчас я еще принимаю Гентос. Еще раз спасибо за статью.»
Ответ: Здравствуйте. Дальфаз, на мой взгляд, принципиально не отличается от других препаратов этой группы. Его «великолепное действие» на практике обычно. В тоже время за бренд переплата достаточно высокая.
Современные возможности медикаментозного лечения доброкачественной гиперплазии ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2].
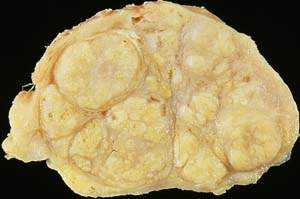 |
| Рисунок 1. Доброкачественная гиперплазия предстательной железы (макропрепарат) |
К числу наиболее распространенных урологических заболеваний у пациентов пожилого возраста относится доброкачественная гиперплазия предстательной железы (ДГПЖ) [2]. Около 80% мужчин старше 80 лет страдают этим заболеванием. Другая статистика свидетельствует, что из всех заболеваний, которым подвержены мужчины старше 50 лет, на долю доброкачественной гиперплазии простаты приходится 36% [1]. Эти сведения настолько общеизвестны, что ухудшение качества мочеиспускания часто рассматривается как естественное явление.
Клинически данное заболевание проявляется различными симптомами, связанными с нарушением пассажа мочи по нижним мочевым путям. При значительно выраженной инфравезикальной обструкции, как правило, прибегают к хирургическому вмешательству. Оперативное лечение по поводу ДГПЖ показано 30% больных в возрасте от 50 до 80 лет [4]. Однако в последние годы все большую популярность завоевывает медикаментозная терапия доброкачественной гиперплазии предстательной железы. Это, с одной стороны, объясняется вполне логичным желанием врача и пациента по возможности избежать операции, с другой — развитием представлений о патогенезе расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы.
До недавнего времени патогенез расстройств мочеиспускания при доброкачественной гиперплазии предстательной железы рассматривали с позиции классических представлений о механической инфравезикальной обструкции и развитии вторичных структурно-функциональных изменений детрузора (компенсация, декомпенсация). За последние два десятилетия получены принципиально новые данные о природе повышенного внутриуретрального сопротивления. Его перестали отождествлять исключительно с механическим сдавлением шейки мочевого пузыря и задней уретры. Обнаружен динамический компонент обструкции, который состоит в повышении тонуса указанных анатомических структур за счет активности a-адренорецепторов. Появились также иные трактовки происхождения ирритативных симптомов. Их считают проявлением первичного нестабильного мочевого пузыря и не связывают напрямую с обструкцией [5].
Результаты нашей работы свидетельствуют, что при ДГПЖ клиническая симптоматика развивается вследствие недостаточности энергетического метаболизма и гипоксии детрузора в условиях повышенного уретрального сопротивления [3]. Об этом свидетельствуют:
Причины нарушений энергетического метаболизма и функций детрузора крайне многообразны. В частности, к таким нарушениям могут привести повышение активности симпатической нервной системы, расстройства органного кровообращения, авитаминоз (группа В), хронические заболевания дыхательной и сердечно-сосудистой систем, влияние приема ряда фармакологических препаратов, угнетающих дыхательную цепь, и, естественно, обструктивные нарушения уродинамики и т. д. Весьма важно, что нарушения гипоксического характера в гладкомышечной ткани могут иметь и первичный митохондриальный генез (первичные нарушения энергетического метаболизма детрузора [3].
Необходимо отметить, что у больных ДГПЖ в нижнем отделе мочевого тракта протекают два параллельных процесса — формирование уретральной обструкции и нарушение энергетического метаболизма детрузора (митохондриальная недостаточность).
Подобное представление патогенеза расстройств мочеиспускания открывает широкие возможности для фармакотерапии. Сокращения и расслабления детрузора можно достичь с помощью средств метаболической терапии, прямого улучшения снабжения детрузора кислородом и т. д. Наиболее значимые расстройства основных функций мочевого пузыря все же опосредованы расстройствами кровообращения. И если процесс обратим, то до или после хирургического вмешательства можно существенно влиять на функциональное состояние мочевого пузыря с помощью вазоактивных препаратов, к которым в первую очередь относятся a1-адреноблокаторы.
При определении критериев отбора пациентов для медикаментозной терапии ДГПЖ мы воспользовались рекомендациями IV Международного консультативного комитета по ДГПЖ.
Основу настоящего исследования составили собственные клинические наблюдения за 1724 пациентами (средний возраст 61,4 года), страдающими ДГПЖ и получавшими различные варианты медикаментозного лечения. Нами применялись препараты всех групп, использующихся в настоящее время для лечения ДГПЖ: a-адреноблокаторы, блокаторы 5-a-редуктазы, препараты растительного происхождения и их комбинации. Схемы проведенного лечения и характеристика групп пациентов приведены в табл. 1.
Из наиболее многочисленной и популярной сегодня группы препаратов для медикаментозного лечения ДГПЖ — селективных a-адреноблокаторов мы использовали альфузозин, теразозин, доксазозин и тамсулозин. Общее число пациентов, получавших a-адреноблокаторы, составило 1408. Финастерид был взят нами как классический представитель блокаторов 5-a-редуктазы. Из препаратов растительного происхождения мы использовали пермиксон и таденан.
В пяти группах общей численностью 1305 человек проводилась терапия селективными a-адреноблокаторами в течение длительного периода времени по стандартным схемам и в стандартных дозах. Результаты лечения приведены в табл. 2.
Улучшение качества мочеиспускания отметили в среднем 86,74% пациентов. Суммарный балл I-PSS сократился на 38,68% к окончанию первого года лечения и на 43,4% к окончанию курса терапии. Балл QOL уменьшился на 29,04% и 35,58% соответственно. Максимальная скорость потока мочи увеличилась на 45,25% к окончанию первого года лечения и стабилизировалась на достигнутом уровне. Количество остаточной мочи сократилось в среднем на 57,6%. Процент пациентов, по тем или иным причинам выбывших из исследования, был тождествен во всех группах и равнялся 14,38%.
Особо следует остановиться на препарате тамсулозин (омник, Yamanouchi) — пока единственном простатселективном a1А-адреноблокаторе на отечественном рынке. Этот препарат обладает рядом свойств, которые позволяют его использовать в различных функциональных тестах. Прежде всего это возможность назначения единой терапевтической дозы (один раз в сутки по 0,4 мг). А отсутствие выраженного влияния на артериальное давление и сердечную деятельность избавляет от необходимости титрования дозы. Мы согласны с рядом авторов, которые считают возможным применение коротких курсов терапии тамсулозином в качестве прогностических тестов эффективности лечения a1-адреноблокаторами, что может иметь решающее значение при выборе того или иного метода медикаментозного лечения ДГПЖ [4].
Части больных (группа А5) проведена проверка возможности разрешения острой задержки мочеиспускания (ОЗМ) приемом альфузозина по 5 мг два раза в сутки. Эта терапия проводилась пациентам с впервые возникшей ОЗМ и отсутствием симптомов нарушения мочеиспускания в анамнезе. Положительный эффект был достигнут у 8 из 14 пациентов (57,1%), которым параллельно приему альфузозина производилось кратковременное (трое суток) дренирование мочевого пузыря катетером. Единовременный прием суточной дозы альфузозина (10 мг) способствовал восстановлению самостоятельного мочеиспускания лишь у одного из четырех пациентов, которым проводилась подобная терапия. Вероятно, это объясняется гипотонией детрузора, усугубляющейся в ситуации длительного перерастяжения мочевого пузыря на фоне задержки мочеиспускания.
Для изучения эффективности и безопасности комбинированной медикаментозной терапии ДГПЖ препаратами разных групп, а также для уточнения целесообразности проведения терапии нами были созданы три группы.
В первой группе (К1) пациенты получали проскар по 5 мг/сут. параллельно с приемом теразозина по 5-10 мг/сут. Обращало на себя внимание значительное повышение показателей максимальной скорости потока мочи (+40%), характерное для группы монотерапии a-адреноблокаторами, и постепенное, на протяжении курса лечения, снижение объема предстательной железы (-20,4%), характерное для группы монотерапии финастеридом. Очевидно, что положительные изменения показателей мочеиспускания в этой группе являются следствием воздействия обоих препаратов. Тем не менее процент выбывших пациентов в этой группе был крайне высоким — 32,3%. Основной причиной прекращения комбинированной терапии ДГПЖ пациенты называли неприемлемо высокую стоимость лечения.
В третьей группе комбинированной терапии (К3) лечение проводилось финастеридом по 5 мг/сут. в сочетании с пермиксоном по 160 мг два раза в сутки. Через два года после начала лечения 50% пациентов покинули группу, приводя причиной отказа от дальнейшей терапии высокую стоимость лечения при отсутствии быстрого улучшения качества мочеиспускания. При сравнении полученных данных с результатами в других группах очевидно, что эффективность лечения в третьей существенно ниже.
Таким образом, эффективность медикаментозной терапии больных ДГПЖ при соблюдении показаний и противопоказаний к ее назначению, правильном выборе препарата и схемы его назначения высока и достигает в среднем 80,2%. При этом эффективность монотерапии a-адреноблокаторами составляет 86,7%, блокаторами 5a-редуктазы — 69,4%, препаратами растительного происхождения — 69,3% и при комбинированной терапии — 95,45%. Комбинированная медикаментозная терапия a-адреноблокаторами в сочетании с блокаторами 5a-редуктазы эффективнее монотерапии этими препаратами. С целью снижения стоимости лечения возможен переход на монотерапию блокаторами 5a-редуктазы после достижения выраженного регресса обструктивной симптоматики. Медикаментозная терапия a-адреноблокаторами является эффективным способом консервативного лечения острой задержки мочеиспускания. Терапия должна проводиться на фоне кратковременного (трое суток) дренирования мочевого пузыря уретральным катетером.
Литература
1. Гориловский Л. М. Эпидемиология и факторы риска развития доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 10-18.
2. Лопаткин Н. А., Перепанова Т. С. Клинический опыт лечения больных доброкачественной гиперплазией предстательной железы a1-адреноблокатором альфузозином // Урол. и нефрол., 1997, № 5, с. 14-17.
3. Лоран О. Б., Вишневский Е. Л., Вишневский А. Е. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты a-адреноблокаторами. Монография. М., 1998.
4. Сивков А. В. Медикаментозная терапия доброкачественной гиперплазии предстательной железы. В кн.: Доброкачественная гиперплазия предстательной железы / Под ред. Н. А. Лопаткина. М., 1997, с. 67-83.
5. McConnell J. D. Prostatic growth: new insights into hormonal regulation // Br. J. Urol. 1995. Vol.76.(suppl.1). P. 5-10.
Сравнительная эффективность различных α-адреноблокаторов
Современная терапия гиперплазии предстательной железы является одной из динамично развивающихся фармацевтических дисциплин. Стоит помнить, что долгое время консервативное лечение нарушений мочеиспускания ограничивалось фитотерапией. Механизм действия растительных препаратов заключался в ингибиции ряда ферментов (5α-редуктаза), блокирующем действие на андрогенные рецепторы, сокращении продукции глобулинсвязывающего полового гормона, ингибировании синтеза простагландинов в простате. Во второй половине ХХ в. накопленные знания о роли нарушений симпатической регуляции в патогенезе заболевания привели к внедрению в клиническую практику α-адреноблокаторов. В 1975 г. Марко Кэйн впервые применил на практике неселективный α-адреноблокатор феноксибензамин, и после клинических исследований его терапевтический эффект был подтвержден. При дальнейших исследованиях было выявлено, что α-адреноблокаторы не влияют на размер и рост предстательной железы, а их прием может вызывать побочные эффекты, в основном со стороны сердечно-сосудистой системы. В дальнейшем в простате были выделены α1- и α2-адренорецепторы, а в 1988 г. было доказано, что в регуляции мочеиспускания принимают участие только α1-адренорецепторы. В 1992 г. опубликованы результаты мультицентрового рандомизированного плацебо-контролируемого исследования, показавшие эффективность и безопасность селективного α1-адреноблокатора теразозина. Впоследствии продемонстрирована и доказана безопасность длительного приема альфузозина и доксазозина. Активное изучение данной группы препаратов кардинально изменило подход клиницистов к лечению гиперплазии предстательной железы. Первые публикации и клинические исследования по данной теме в нашей стране принадлежат Ю.А. Пытелю (1988).
В дальнейшем были выделены подтипы α-адренорецепторов: α1A, α1B и α1D. Было доказано, что в шейке мочевого пузыря и простате человека до 70 % всех адренорецепторов относится к α1A-подтипу, они отвечают за регуляцию тонуса гладких мышц этой локализации. α1B-Подтип регулирует артериальное давление через релаксацию гладких мышц артерий, а α1D-подтип связан с сокращением мышц мочевого пузыря. В дальнейшем был синтезирован первый а1A-адреноблокатор тамсулозин, который в сравнении с другими имеющимися на тот момент препаратами оказывал гораздо меньшее системное воздействие и, как следствие, демонстрировал снижение побочных эффектов, связанных с постуральной гипотензией.
Последний препарат из данной группы, силодозин, был зарегистрирован в 2006 г. Он является максимально избирательным по отношению к α1A-адренорецепторам по сравнению с α1B-адренорецепторами (более чем в 100 раз) и α1D-адренорецепторами (более чем в 50 раз). Вследствие этого силодозин давал минимум побочных проявлений со стороны сердечно-сосудистой системы при сохранении схожей эффективности с менее селективными адреноблокаторами. При этом отмечено, что частота побочных эффектов, связанных с нарушениями эякуляции у мужчин, ведущих половую жизнь, у силодозина оказалась выше (28 %), чем у альфузозина (Descazeaud A., 2015).
В настоящее время α-адреноблокаторы являются первой линией терапии для большинства мужчин с гиперплазией предстательной железы и симптомами нижних мочевых путей. При назначении препарата стоит обращать внимание на сопутствующую патологию, возраст больного и стараться назначить препарат с минимальными побочными эффектами. Поскольку средняя продолжительность жизни в России постепенно увеличивается, наблюдается и тенденция к позднему отцовству. И у такой группы больных следует отдавать предпочтение препаратам, максимально сохраняющим эякуляторный компонент копулятивной функции.
Какие группы лекарств эффективны от простатита: полный перечень
Простатит – острый воспалительный процесс в предстательной железе, который устраняется разными группами лекарств. Подбор эффективных препаратов от простатита у мужчин зависит от нескольких факторов – курс лечения подбирает только врач по результатам диагностики.
Группы препаратов от простатита
В зависимости от фазы и стадии заболевания, патогенеза и клинической картины, специалист назначит комплекс лекарств из одной или нескольких групп препаратов:
В дополнение к препаратам назначаются:
Оперативное вмешательство назначается также по показаниям. Подбор препарата, курса лечения и дозировки зависит от причины простатита, степени поражения железы и выраженности симптомов, потому для каждого пациента врач подберет индивидуальную схему.
Антибиотики
Антибактериальные препараты при остром простатите назначаются, когда обнаружена патогенная микрофлора – ее определяют по результатам бакпосева вместе с ее чувствительностью к тем или иным антибиотикам. В числе антибиотиков: Солютаб, Сумамед, Офлоксацин, Ципрофлоксацин, Амоксиклав и др.
Самостоятельный прием антибиотиков угрожает развитием резистентности у бактерий! Принимать антибиотики безопасно только по рекомендации врача, строго в указанной дозировке и не меньше предписанного количества дней.
Адреноблокаторы
Препараты этой группы расслабляют чрезмерно напряженную шейку мочевого пузыря, гладкие мышцы простаты, улучшают дренирование тканей железы. Облегчают симптомы заболевания: задержку мочеиспускания, болезненность при опорожнении мочевого пузыря.
В числе адреноблокаторов: Алфузозин, Артезин, Ницерголин и другие. Форму препарата и его дозировку при необходимости приема определит уролог.
Воспалительный процесс ослабляется негормональными противовоспалительными средствами. Они устраняют болезненные симптомы патологии: отечность, температуру, слабость. Применяются в форме таблеток, свечей, инфузий, инъекций – форму подбирает врач по результатам обследования. К этой группе относятся Диклофенак, Кетопрофен и другие.
Обратите внимание! НПВС способны пагубно влиять на состояние слизистой оболочки желудка и кишечника, имеют ряд побочных эффектов. Не принимайте препараты, если их не назначил врач!
Миорелаксанты
Снимают спазмы мышц, облегчая мочеиспускание и физическую активность. Так как воспаление провоцирует спазмы гладкой мускулатуры близлежащих органов, миорелаксанты используются в рамках симптоматической терапии. К ним относятся Баклофен, Тамсулозин и другие.
Антикоагулянты
Улучают микроциркуляцию крови, предотвращают образование тромбов. Помогают доставлять активные компоненты лекарств к железе за счет улучшенного кровоснабжения. Принимаются строго под наблюдением врача – запишитесь к урологу для получения полной схемы лечения, и только затем приступайте к приему. К группе относятся Кумадин, Синтром, Прадакса и другие.
Растительные препараты при простатите
К недорогим, но эффективным препаратам от простатита относятся растительные биодобавки – они назначаются в рамках комплексной терапии, как вспомогательное средство:
Натуральные препараты содержат антиоксиданты, флаваноиды, которые при неправильном назначении могут ухудшить состояние пациента. Схему лечения назначит уролог после инструментальной и лабораторной диагностики.
Комплексное лечение простатита
Уролог назначает процедуры, медикаменты и физиотерапию по результатам:
Препараты, которые принимают при простатите, действуют комплексно и только в случае, когда назначены в правильной дозировке и длительности приема.
Специалисты клиники Dr. AkNer в Москве более 40 лет занимаются диагностикой и лечением острого, хронического простатита. Обращайтесь, чтоб пройти обследование на современном оборудовании, получить консультацию и лечение от опытных урологов, распрощаться с заболеванием навсегда!
Фокусин : инструкция по применению
Состав
Действующее вещество: tamsulosin;
1 капсула содержит тамсулозина гидрохлорида 0,4 мг
Вспомогательные вещества: метакрилатного сополимера дисперсия, целлюлоза микрокристаллическая, дибутилсебацинат, полисорбат 80, кремния диоксид водный, тальк, азорубин (Е 122), краситель патентованный синий V (Е 131), желатин.
Лекарственная форма
Капсулы твердые с модифицированным высвобождением.
Основные физико-химические свойства: твердые желатиновые капсулы. Тело: темно-синее, прозрачное. Крышка: темно-синяя, прозрачная. Содержимое капсулы: почти белые микропелеты.
Фармакологическая группа
Средства, применяемые при доброкачественной гипертрофии предстательной железы. Антагонисты α 1адренорецепторов.
Фармакологические свойства
Эти эффекты долгое время сохраняются при долгосрочном лечении и в значительной степени сдерживают проведение хирургической операции или катетеризации.
Всасывания: тамсулозин хорошо всасывается из желудочно-кишечного тракта, а его биодоступность составляет почти 100%. Всасывания тамсулозина происходит несколько медленнее после приема пищи. Равномерность всасывания достигается в том случае, когда пациент принимает препарат в одно и то же время после приема пищи. Фармакокинетика тамсулозина имеет линейный характер.
После приема разовой дозы препарата после еды максимальная концентрация тамсулозина в плазме крови достигается через 6:00, а стабильная концентрация образуется на пятые сутки после ежедневного приема препарата. C max при этом приблизительно на две трети выше той, что образуется после приема разовой дозы.
Распределение у мужчин тамсулозин примерно на 99% связывается с белками плазмы крови. Объем распределения препарата незначительный (примерно 0,2 л / кг).
Выведение: тамсулозин и его метаболиты выводятся из организма преимущественно с мочой. Примерно 9% дозы остается в виде неизмененной действующего вещества.
После разового приема препарата после еды и при стабильной концентрации в плазме крови периоды полувыведения составляют примерно 10 и 13 часов.
Показания
Лечение функциональных расстройств со стороны нижних мочевыводящих путей при доброкачественной гиперплазии простаты.