Фототоксичность антибиотиков что это
Синтетические химиотерапевтические антибактериальные ЛС
К синтетическим химиотерапевтическим антибактериальным средствам относятся вещества различной химической структуры. Классифицируют эту группу лекарственных средств по химическому строению на производные: хинолона/фторхинолона; сульфаниламиды; 8-оксихинолина; хиноксалина; нитроимидазола; нитрофурана.
Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета Первого МГМУ им. И.М. Сеченова
В терапевтической практике наиболее широко применяются синтетические химиотерапевтические антибактериальные средства – производные хинолона/ фторхинолона. Все хинолоны/фторхинолоны обладают одинаковым механизмом действия и оказывают бактерицидный эффект. Препараты способны ингибировать жизненно важный фермент микробной клетки – ДНК-гидразу. ДНК-гидраза играет особую роль в суперспирилизации, раскручивание «упакованной» в хромосомы двойной спирали ДНК. В результате образуется комплекс – хинолона с тетрамером гиразы (субъединиц А2В2). Ингибирование фермента предотвращает образование положительных вторичных суперзавитков в отрицательные, не происходит разрыва и сшивания спирали ДНК. ДНК превращается в ковалентную закрытую циркулярную структуру. Нарушается репликация и трансляция ДНК. Клетки теряют способность «считывать» генетическую информацию и размножаться, снижается рост числа микроорганизмов. Некоторые хинолоны способны влиять на РНК бактерий, на стабильность мембран и ингибировать ДНК-топоизомеразу IV типа, разделяющую перекрученные между собой кольцевые молекулы ДНК, образующиеся при репликации. Подавляя активность этого фермента, хинолоны препятствуют разъединению дочерних ДНК. Ферменты микроорганизмов структурно отличаются от ферментов клеток человека. Производные хинолона/фторхинолона не взаимодействуют с клетками макроорганизмов, чем объясняется высокая избирательность их действия и низкая токсичность препаратов данной группы.
Данную группу препаратов принято различать по поколениям:
1-е поколение – нефторированные хинолоны (налидиксовая кислота, пипемидовая кислота, оксолиновая кислота). Производное нафтиридинкарбоновой кислоты – Налидиксовая кислота (Неграм, Невиграмон) – получено в 1962 г. Препараты обладают узким спектром действия, в основном на грамотрицательные бактерии (кишечную палочку, энтеробактерии, клебсиеллы, протей, шигеллы, сальмонеллы). К налидиксовой кислоте устойчива синегнойная палочка, этот препарат практически неактивен против грамположительной и анаэробной микрофлоры. Проявляет активность в отношении возбудителей, устойчивых к некоторым антибиотикам и сульфаниламидам. Позже были получены другие производные: пиридопиримидинкарбоновой кислоты – Пипемидовая кислота (Палин, Пиламин, Пимидель, Пипелин) и диоксолохолинкарбоновой кислоты Оксолиновая кислота (Диоксацин). Препараты всасываются в ЖКТ хорошо и быстро. Не создают терапевтических концентраций в крови, органах и тканях. Налидиксовая и пипемидовая кислоты создают высокие концентрации в моче, при ощелачивании последней активность препаратов возрастает. По антибактериальному спектру действия и применению эти препараты существенно не отличаются друг от друга. Назначают в основном при инфекциях мочевыводящих путей (пиелонефрит, уретрит, цистит), при кишечных инфекциях (энтериты, энтероколиты) и воспалении среднего уха. Пипемидовая кислота проявляет свою активность на некоторые грамположительные микроорганизмы, поэтому может применяться при стафилококковых инфекциях. В этой группе наблюдается перекрестная устойчивость. Могут развиваться побочные эффекты: диспептические явления, аллергические реакции, фототоксичность, головная боль и головокружение, а также тремор и судороги. Налидиксовая кислота выпускается по 0,5 г (тб., капс.). Пипемидовая кислота – по 0,2 и 0,4 г (капс.) и 0,4 г (тб.). Оксолиновая кислота – по 0,25 г (тб.).
Налидиксовая и оксолиновая кислоты противопоказаны детям до 2 лет, Пипемидовая кислота – до 1 года.
Важно! При приеме данных препаратов, особенно при лечении инфекций мочевыводящих путей, необходимо поддерживать интенсивный диурез, поэтому таблетки (капсулы) следует запивать большим количеством воды – не менее двух стаканов, лучше соблюдать суточный водный режим от 1,0 до 2,0 л.
Введение в положение 6 одного или нескольких атомов фтора и различных радикалов в положение 7 хинолинового ядра, позволило не только усилить антибактериальное действие, но и расширить спектр действия, изменить продолжительность развития фармакологических эффектов данной группы препаратов. Впервые наиболее эффективный класс химиопрепаратов «фторхинолоны» появились в 1985 г. Были синтезированы монофторированные, дифторированные и трифторированные вещества, по числу атомов фтора в молекуле.
Первыми были синтезированы вещества с одним атомом фтора. Их отнесли ко 2-му поколению монофторированных – Норфлоксацин (Нолицин) – синтезирован в 1986 г; Пефлоксацин (Абактал), Ципрофлоксацин (Цифран, Ципробай) – в 1987 г; Офлоксацин (Таривид) – в 1991 г.
Впоследствие были созданы препараты: 3-го поколение монофторированных – Левофлоксацин (Таваник) – в 1997 г. и 4-го поколения монофторированных – Моксифлоксацин (Авелокс) и Гатифлоксацин (Гатиспан, Зарквин) – в 1999 г. В 2000 г. создан и внедрен в клиническую практику Гемифлоксацин (Фактив).
Параллельно были синтезированы и внедрены в клиническую практику препараты: 2-го поколения дифторированные – Ломефлоксацин (Максаквин) – в 1992 г. и 3-го поколения дифторированные – Спарфлоксацин (Спарбакт, Спарфло) – в 1997 г.
Синтезированные трифторированные хинолоныТосуфлоксацин и Флероксацин в РФ пока не зарегистрированы.
Существует другая классификация хинолонов/фторхинолонов. В 1-ю группу входят нефторированные хинолоны, узкого спектра действия. 2-я группа включает фторхинолоны, действующие в основном на грамотрицательные микроорганизмы. В 3-ю группу входят так называемые «респираторные» фторхинолоны, наиболее активные в отношении пневмококков и атипичных возбудителей. 4-я группа включает «респираторные» препараты последних поколений и антианаэробные фторхинолоны. Этой классификацией пользуются в основном врачи.
Фармакокинетика фторхинолонов отличается от нефторированных. Все они хорошо всасываются в ЖКТ и создают высокие концентрации в тканях (ЖКТ, легких, почках, мышцах, матке, глазах) и жидкостях организма (синовиальной, воспалительной сыворотке крови, слюне, мокроте). Они легко проникают в макрофаги, нейтрофилы, внутриклеточные концентрации значительно превышают внеклеточные, что учитывается при лечении инфекций с внутриклеточной локализацией микроорганизмов. Концентрация препаратов в тканях организма в 3–7 раз выше, чем в плазме крови. Время сохранения терапевтической концентрации для большинства препаратов 12 ч., а для пролонгированных форм 24 ч. Фторхинолоны долго циркулируют в организме людей, их период полувыведения колеблется от 3 до 5 ч. у ципрофлоксацина, до 20 ч. – у Спарфлоксацина. Фторхинолоны проходят через ГЭБ, плацентарный барьер, проникают в грудное молоко. В организме подвергаются биотрансформации в печени с образованием метаболитов, выводятся почками или экскретируются с фекалиями. Норфлоксацин, Офлоксацин, Ципрофлоксацин и Левофлоксацин мало вступают в реакции метаболизма с участием цитохромов Р450, тогда как Спарфлоксацин и Моксифлоксацин подвергаются биотрансформации с участием ферментов печени.
Фторхинолоны сверхширокого спектра действия охватывают как грамположительную (стрептококки, стафилококки и др.), так и грамотрицательную микрофлору (сальмонеллы, шигеллы, протей, кишечная палочка, гонококки, менингококки). К фторхинолонам чувствительны пневмококки, внутриклеточные микроорганизмы (хламидии, микоплазма), а также быстрорастущие атипичные микобактерии и микобактерии туберкулеза. Мало чувствительны к ним энтерококки и анаэробы.
Ципрофлоксацин (Цифран, Ципробай, Квинтор, Ципролет и др.) – самый эффективный фторхинолон в отношении синегнойной палочки – тб. по 0,25, 0,5 и 0,75 г и 0,2% р-р во фл. 50 и 100 мл; 1% р-р в амп. по 10 мл для разведений.
Офлоксацин (Таривид, Заноцин, Офлоксин) уступает ему, но более активный в отношении пневмококков и хламидий, – тб. 0,2 г; р-р для инфузий 200 мг, в фл. 100 мл. Среди фторхинолонов превосходят по активности в отношении пневмококков Гемифлоксацин > Моксифлоксацин > Левофлоксацин, в т.ч. пенициллинрезистентных штаммов.
Активный левовращающий изомер Офлоксацина – Левофлоксацин в 2 раза активнее офлоксацина по отношению к лекарственно-устойчивым микобактериям и атипичным бактериям (хламидии, микоплазмы). В 3 раза увеличивается активность у Левофлоксацина (Таваник, Элефлокс, тб., покр. обол., по 0,25 и 0,5 г) в отношении чувствительных микобактерий туберкулеза. Моксифлоксацин активен в отношении неспорообразующих анаэробов.
Пефлоксацин (Абактал) выпускается в тб. 0,4 г и амп. по 5 мл 0,4 г.; Ломефлоксацин (Максаквин) – в тб. по 0,4 г; 0,3% глазные капли – в фл. 5 мл.
Важно! Растворы фторхинолонов очень чувствительны к свету, поэтому их готовят перед вливанием, а систему закрывают от прямого солнечного света. Вводить внутривенные растворы необходимо только инстиляционно (капельно) со скоростью 200–250 мг в течение 30 мин.
Широкий спектр антимикробной активности, высокая биодоступность, относительно низкая токсичность и малая резистентность фторхинолонов быстро снискали популярность при лечении различных инфекционных заболеваний. Препараты фторхинолонов показаны при лечении инфекций дыхательных путей, при инфекциях, передающихся половым путем (гонорея, хламидиоз), при хирургических инфекциях, послеоперационных инфекциях, инфекциях желудочно-кишечного тракта, ЛОР–инфекциях, инфекциях кожи, мягких тканей, костей, суставов, раневых, ожоговых. Их широко используют для лечения внебольничных и тяжелых инфекций (сепсис и менингит). Они входят в состав комплексной терапии туберкулеза легких, обширных казеозно-некротических или фиброзо-кавернозных поражений тканей, при выраженном неспецифическом компоненте воспаления, при лекарственной устойчивости микобактерий к рифампицину или плохой переносимости последнего.
Степень снижения нежелательных проявлений со стороны ЖКТ распределяется следующим образом: Спарфлоксацин > Пефлоксацин > Ципрофлоксацин > Левофлоксацин > Норфлоксацин > Офлоксацин. Со стороны ЦНС (головная боль ≈ 3%, нарушение сна ≈ 0,7%, психозы, тремор, судороги ≈ 0,5%). Аллергические реакции (сыпь, зуд, крапивница) – не более 0,5%. Возникает синдром отмены ≈ 3%. Фторхинолоны могут давать редкие побочные эффекты, характерные только для них. Например, нарушение развития хрящевой ткани, разрыв сухожилий или миалгия, отечность суставов, особенно в пожилом возрасте. Фототоксические реакции наблюдаются в 0,5–3% случаев у Ломефлоксацина > Спарфлоксацин > Пефлоксацина > Ципрофлоксацина > Офлоксацин> Левофлоксацин. Фотосенсибилизация может наблюдаться через 3 недели после прекращения лечения. Довольно часто развивается кандидоз слизистой оболочки полости рта или влагалища, что зависит от способа введения препарата в организм. Все нежелательные явления при применении фторхинолонов не относятся к серьезным и легко переносятся больными.
Фторхинолоны противопоказаны беременным, в период лактации; детям до 15–16 лет (до полного формирования скелета), дифторированные и трифторированные препараты – до 18 лет. Несмотря на ограничения применения фторхинолонов в детском возрасте, их назначают по жизненным показаниям при таких заболеваниях, как гнойный менингит, инфекции с муковисцидозом или вызванные полирезистентными штаммами микроорганизмов и др. заболеваниях при отсутствии альтернативных препаратов. Накопленный опыт применения их в педиатрии свидетельствует об их высокой эффективности и хорошей переносимости.
Все препараты хинолонов/фторхинолонов применяются только при назначении врачом. В течение всего курса терапии необходимо строго соблюдать режим дозирования и схему лечения. Длительность лечения определяется чувствительностью возбудителя и клинической картиной. Лечение следует продолжать минимум 3 дня после исчезновения симптомов заболевания, до полной нормализации температуры тела, т.к. клиническое выздоровление больного всегда наступает раньше бактериологического. При длительности лечения фторхинолонами (2 недели), необходимо контролировать анализы крови, функции почек и печени. В период лечения необходимо соблюдать осторожность при вождении автотранспорта или других потенциально опасных видах деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций.
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
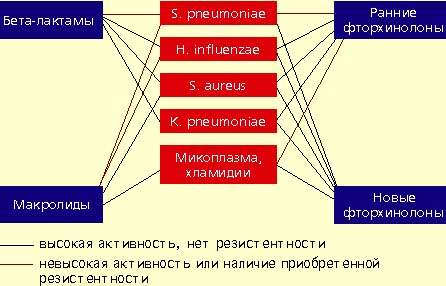 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Как выбрать пробиотики для кишечника: список препаратов
Правильное, сбалансированное содержание белков, жиров и углеводов является ключом к здоровью на долгие годы. Продукты не способны в полной мере обеспечить организм человека всем необходимым. Есть целый перечень лекарств, которые помогают держать себя в хорошей форме и не болеть от легкого дуновения ветра.
Предлагаем список лучших пробиотиков. Перед началом терапии рекомендуется проконсультироваться с врачом, чтобы исключить наличие противопоказаний и правильно рассчитать дозировку.
Полезные свойства
Пробиотики – живые микроорганизмы, которые могут принести пользу человеку. В большинстве случаев это бактерии, но могут быть и другие представители микробов (например, дрожжи). Пробиотики несут пользу для кишечника, нормализуя микрофлору и устраняя дисбактериоз.
Нормы и различные вариации
Пробиотики колонизируют кишечник полезными бактериями, противодействуют патогенной (вредной) флоре, вызывающей запор или диарею, повышают иммунитет.
Основную массу бактерий – пробиотиков можно разделить на 2 вида: лакто- и бифидобактерии. В каждом из них существует значительное количество подвидов. Они оказывают то или иное благотворное влияние на организм человека.
Отклонения от нормы
Чем отличаются пробиотики от пребиотиков?
Могут ли навредить пробиотики?
Пробиотики практически не имеют противопоказания. Не рекомендуется принимать при онкологических заболеваниях, поражении лимфатический и кровеносной системы, ВИЧ. С осторожностью рекомендуется принимать в период беременности и лактации. Маленьким детям допустимо давать только те препараты, которые не имеют возрастных ограничений.
Как выбрать пробиотики для кишечника?
Лучшие пробиотики для восстановления кишечника может посоветовать только врач. Должны быть учтены основные критерии: возраст пациента, состояние организма, характер дисфункций, противопоказания и пр. Самолечение может не дать должного результата и привести к развитию проблем со здоровьем.
В список препаратов включены лучшие пробиотики для восстановления микрофлоры кишечника. Рейтинг основан на эффективности, безопасности и соотношении цена-качество.
№1 – «Нормофлорин-Д» (Бифилюкс, Россия)
Биологически активная добавка разработана на основе лактобактерий и их метаболитов. Используется в комплексном лечении язвы двенадцатиперстной кишки и желудка, при ожирении и метаболическом синдроме. Назначается после антибактериальной терапии для восстановления нарушенного микробиоценоза.
Производитель: Бифилюкс, Россия
№2 – «Бифиформ» (Ferrosan, Дания)
Противодиарейный препарат регулирует равновесие микрофлоры кишечника. Содержит Bifidobacterium longum и Enterococcus faecium. МИБП-эубиотик назначается при непереносимости лактозы, для восстановления микрофлоры кишечника и для лечения хеликобактерной инфекции в составе комплексной терапии.
Производитель: Ferrosan [Ферросан], Дания
№3 – «Линекс» (Lek d. d., Словения)
Находится в первых рядах списка пробиотиков для кишечника. Основные активные компоненты этого препарата стимулируют изменение рН путем брожения лактозы. Это тормозит развитие патогенных и условно-патогенных микроорганизмов и создает благоприятные условия для пищеварительных ферментов.
Активные вещества, входящие в «Линекс» устойчивы к антибиотикам. Они оказывают влияние не только на нижние отделы кишечника, но и на верхние (этими свойствами обладают далеко не все пробиотики). Многокомпонентное средство, пригодно практически для всех пациентов, включая детей (даже тех, кто находится на искусственном питании).
Производитель: Lek d. d. [Лек д.д.], Словения
№4 – «Хилак Форте» (Merckle, Германия)
Комбинированный препарат для нормализации кислотности желудка в соответствии с физиологической нормой. Биологически восстанавливает микрофлору кишечника. Таким образом, создает неблагоприятную среду для жизнедеятельности патогенных и условно-патогенных бактерий.
Производитель: Merckle [Меркле], Германия
№5 – «Линекс Форте» (Sandoz, Словения)
Пробиотик регулирует равновесие микрофлоры кишечника. Разработан на основе молочнокислых живых бактерий, которые представляют собой составляющие естественной микрофлору. Широко используется при дисбактериоза, запорах и хеликобактериозе у детей и взрослых.
Производитель: Sandoz [Сандоз], Словения
№6 – «Бифидумбактерин» (Ланафарм, Россия)
Лучший пробиотик для восстановления микрофлоры, который устойчив ко многим лекарственным средствам и антибиотикам. «Бифидумбактерин» является антагонистом достаточно широкого спектра болезнетворных и условно болезнетворных микроорганизмов. Выпускается в форме ректальных суппозиториев и капсул.
Эффективность препарата обусловлена сильной концентрацией бифидобактерий. Быстро нормализует микрофлору кишечника, которая, будучи естественной, накапливает токсические вещества (как поступающие в организм извне, так и находящиеся в нем) и разлагает их на нетоксичные компоненты. Нельзя давать детям, страдающим непереносимостью молочных продуктов.
Производитель: Ланафарм, Россия
№7 – «Бак-Сет Форте» (Probiotics International, Великобритания)
Мульти-пробиотик нового поколения, который включает в состав 14 видов пробиотических живых бактерий. Они дополняют действие друг друга, устраняя проблемы с пищеварением у детей от 3-х летнего возраста и у взрослых. Усовершенствованная микрокапсулированная технология способствует сохранению полезных свойств бактерий на протяжении всего срока хранения препарата.
Производитель: Probiotics International [Пробиотикс Интернейшенал], Великобритания
№8 – «Бифиформ Баланс» (Pfizer, Россия)
Один из лучших пробиотиков для восстановления микрофлоры кишечника. разработан на основе лакто- и бифидобактерий. Биологически активная добавка к пище назначается для лечения дисбактериоза различной этиологии и поддерживает микрофлору кишечника. Способствует коррекции функциональных нарушений желудочно-кишечного тракта.
Производитель: Pfizer [Пфайзер], Россия
№9 – «Флорин Форте» (Партнер, Россия)
Лакто- и бифидобактерии, входящие в состав, принимают участие в процессах синтеза аскорбиновой кислоты, калия, витаминов группы В. В результате повышается устойчивость к агрессивным воздействиям окружающей среды. Также действующие компоненты участвуют в обменных процессах желчных кислот и пигментов. В их присутствии происходит синтез веществ, оказывающих антибактериальное действие. Также препарат повышает иммунную-реактивность человеческого организма.
Производитель: Партнер, Россия
№10 – «Бактериофаг» (Микроген НПО, Россия)
Стафилококковый раствор входит в список лучших пробиотиков для кишечника для взрослых и детей. Используется преимущественно в составе комплексной терапии с антибактериальными препаратами и другими лекарственными средствами.
Производитель: Микроген НПО, Россия
№11 – «Секстафаг» (Микроген НПО, Россия)
Завершает список препаратов пробиотиков для кишечника. Иммунобиологический препарат специфически лизирует бактерии стрептококков и стафилококков, протеи, кишечной и синегнойной палочки. Назначается при энтеральных и гнойно-воспалительных заболеваниях. При необходимости может быть использован в составе комплексной терапии.
Производитель: Микроген НПО, Россия
Пробиотические средства нормализуют процессы пищеварения, активируя перистальтику кишечника и восстанавливая микрофлору. Препараты способствуют синтезу полиаминов, укрепляют клеточный цитоскелет и регенерируют кишечный эпителий, повышая защитные функции организма. Они не только уменьшают газообразование, н и тормозят рост вредоносных микроорганизмов.
Какие пробиотики принимать в том или ином случае может посоветовать врач. Специалист отталкивается от показаний и общего состояния организма пациента, исключая развитие передозировки или побочных реакций.















