Тимико лимфатический статус у детей что это
Статус тимико-лимфатический
Оглавление
Статус тимико-лимфатический
Статус тимико-лимфатический (status thymicolymphaticus синонимы: тимико-лимфатическое состояние, тимико-лимфатическая конституция) — врождённая конституциональная особенность организма (конституциональный тип), проявляющаяся чрезмерным развитием подкожной клетчатки, пастозностью, бледностью кожи, гиперплазией лимфоидных органов (небных миндалин, лимфатических узлов, селезенки), увеличением вилочковой железы, гипоплазией сердечно-сосудистой системы и надпочечников. Обратное развитие вилочковой железы мало выражено и происходит позднее обычного.
Хотя причина внезапной смерти Статус тимико-лимфатический до сих пор окончательно не выяснена, в настоящий, время существует мнение, что она связана с дисфункцией коры надпочечников (смотри полный свод знаний) и нарушениями взаимосвязей эндокринных желёз. Такое объяснение находит все больше сторонников.
Функция вилочковой железы находится в коррелятивной связи с функциями других желёз внутренней секреции, в том числе надпочечников, оказывая на них тормозящее влияние. Проведенные Е. А. Домбровской в 1965 год исследования деятельности надпочечников при Статус тимико-лимфатический позволили доказать их функциональную несостоятельность — значительное обеднение коры надпочечников липидами, кетостероидами, холестерином.
Таким образом, причиной Статус тимико-лимфатический считают недостаточную секрецию глюкокортикоидов корой надпочечников, а основной причиной внезапной смерти при этом состоянии — острую адренокортикальную недостаточность. Однако механизм развития этого состояния остаётся неясным.
Для лиц со Статус тимико-лимфатический характерны, как указывалось, пастозность, бледность и некоторая истончённость кожи, рыхлость подкожной клетчатки, гидролабильность и склонность к увеличению веса, связанные с нарушением водносолевого обмена, мышечная гипотония с некоторым увеличением массы мышц, гипоплазия сердечно-сосудистой системы (узкая аорта, «капельное» сердце). Дети адинамичны, реакция у них замедлена, сухожильные рефлексы понижены; характерны лабильность нервной системы, писклявый голос, продолжительный звонкий плач. У таких детей возможны частая рвота, стридорозное дыхание (смотри полный свод знаний: Стридор), апноэ (смотри полный свод знаний: Дыхание), цианоз носогубного треугольника (в покое и во время сна), проявления сердечно-сосудистой недостаточности. Отмечается недоразвитие наружных и внутренних половых органов, изменения скелета (например, длина конечностей больше длины туловища). Ослабление защитных сил организма при Статус тимико-лимфатический является одной из причин снижения сопротивляемости организма к вирусным и бактериальным инфекциям и склонности его к аллергическим реакциям. Дети предрасположены к ангине, риниту, трахеиту, конъюнктивиту, дерматозам. У детей с увеличенной вилочковой железой нередко (на первом году жизни) возникают пневмонии с рецидивирующим течением.
Диагноз Статус тимико-лимфатический ставят на основании клинические картины, анамнестических данных (неблагоприятно протекавшая беременность у матери, крупный вес ребёнка при рождении), а также особенностей периода новорожденности (например, тяжело протекающая пневмония, частые острые респираторные заболевания).
Для определения размеров вилочковой железы проводят её рентгенологическое исследование в прямой и боковой проекции. Для оценки функционального состояния вилочковой железы при её увеличении используют показатели состояния иммунной системы организма (смотри полный свод знаний: Иммунологическая недостаточность, Иммуноморфология), а также определяют уровень гормонов в организме. При этом характерны высокий уровень соматотропного гормона и резкое снижение содержания АКТГ, кортизола и его метаболитов.
Дифференциальный диагноз проводят с новообразованиями и кистами, исходящими из вилочковой железы (смотри полный свод знаний) и средостения (смотри полный свод знаний).
Лечение сводится к назначению диеты с ограничением липидов; особенно полезны молоко, картофель, бобы. Переедание не допускается во избежание развития ожирения.
Тимомегалия (увеличение вилочковой железы) должна рассматриваться как неблагоприятный фон при острых инфекционные болезнях, при оперативных вмешательствах, при проведении профилактических прививок. В этих случаях показано назначение димедрола, пипольфена, глюкокортикоидов (гидрокортизон, преднизолон), а также препаратов, стимулирующих иммунологический реактивность организма (апилак, пентоксил, элеутерококк, дибазол).
Своевременное выявление тимомегалии и определение у ребёнка Статус тимико-лимфатический позволяет выделять таких детей в группу риска по иммуно-дефицитному состоянию, развитию острой и хронической надпочечниковой недостаточности, по склонности к аллергическим реакциям и тяжелому течению острых инфекционные болезней, пневмоний. Для обеспечения нормального развития ребёнка с тимомегалией и предотвращения внезапной смерти следует особенно оберегать его от острых инфекционные болезней в течение первых 3 лет жизни. Необходимо отсрочить профилактические прививки; если это невозможно, их следует проводить на фоне гипосенсибилизирующей терапии (димедрол, супрастин и другие) для предупреждения осложнений, /ети с тимомегалией должны находиться на обязательном диспансерном учете. В течение первых 3 лет жизни раз в год им производят рентгенографию грудной клетки в прямой и боковой проекциях. Таких детей не рекомендуется направлять в ясли.
Смотри полный свод знаний: Вилочковая железа.
STATUS THYMICOLYMPHATICUS
STATUS THYMICOLYMPHATICUS (син.: тимико-лимфатическое состояние, тимико-лимфатическая конституция) — врожденная конституциональная особенность организма (конституциональный тип), проявляющаяся чрезмерным развитием подкожной клетчатки, пастозностью, бледностью кожи, гиперплазией лимфоидных органов (небных миндалин, лимфатических узлов, селезенки), увеличением вилочковой железы, гипоплазией сердечно-сосудистой системы и надпочечников. Обратное развитие вилоч-ковой железы мало выражено и происходит позднее обычного.
Хотя причина внезапной смерти npuS. t. до сих пор окончательно не выяснена, в наст, время существует мнение, что она связана с дисфункцией коры надпочечников (см.) и нарушениями взаимосвязей эндокринных желез. Такое объяснение находит все больше сторонников.
Функция вилочковой железы находится в коррелятивной связи с функциями других желез внутренней секреции, в том числе надпочечников, оказывая на них тормозящее влияние. Проведенные Е. А. Домбровской в 1965 г. исследования деятельности надпочечников при S. t. позволили доказать их функциональную несостоятельность — значительное обеднение коры надпочечников липидами, кето-стероидами, холестерином.
Т. о., причиной S. t. считают недостаточную секрецию глюкокорти-коидов корой надпочечников, а основной причиной внезапной смерти при этом состоянии — острую адре-нокортикальную недостаточность. Однако механизм развития этого состояния остается неясным.
Для лиц со S. t. характерны, как указывалось, пастозность, бледность и нек-рая истонченность кожи, рыхлость подкожной клетчатки, гидролабильность и склонность к увеличению веса, связанные с нарушением водно-солевого обмена, мышечная гипотония с нек-рым увеличением массы мышц, гипоплазия сердечно-сосудистой системы (узкая аорта, «капельное» сердце). Дети адинамичны, реакция у них замедлена, сухожильные рефлексы понижены; характерны лабильность нервной системы, писклявый голос, продолжительный звонкий плач. У таких детей возможны частая рвота, стридорозное дыхание (см. Стридор), апноэ (см. Дыхание), цианоз носогубного треугольника (в покое и во время сна), проявления сердечно-сосудистой недостаточности. Отмечается недоразвитие наружных и внутренних половых органов, изменения скелета (напр., длина конечностей больше длины туловища). Ослабление защитных сил организма при S. t. является одной из причин снижения сопротивляемости организма к вирусным и бактериальным инфекциям и склонности его к аллергическим реакциям. Дети предрасположены к ангине, риниту,трахеиту, конъюнктивиту, дерматозам. У детей с увеличенной вилочковой железой нередко (на первом году жизни) возникают пневмонии с рецидивирующим течением.
Диагноз S. t. ставят на основании клин. картины, анамнестических данных (неблагоприятно протекавшая беременность у матери, крупный вес ребенка при рождении), а также особенностей периода новорожденное™ (напр., тяжело протекающая пневмония, частые острые респираторные заболевания).
Для определения размеров вилочковой железы проводят ее рентгенол. исследование в прямой и боковой проекции. Для оценки функционального состояния вилочковой железы при ее увеличении используют показатели состояния иммунной системы организма (см. И ммунологи-ческая недостаточность, Иммуномор-фология), а также определяют уровень гормонов в организме. При этом характерны высокий уровень сома-тотропного гормона и резкое снижение содержания АКТГ, кортизола и его метаболитов.
Дифференциальный диагноз проводят с новообразованиями и кистами, исходящими из вилочковой железы (см.) и средостения (см.).
Лечение сводится к назначению диеты с ограничением липидов; особенно полезны молоко, картофель, бобы. Переедание не допускается во избежание развития ожирения.
Тимомегалия (увеличение вилочковой железы) должна рассматриваться как неблагоприятный фон при острых инф. болезнях, при оперативных вмешательствах, при проведении профилактических прививок. В этих случаях показано назначение димедрола, пипольфена, глюкокортикоидов (гидрокортизон, преднизолон), а также препаратов, стимулирующих иммунол. реактивность организма (апилак, пентоксил, элеутерококк, дибазол).
Своевременное выявление тимо-мегалии и определение у ребенка S. t. позволяет выделять таких детей в группу риска по иммуноде-фицитному состоянию, развитию острой и хронической надпочечниковой недостаточности, по склонности к аллергическим реакциям и тяжелому течению острых инф. болезней, пневмоний. Для обеспечения нормального развития ребенка с тимомегалией и предотвращения внезапной смерти следует особенно оберегать его от острых инф. болезней в течение первых 3 лет жизни. Необходимо отсрочить профилактические прививки; если это невозможно, их следует проводить на фоне гипосенсибилизирующей терапии (димедрол, супрастин и др.) для предупреждения осложнений. Дети с тимомегалией должны находиться на обязательном диспансерном учете. В течение первых 3 лет жизни раз в год им производят рентгенографию грудной клетки в прямой и боковой проекциях. Таких детей не рекомендуется направлять в ясли.
С. А. Жданова, В. А. Таболин.
Тимус – что это? Роль тимуса на первому году жизни ребенка
Консультацию педиатра и аллерголога-иммунолога
Тимус (вилочковая железа) – важный орган иммунной системы детей. Он расположен в верхнем отделе грудной клетки и состоит из двух долей, соединяющихся в передней части трахеи. Железа растет до наступления половой зрелости, достигая массы 30–40 грамм, затем постепенно уменьшается (обратное развитие).
Она играет доминирующую роль в иммунной, эндокринной системе. Тимус продуцирует тимозин, тимопоэтин, стимулирующие выработку антител, а также производит Т-лимфоциты – белые клетки крови, уничтожающие аномальные клетки с чужеродными антигенами. Другая функция вилочковой железы – предотвращение патологического роста клеток и предупреждение рака. Следует отметить, что тимус играет ведущую роль в иммунитете ребенка до трех лет.
Роль тимуса в жизни ребёнка
До рождения и в детстве тимус ответственен за производство плюс созревание Т-лимфоцитов, защищающих организм от определенных угроз, включая вирусы, бактерии. Тимус является крупнейшим лимфоидным органом у новорожденных, так как активнее других тканей продуцирует лимфоциты. Железа выступает «первой скрипкой» в развитии и улучшении иммунной системы ребенка.
Тимус производит и секретирует тимозин – гормон, необходимый для выработки Т-клеток. После «созревания» в железе они поступают в кровь и мигрируют в лимфоузлы и селезенку, где помогают иммунной системе бороться с болезнью.
В некоторых случаях функции вилочковой железы снижены, что ослабляет иммунную систему, увеличивая склонность к инфекциям и аллергии. Ребенок страдает затяжными ОРВИ, патология легко переходит в хроническую. Недостаток Т-лимфоцитов в организме может привести к иммунодефицитным заболеваниям, характеризующимися сильной потливостью, отечностью и/или болезненностью горла, припухлостью лимфатических узлов, депрессией.
Недоедание и дефицит белка в раннем возрасте обусловливает медленный или ограниченный рост тимуса, «подрывая» тем самым нормальное функционирование лимфоцитов. Вот почему важно сбалансированное питание с достаточным количеством белка.
Доктора данного направления
Патология тимуса
Основные виды патологии тимуса:
Увеличение тимуса у детей
Отклонение в размере тимуса в большую сторону и снижение его функции обозначают термином «синдром увеличенной вилочковой железы» (СУВЖ) у детей. Проблему увеличенного тимуса чаще рассматривают в свете дифференциальной диагностики с плевритом, перикардитом, опухолями средостения, другими патологиями.
Ошибочно считают, что увеличенный тимус у детей грудного или раннего возраста является физиологическим состоянием. Особенности протекания инфекционных заболеваний у маленьких пациентов с СУВЖ заставляют классифицировать синдром, как патологию. Дети с СУВЖ имеют большую вероятность развития дисбаланса нейроэндокринной плюс иммунной систем. Поэтому пациенты с выявленным увеличением тимуса требуют полного обследования и диспансерного наблюдения у эндокринолога, иммунолога.
Симптомы заболевания или нарушения развития вилочкой железы
Для того, что бы вовремя выявить патологию тимуса, родителям стоит обратить внимание на отклонения, имеющие различную степень выраженности, которые могут свидетельствовать о заболевании или нарушении развития вилочковой железы:
При возникновении подозрений на патологию тимуса, врач может назначить дополнительные методы обследования:
Тимическая недостаточность поддается иммунокорекции, которая индивидуально подбирается врачом аллергологом-иммунологом. Стоит обратить внимание, что своевременная диагностика патологии вилочковой железы особенно актуальна на первом году жизни ребенка, когда ребенку начинают проводить вакцинацию.
Для получения подробных консультаций о роли тимуса в жизни ребёнка на первом году жизни обращайтесь к педиатрам медицинских центров «Президент-Мед»
ТИМОМЕГАЛИЯ И СИНДРОМ ПЛАТТЕРА
История относительно интенсивного изучения вилочковой железы ( glandula thymus, thymus ) насчитывает около 400 лет. Начало его относится к 1614 г., когда профессор Базельского университета Феликс Платтер описал происшедшую у него
В середине XIX в. профессор Венского университета Карл Рокитанский высказал предположение об инкреторной функции вилочковой железы. Данная концепция была положена в основу представлений о тимико-лимфатическом статусе [1, 2] как врожденной особенности конституции, предрасполагающей к внезапной смерти от незначительных причин. В симптомокомплекс тимико-лимфатического статуса включались первичная гиперфункция вилочковой железы, гипоплазия надпочечников, сердца и аорты [1–5]. С этого времени причиной тимической смерти стали считать острую надпочечниковую недостаточность [3, 4]. Однако отсутствие характерных для тимико-лимфатического состояния признаков во многих случаях при такой смерти, в том числе и симптомов надпочечниковой недостаточности, позволило поставить под сомнение и данную концепцию.
В начале 1960-х гг. было доказано, что тимус является центральным органом иммунной системы. С этого времени вилочковая железа рассматривается в качестве железы внутренней секреции, действие гормонов которой направлено на дифференцировку тимических лимфоцитов. Открытие основной функции вилочковой железы — продукции Т-лимфоцитов и регуляции иммунитета, а также принадлежность ее к системе эндокринных желез позволяют рассматривать данный орган как коммутатор иммунной и эндокринной систем. В серии работ отечественных исследователей последних 20 лет доказывается, что дети с большой вилочковой железой относятся к числу иммунодефицитных лиц.
В 1970 г. проф. Т. Е. Ивановской [6] для обозначения увеличенной вилочковой железы вместо вышеуказанных терминов был предложен термин «тимомегалия». Под тимомегалией российские морфологи понимают увеличение объема и массы тимуса выше предельных возрастных значений с сохранением нормальной гистоархитектоники органа. Начиная с 1970 г., этот термин стал широко использоваться как морфологами, так и клиницистами.
Однако проведенные исследования показали, что тимомегалия является лишь одним из симптомов того состояния, которое существует у детей, имеющих увеличенную вилочковую железу [7]. В связи с отсутствием другого термина, отражающего сущность состояния, которое имеет место у детей с увеличенной вилочковой железой (соответствующей тимомегалии в понимании патологоанатомов), предлагаем называть его синдромом Платтера.
Термином «синдром Платтера» следует обозначать состояние, при котором клинические и параклинические методы обследования позволяют выявить у детей и подростков ряд специфических изменений организма, сочетающихся с первичной длительно сохраняющейся тимомегалией. Клиническое понимание тимомегалии при синдроме Платтера отражает морфологическое состояние вилочковой железы, при котором масса и объем тимуса превышают предельные возрастные значения при сохранении нормальной гистоархитектоники органа.
Диагностика тимомегалии в клинической практике
Ориентировочная диагностика тимомегалии может быть проведена с помощью объективного исследования: осмотра, пальпации, перкуссии. Однако оценка результатов во многом субъективна и зависит от опыта исследователя [7].
Из инструментальных методов, позволяющих объективно выявить тимомегалию, используются рентгенодиагностика и ультразвуковое исследование (УЗИ).
Рентгенодиагностика. Методологической основой рентгенодиагностики увеличенного тимуса является следующее положение: в норме у детей любого возраста на стандартных рентгенограммах грудной клетки в прямой проекции тень тимуса не должна выходить за пределы тени сосудистого пучка и сердца.
В целях диагностики тимомегалии на рентгенограммах грудной клетки в прямой проекции мы применяли кардио-тимико-торакальный индекс (КТТИ) по J. Gewolb [8] и вазокардиальный индекс (ВКИ) [7]. Оба индекса определяются на стандартных рентгенограммах грудной клетки в прямой проекции. КТТИ представляет собой частное от деления ширины сосудистого пучка на уровне бифуркации трахеи (точка carina) на ширину грудной клетки на уровне купола диафрагмы. ВКИ представляет собой частное от деления ширины сосудистого пучка на уровне бифуркации трахеи (точка carina) на максимальную ширину тени сердца. Максимальная ширина тени сердца определяется как сумма двух перпендикулярных отрезков, опущенных на вертикальную линию (проведенную через середину позвоночного столба) из максимально удаленных от нее точек сердца слева и справа (рис. 1).
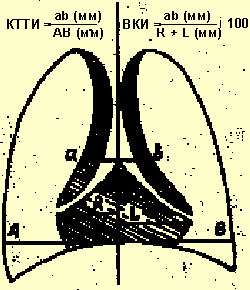 |
| Рисунок 1. Схема вычисления индексов КТТИ и ВКИ |
Выявление в средостении характерной овальной, треугольной или лентовидной тени с прямым, волнообразным или неровным контуром, расположенной с одной или обеих сторон сосудистого пучка, искажающей линию «сердечной талии» слева и/или вазокардиальный угол справа, позволяет сделать заключение о существовании у пациента тимомегалии. Наличие увеличенных значений КТТИ и ВКИ подтверждает данный диагноз. Рентгенологический метод, однако, информативен только для детей грудного и раннего возраста, поскольку у детей в возрасте старше 3 лет, как правило, тимус располагается за тенью сосудистого пучка и сердца. В таблице 1 приведены значения КТТИ и ВКИ у детей первых 3 лет жизни при разных степенях увеличения тимуса.
УЗИ. УЗИ тимуса в нашей стране впервые было проведено у новорожденных детей С. М. Воеводиным [9]. Путем клинико-морфологических сопоставлений нами были разработаны коэффициенты пересчета линейных параметров тимуса в более привычные для клиницистов формы (объема и массы органа). Округленные величины указанных коэффициентов, по нашим данным, равны 0,7 (для массы) и 0,5 (для объема). Таким образом, величины массы и объема тимуса при ультразвуковом сканировании вычисляются следующим образом:
М = 0,7 в a в b в c;
V = 0,5 в a в b в c,
где a, b, c — линейные параметры тимуса (ширина, длина, передне-задний размер, выраженные в см); 0,7 и 0,5 коэффициенты пересчета линейных параметров на массу и объем органа соответственно [10]. Для практических целей массу и объем вилочковой железы достаточно определять так, как это указано выше: без вычисления объема и массы отдельных долей.
Методом центильного распределения нами были определены нормальные значения массы и объема тимуса для детей в возрасте 1–24 мес (табл. 2). При превышении массы и объема тимуса выше верхних предельных значений нормы состояние ребенка следует расценивать как тимомегалию.
На основании анализа более 5000 рентгенограмм, выполненных у детей грудного возраста при подозрении на пневмонию, диагноз которой рентгенологически не был подтвержден, тимомегалия нами была выявлена у 35% пациентов 1 — 3 мес, у 15% детей в возрасте 3–6 мес, у 8% — в возрасте 7–15 мес, у 2% — в возрасте 16 — 36 мес, а в популяции детей старше 3 лет частота выявления тимомегалии не превышала 0,5% [8].
Наблюдение за одними и теми же детьми на протяжении длительного отрезка времени позволило нам сделать вывод, что тимомегалия в детском возрасте может быть как транзиторной, так и стойкой.
В 1993 г. нами совместно с О. В. Зайратьянцем была предложена классификация тимомегалии в детском возрасте на основе клинико-морфологических данных. Несколько измененный вариант указанной классификации приведен в табл. 3 (см. рубрику «Под стекло»). Наиболее частым вариантом тимомегалии в детском возрасте является синдром Платтера.
Анализ родословных позволил выявить у родственников первой и второй линии родства детей с синдромом Платтера высокую частоту встречаемости злокачественных новообразований, аутоиммунных заболеваний и заболеваний системы эндокринных органов. Так, злокачественные новообразования встречаются в каждой третьей семье, где есть дети с синдромом Платтера, с такой же частотой в этих семьях регистрируются эндокринные заболевания (преимущественно сахарный диабет и заболевания щитовидной железы). В семьях детей с синдромом Платтера статистически чаще, чем в семьях детей из выборки общей популяции, распространены аутоиммунные заболевания (диффузные болезни соединительной ткани) и туберкулез. Помимо этого, многие родители детей с указанным синдромом в дошкольном и младшем школьном возрасте относились к группе часто болеющих, т. е. к группе детей имевших повышенную склонность к острым респираторным вирусным инфекциям (ОРВИ).
Характер перечисленных заболеваний (склонность к вирусным, аутоиммунным, онкологическим заболеваниям, туберкулезу) может указывать на существование у близких родственников детей с синдромом Платтера недостаточной активности клеточного звена иммунной системы, поскольку, согласно современным воззрениям, все перечисленные заболевания находятся под контролем Т-клеточного иммунитета, формируемого вилочковой железой. При этом не совсем ясно, чем объясняется высокая отягощенность родственников детей с синдромом Платтера болезнями системы эндокринных органов. Однако не следует забывать о том, что эндокринные заболевания (в том числе сахарный диабет, диффузный токсический зоб, гипотиреоз) могут иметь аутоиммунный генез.
В таком случае у близких родственников детей с синдромом Платтера отчетливо просматривается тенденция к заболеваниям, связанным с иммунными механизмами клеточного типа, контролирующимися вилочковой железой. Это позволяет предполагать возможность передачи детям, у которых развился синдром Платтера, какого-то дефекта Т-звена иммунной системы.
Антенатальный период у большинства детей с синдромом Платтера осложняется хронической гипоксией, обусловленной острыми инфекционными заболеваниями или обострением хронических экстрагенитальных заболеваний матерей, наличием у них сосудистой дистонии, анемии, гестозов.
Осложненное течение интранатального периода отмечается не менее чем у 2/3 детей с синдромом Платтера. Наиболее частыми осложнениями этого периода явились стремительные или затяжные роды, приведшие к наложению щипцов или экстренному кесареву сечению.
Группа детей с указанным синдромом по фенотипу гетерогенна. 90% детей имеют мягкие округлые формы тела, некоторую пастозность тканей, относительно крупные черты уплощенного лица, прямой тип лба, широкоовальные глаза, относительно короткий нос с низким переносьем, средней величины или толстые губы, слабый изгиб профиля, короткую шею. Дети этой группы имеют как бы увеличенные поперечные размеры тела: широкое лицо, широкая грудная клетка, широкие плечи, широкие ладони и стопы, относительно короткие и широкие пальцы. Около 3/4 детей-европеоидов этой подгруппы имеют нежную, но несколько утолщенную, слабопигментированную белую кожу, для которой характерно быстрое развитие ожога после инсоляции, светлую окраску волос и глаз, слабое развитие мускулатуры, сниженную физическую активность. Дети данной подгруппы отличаются хорошим (и даже избыточным) аппетитом и высокими темпами роста.
В дошкольном и младшем школьном возрасте у них отмечаются хорошее развитие подкожного жирового слоя, слабое развитие мускулатуры, снижение общего тонуса и тургора тканей, а также физической активности, замедленная реакция на внешние раздражители, замедленное образование новых условных рефлексов, ослабление процессов внутреннего торможения с преобладанием реакций внешнего торможения.
Клиническая характеристика детей с синдромом Платтера включает характеристику системы лимфоидных органов, которая, согласно мнению большинства исследователей, отличается генерализованной гиперплазией системы лимфоидных органов: лимфатических узлов, лимфатических фолликулов корня языка, задней поверхности глотки, поверхности надгортанника, гипертрофией небных и глоточной миндалин. Наши наблюдения, однако, показали, что состояние периферических лимфоидных органов зависит от воздействия антигенного стимула — при отсутствии такого воздействия генерализованная гиперплазия периферического лимфоидного аппарата не развивается [7].
К числу особенностей физического развития детей грудного и раннего возраста относятся: высокие темпы увеличения длины тела, слабое развитие скелетной мускулатуры, несвоевременность и неправильный порядок прорезывания молочных зубов, относительно позднее начало самостоятельной ходьбы.
В эмоциональной сфере в первые 2–3 мес жизни обращает внимание менее выраженный комплекс оживления (за счет снижения двигательной активности).
Начало становления речи у детей с синдромом Платтера не отличалось от такового у детей соответствующего возраста в популяции в целом: гуление, слоги и первые слова у них появлялись своевременно.
К возрасту 10–11 мес они начинали произносить первые одно- и двусложные слова, к 1 году количество активно произносимых слов достигало 10–12. В дальнейшем 8% детей данной группы до 2-летнего возраста продолжали пользоваться только этими 10–12 словами. В возрасте 4,5–6 лет 25% детей этой группы страдали дислалией, требующей проведения корригирующих логопедических занятий в условиях детской поликлиники или в условиях специализированного детского сада. У отдельных пациентов нарушение, связанное с произношением звуков, сохранялось и в подростковом возрасте.
Состояние здоровья детей с синдромом Платтера. Здесь рассматриваются только те заболевания и патологические состояния, которые достоверно чаще встречались у детей с указанным синдромом, по сравнению с детьми из общей популяции. При анализе структуры выявленных заболеваний наибольшую по численности группу составили аномалии развития (выявлены у 80% наблюдавшихся пациентов) — пороки развития, множественные стигмы дизэмбриогенеза, биохимические дефекты. Пороки развития чаще проявлялись гипоплазией органов и тканей: широкие отверстия паховых каналов и пупочного кольца, септальные дефекты в сердце, гипоплазия аорты, сердца, легких, почек, щитовидной железы и др.
Вторая группа заболеваний была представлена патологическими состояниями нервной системы. Наряду с заболеваниями нервной системы, обусловленными биохимическими дефектами (синдром Менкеса; ганглиозидоз Gm1; фенилкетонурия; галактоземия), обращали на себя внимание такие синдромы, как гипертензионно-гидроцефальный (у 49%), фебрильных судорог (у 20%), мышечной гипотонии (у 18%) и вегетативно-висцеральной дисфункции (у 12,5%). Включение в комплекс обследования электрофизиологических методов, компьютерной и ядерно-магнитно-резонансной томографии привело к существенному увеличению частоты выявления гипертензионно-гидроцефального синдрома (выявлен у 90%). Указанный синдром у 2/3 детей сочетался с синдромами фебрильных судорог и вегетативно-висцеральных дисфункций, однако последние два синдрома у части детей встречались и изолированно.
Изолированный синдром вегетативно-висцеральных дисфункций характеризовался крайне выраженным полиморфизмом проявлений: нарушение терморегуляции, дыхания, сердечной деятельности, функции желудочно-кишечного тракта, пароксизмальное повышение артериального давления и другие расстройства. Мы склонны считать, что синдром вегето-висцеральных дисфункций у детей с синдромом Платтера встречается значительно чаще, чем у указанных 12,5% пациентов. На существование гиподиагностики синдрома вегето-висцеральных дисфункций могут указывать выявленные нами фенотипические особенности детей, в том числе очень хороший (скорее избыточный) аппетит, склонность к задержке жидкости, как бы немотивированный субфебрилитет. Наши наблюдения показали, что у большинства детей с якобы немотивированным субфебрилитетом последний хорошо контролировался мочегонными средствами, что явно указывает на связь этого симптома с ликворной гипертензией, в том числе с повышением давления в области третьего желудочка мозга — месте локализации центра терморегуляции.
У детей с синдромом Платтера обращал на себя внимание и синдром мышечной гипотонии, который у ряда пациентов был настолько сильно выражен, что специалисты высказывали предположение о наличии у них болезни Верднига–Гоффманна или миелодисплазии.
Таким образом, частое выявление у детей с синдромом Платтера внутренней гидроцефалии, изолированного синдрома вегето-висцеральных дисфункций, наличие вегетативных нарушений указывает на возможность нарушения функции диэнцефальной области. Изменения со стороны скелетной мускулатуры трактовать сложнее. Однако если учесть, что средний мозг, примыкающий к области сильвиева водопровода, контролирует регуляцию мышечного тонуса и сигналы к мышцам поступают через ретикулярную формацию по двум ретикулоспинальным путям [11], то это нарушение может быть рассмотрено с позиции существования у данного контингента детей внутренней гидроцефалии и расстройства ликвородинамики, поскольку гипоталамус, таламус и ретикулярная формация являются звеньями единой суперфункциональной системы, корригирующей гомеостатические программы наиболее сложных вегетативных, эндокринных, трофических и психических функций [12].
У 9% пациентов школьного возраста с синдромом Платтера зарегистрированы заболевания нейроэндокринной и эндокринной системы (диэнцефальный синдром, несахарный диабет, транзиторный несахарный диабет, транзиторный гипопаратиреоз, инсулинозависимый сахарный диабет, поликистоз яичников, эутиреоидная струма, диффузный токсический зоб, субкомпенсированный гипокортицизм). У детей с синдромом Платтера, отмечается тенденция к высоким показателям роста и слабой пигментации кожи, что может также указывать на дисфункцию гипоталамо-гипофизарной системы. Кроме того, у этих детей существует ряд симптомов, которые мы назвали торакальными и к числу которых относится синдром сдавления средостения. Этот синдром мы наблюдали только у детей первых 2–2,5 мес жизни при значительном увеличении тимуса.
Все исследователи, занимавшиеся изучением особенностей лиц со стойкой тимомегалией (а основную группу в них, вне всякого сомнения, составляют дети с синдромом Платтера), обращали внимание на их пониженную физическую активность.
При специальном опросе 72 пациентов в возрасте 10–24 лет с синдромом Платтера у 46% из них было отмечено негативное отношение к физическим нагрузкам, особенно к бегу на длинные дистанции и езде на велосипеде. Подростки и лица молодого возраста, способные передать ощущения, появлявшиеся при физической нагрузке, отмечали на ее фоне чувство слабости, ощущение нехватки воздуха.
Когда у 30 подростков с синдромом Платтера, не имевших органических заболеваний сердца, было проведено эхокардиографическое исследование сердца на аппарате 128 х Р — ACUSON (США) с определением массы миокарда левого желудочка сердца, у 27 из них индексированная (относительно массы тела) масса миокарда левого желудочка сердца оказалась достоверно меньше (р
Л. Г. Кузьменко, доктор медицинских наук, профессор
РУДН, Москва



