У ребенка после болезни упадок сил что делать
Повышенная утомляемость у детей
Автор: Росточек —
Быстрая утомляемость у ребенка неизбежно вызывает беспокойство родителей. Заподозрить причины снижения умственной и физической активности можно самостоятельно, но достоверно их подтвердят только результаты медицинского обследования. В зависимости от того, что вызвало хроническую усталость, назначается коррекция образа жизни, рациона питания или лекарственная терапия.
Физиологические причины повышенной утомляемости
Причиной утомляемости у ребенка могут стать физиологические факторы. Они не вызывают опасения у врачей и легко поддаются коррекции.
Когда усталость – симптом патологии
Если ребенок жалуется на усталость внезапно, при условии отсутствия изменений в физической и умственной нагрузке, необходимо внимательно присмотреться к дополнительным признакам. Причиной повышенной утомляемости могут стать:
Чаще всего усталость появляется в период респираторных заболеваний. Родители могут еще не замечать катаральных проявлений, но отметить повышенную сонливость, неуклюжесть, капризы.
Чем помочь ребенку в домашних условиях
Чтобы предотвратить повышенную утомляемость, необходимо правильно организовать режим дня, питания, а также составить расписание физических и умственных тренировок.
Не менее двух раз в год необходимо проходить диспансеризацию, включающую:
К Вашим услугам консультации и лечение опытными неврологами.
Астеновегетативный синдром у детей после перенесенных инфекционных заболеваний
В развитии инфекционного заболевания обычно выделяют четыре периода: латентный (инкубационный), продромальный, разгар болезни и исход. Латентный период продолжается от момента воздействия этиологического фактора до появления первых кли
В развитии инфекционного заболевания обычно выделяют четыре периода: латентный (инкубационный), продромальный, разгар болезни и исход. Латентный период продолжается от момента воздействия этиологического фактора до появления первых клинических признаков болезни. В этот период происходит мобилизация защитных сил организма, направленных на компенсацию возможных нарушений, на уничтожение болезнетворных агентов и удаление их из организма. Продромальный период представляет собой временной интервал от первых симптомов заболевания до полного проявления. Период выраженных проявлений заболевания характеризуется полным развитием клинической картины. При различных инфекционных заболеваниях может страдать нервная система ребенка, что клинически проявляется синдромом нейротоксикоза. Нейротоксикоз — ответная неспецифическая реакция детского организма на воздействие вирусной, бактериальной или вирусно-бактериальной флоры, характеризующаяся преимущественным поражением центральной (ЦНС) и вегетативной нервной системы. С истощением функциональных возможностей органов и систем в результате перенесенного заболевания, особенно нервной системы при ее перенапряжении, а также вследствие аутоинтоксикации или экзогенного токсикоза связывают возникновение астенического синдрома. Это наиболее частое клиническое проявление периода реконвалесценции. Утомление в течение длительного времени, которое не компенсируется полным восстановлением, вызывает синдром перегрузки, следом за которым развивается состояние истощения. Субъективно ощущаемое чувство утомления — прежде всего сигнал о перегрузке центральных регуляторных систем, неудовлетворительном состоянии энергетических ресурсов организма и аутоинтоксикации продуктами метаболизма. Длительное утомление, приводящее к истощению, по сути своей является результатом стрессорного воздействия на организм, вызывающего нарушение функций регуляторных систем — вегетативной, эндокринной и иммунной. Если стрессорные факторы действуют в течение длительного времени, может развиться реакция организма, при которой возможны функциональные изменения в виде вегетативной дисфункции [1, 6]. Синдром вегетативной дисфункции (СВД) включает в себя проявление всех форм нарушения вегетативной регуляции. Наряду с соматическими проявлениями: головокружением, головными болями, сердцебиением, одышкой, жаждой, булимией, рвотой после еды, непереносимостью отдельных видов пищи, субфебрилитетом неясного происхождения, кожными высыпаниями и др., у пациентов с СВД выявляют эмоциональные расстройства разной степени выраженности в виде тревожности, нарушения сна, беспричинного плача, а также расстройства поведения, в частности, импульсивности, повышенной двигательной активности и возбудимости, дефицита внимания, что клинически определяется как астеновегетативный или психовегетативный синдром [Вейн А. М., 1981].
Интерес и сложность проблемы астеновегетативного синдрома заключается в том, что она является комплексной: медицинской, психологической и педагогической. Однако все специалисты сходятся в том, что такое состояние существует, его необходимо диагностировать и правильно корректировать.
Задачи исследования
Данное исследование посвящено изучению динамики состояния вегетативной нервной системы детей с астеновегетативным синдромом после перенесенных инфекционных заболеваний, а также оценке эффективности препарата Тенотен детский при названной патологии.
Тенотен детский содержит сверхмалые дозы антител к мозгоспецифическому белку S-100, создан по особой технологии специально для детского возраста, оказывает успокаивающее, нормализующее настроение и поведение действие, а также выраженное вегетостабилизирующий эффект [3, 5].
Критерии включения больных в исследование:
Критерии исключения больных из исследования:
Материал исследования
В МУЗ «5 Детская инфекционная больница г. Саратова» наблюдалось 50 детей в возрасте от 3 до 8 лет (4,54 ± 0,18 года), из них 52% мальчиков, 48% девочек, перенесших осложненные респираторные вирусные и другие воздушно-капельные инфекции, протекающие в основном с синдромом нейротоксикоза, а также часто болеющие дети, состоящие на диспансерном наблюдении в поликлинике.
Для исследования методом случайной выборки дети были распределены в две группы. В основной группе (30 человек) дети в периоде реконвалесценции наряду с симптоматической витаминотерапией получали Тенотен детский по 1 таблетке 3 раза в день в течение 4 недель в сочетании со стандартной терапией. В контрольную группу (20 человек) вошли дети, получавшие стандартную витаминотерапию и симптоматическую терапию за исключением препаратов, обладающих вегетотропной активностью.
Достоверных различий по половозрастным показателям между основной и контрольной группами детей не было.
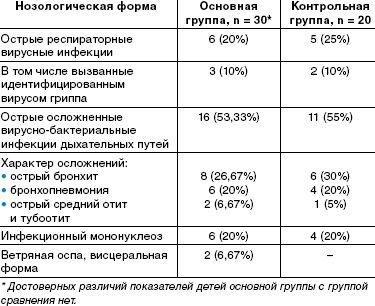
По спектру перенесенных заболеваний, их тяжести, характеру осложнений выделенные группы детей также значительно не отличались. Спектр заболеваний включал вирусные и вирусно-бактериальные инфекции дыхательных путей (этиологически подтвержденные формы гриппа и другие респираторные вирусные инфекции, тяжелые формы бронхитов и пневмоний и др.), острые средние отиты, тяжелые и осложненные формы инфекционного мононуклеоза, висцеральные формы ветряной оспы, протекающие с нейротоксикозом и везикулезными высыпаниями на внутренних органах. Данные о заболеваниях приведены в таблице.
Диагностическое обследование включало в себя клиническую оценку проявлений вегетативной дисфункции, психологическое исследование, неврологическое обследование, электрокардиографию (ЭКГ).
Состояние вегетативной нервной системы определялось по исходному вегетативному тонусу, вегетативной реактивности и вегетативному обеспечению деятельности. Исходный вегетативный тонус, характеризующий направленность функционирования вегетативной нервной системы в состоянии покоя, оценивался по анализу субъективных жалоб и объективных параметров. Оценивалась степень выраженности психопатологических проявлений: утомляемость, тревожность, эмоциональная неустойчивость и др. (модифицированный опросник А. М. Вейна). Определялся внутрисистемный вегетативный тонус по индексу Кердо и межсистемный вегетативный тонус по коэффициенту Хильдебранта. Для оценки вегетативного обеспечения деятельности, отражающего в основном состояние автономной системы регуляции, проводилась клиноортостатическая проба (КОП). Функциональное состояние сердечно-сосудистой системы рассматривалось также на основании данных электрокардиографии.
Уровень внимания оценивался с использованием шкалы SNAP-IV, таблиц Шульте, по результатам модифицированного метода Пьерона–Рузерапо. Выявление расстройств кратковременной и долговременной памяти, косвенно отражающей выраженность астении, проводилось с помощью методики 10 слов и пиктограммы.
Для определения состояния эмоциональной сферы обследуемых (тревоги, депрессии) использовался ахроматический и цветовой тесты Люшера.
После окончания лечения всем детям было проведено повторное комплексное обследование для оценки эффективности терапии. Кроме того, родителям детей предлагалось оценить результаты лечения при помощи десятибалльной аналого-визуальной шкалы, где 0 — это очень плохая оценка, 10 — очень хорошая.
Результаты исследования
Перед началом исследования у всех обследуемых детей (без достоверных различий в обеих группах) с помощью опросника А. М. Вейна определялись умеренно выраженные психопатологические расстройства, в виде неустойчивости эмоционального фона (84%), повышенной тревожности (34%), утомляемости (38%), отвлекаемости (86%), нарушений сна (74%), снижения памяти, а также различные соматические проявления в виде периодических головных болей (52%), головокружения (24%), метеозависимости (12%), снижения аппетита (64%), диспептических нарушений в виде тошноты, рвоты, вздутия живота (44%).
Индекс Кердо позволил определить наличие внутрисистемной дистонии у детей, перенесших тяжелые инфекционные заболевания, он составил в среднем 32,89 ± 0,99 в обеих исследованных группах, что свидетельствовало о превалировании симпатических влияний на организм в покое.
Межсистемный вегетативный тонус, оцениваемый с помощью коэффициента Хильдебранта (средние значения составили 3,98 ± 0,03), имел, в основном, эйтонический характер.
КОП, определяющая вегетативное обеспечение автономной системы регуляции, наряду с нормальным симпатикотоническим вариантом КОП, отражающим устойчивость гемодинамики в ортостазе (14% случаев), выявила и патологические варианты. Гиперсимпатикотонический вариант КОП, характеризующийся резким повышением систолического артериального давления (САД) и диастолического артериального давления (ДАД) и частоты сердечных сокращений (ЧСС) и обусловленный избыточным включением симпатико-адреналовой системы, встречался в преобладающем количестве случаев — у 58% детей. Асимпатикотонический вариант КОП, обусловленный недостаточным подключением симпатического отдела вегетативной нервной системы, при котором САД и ДАД не изменяются или падают, ЧСС остается нормальной или компенсаторно увеличивается, встречался у 28% детей с СВД. Астеносимпатический вариант КОП с падением САД и ДАД и резким увеличением ЧСС в первые минуты ортостаза, с последующей гиперсимпатикотонической реакцией был выявлен в 2% случаев.
Функциональное состояние сердечно-сосудистой системы рассматривалось также на основании данных ЭКГ. Синусовая тахикардия по данным ЭКГ была обнаружена у детей в 70% случаев, по-видимому, как результат экстракардиальных влияний (усиление симпатической иннервации сердца или ослабления вагусной на фоне психоэмоционального возбуждения) при отсутствии органической патологии сердца, так называемая «нервная тахикардия».
Основными психопатологическими проявлениями СВД являлись невнимательность, гиперактивность, импульсивность. Их оценка производилась с помощью шкалы-опросника SNAP-IV (Swanson J., 1992). Показатель невнимательности в двух группах по этой шкале достоверно не отличался и составил в среднем 53,33% (норма (Swanson J., 1992) — 0,40–1,82), средний показатель гиперактивности — 1,96 ± 0,32 (норма (Swanson J., 1992) — 0,27–1,59) и импульсивности 2,13 ± 0,37 (норма (Swanson J., 1992) — 0,26–1,52) (p
Е. В. Михайлова, доктор медицинских наук, профессор
Т. Ильичева
Cаратовская областная детская инфекционная клиническая больница,
Саратовский государственный медицинский университет, Саратов
Постинфекционная астения у детей: выбор оптимальной терапии
С наступлением осенне-зимнего сезона у врачей-педиатров заболеваемость их пациентов острыми респираторными вирусными инфекциями (ОРВИ) приобретает исключительную актуальность.
Постинфекционный астенический синдром
Врачам хорошо известна структура вирусов, провоцирующих это заболевание: на 65‒90% в ней представлены вирусы гриппа и парагриппа, аденовирусы и респираторно-синцитиальный вирус. В половине случаев (52%) педиатры имеют дело с вирусной моноинфекцией, в 36% выявляется ассоциация из 2 (и более) вирусов. 1
У каждого ребенка ОРВИ протекает с разной степенью тяжести. Сказывается не только разнообразие патогенов, но и возраст, состояние иммунитета, наличие неблагоприятного преморбидного фона (аденоиды, аллергия), врожденные патологии.
Тем не менее алгоритмы ведения маленьких пациентов с ОРВИ хорошо отработаны. В общей педиатрической практике детям назначается симптоматическая противовирусная терапия, проводится санация очагов хронической инфекции. 2 Вот только нередко бывает, что на смену катаральным явлениям приходит иная клиническая картина – астенический синдром, проявления которого – утомляемость, слабость, раздражительность, плаксивость – наблюдаются у 55‒64% пациентов. 3,4
И это вполне объяснимо: на борьбу с вирусной инфекцией организм тратит много сил и энергии. Даже при повышении температуры лишь на один градус потребность организма в энергии возрастает на 13%. 5 Свою роль играют лекарственная нагрузка и вирусная интоксикация, которые приводят к изменениям в обмене веществ, к ухудшению аппетита (организм недополучает необходимых веществ, ответственных за выработку энергии и восстановление), снижению защитных сил организма.
И это серьезно, потому как астенические расстройства значительно ухудшают качество жизни, усложняют адаптацию в дошкольных и школьных учреждениях, нарушают процесс обучения, снижают коммуникативную активность.
Говоря о повышенной утомляемости, следует разграничивать два разных понятия: «физиологическая усталость», которая возникает у практически здоровых людей после физической или умственной нагрузки и всегда исчезает после отдыха, и «астения» как ощущения слабости и утомляемости, которые не связаны с какой-либо нагрузкой, возникают и в покое и не исчезают после отдыха. 5
Надо заметить, специалисты рассматривают ощущение утомления и усталости как побуждение к прекращению активности, деятельности, любых усилий и т.д. Если анализировать этот феномен с позиций базовых биологических реакций: нападение – бегство и сохранение – отказ, то астения может рассматриваться как активация системы сохранения энергии посредством отказа и прекращения как физической, так и умственной деятельности. Снижение активности – это универсальный психофизиологический механизм сохранения жизнедеятельности системы в случае любой угрожающей ситуации, который действует по принципу: меньше активности – меньше потребности в энергии. Таким образом, астения – это общая реакция организма на любое состояние, угрожающее истощением энергетических ресурсов. 5
Постинфекционный астенический синдром:
На важное значение астении после перенесенных ОРВИ для клинической практики указывают не только многочисленные научные изыскания, но и тот факт, что в Международной классификации болезней 10-го пересмотра среди других астенических состояний отдельно выделен синдром G93.3 – синдром усталости после перенесенной вирусной инфекции. 6
Астенический синдром (синдром хронической усталости в англоязычной литературе) весьма многолик. В классификации этого состояния постинфекционный астенический синдром относится к классической вторичной (или реактивной) астении, возникающей у исходно здоровых лиц как реакция на напряжение адаптации в условиях стресса, а также в периоде реконвалесценции (после окончания болезненного процесса и продолжающееся до полного восстановления нормального питания и функционирования всех органов) после инфекционных заболеваний. Наиболее подвержены астеническим реакциям дети со сниженными адаптивными возможностями организма.
Ведущий патогенетический механизм развития астении связывают с нарушением функции ретикулярной формации, регулирующей активность коры и подкорковых структур, называемой также «энергетическим центром» центральной нервной системы (ЦНС). 3 К другим механизмам развития этого синдрома относят аутоинтоксикацию продуктами метаболизма, нарушение регуляции выработки и использования энергетических ресурсов на клеточном уровне. Метаболические расстройства, имеющие место при астении, приводят к гипоксии, ацидозу с последующим нарушением процессов образования и использования энергии. 3
Астения, без сомнения, представляет серьезную опасность повышенной истощаемости психических и физических функций организма. В реальной клинической картине ее механизмы могут проявляться не только эмоционально-поведенческими расстройствами (эмоциональной лабильностью, неусидчивостью, чувством тревоги, раздражительностью, беспокойством, внутренним напряжением, неспособностью расслабиться и пр.), но и соматическими проявлениями – нарушениями терморегуляции, респираторными, гастроинтестинальными, вегетативными или функциональными расстройствами (головными болями, потливостью, ухудшением аппетита, перебоями в сердце, одышкой, нарушениями сна). 4
Отмечено, длительно протекающая астения может стать причиной обострения хронического заболевания или реинфекции. Потому это состояние, вне зависимости от причины, вызвавшей его, требует коррекции. Тактика ведения пациентов с постинфекционным астеническим синдромом предполагает комплексный подход, предусматривающий прежде всего полноценный восстановительный период и рациональную фармакотерапию. Ее целью должны быть устранение энергодефицита и гипоксии, церебропротекция и нормализация метаболизма. При этом использование психостимуляторов для лечения больных с постинфекционной астенией нежелательно. 4
L-карнитин в комплексной терапии астенического синдрома
Более 100 лет назад (1905 г.) русскими учеными Р. Кримбергом и В.С. Гулевичем из мышечных тканей животных было выделено витаминоподобное вещество – карнитин. Позже выяснилось, что биологической активностью обладает только L-стереоизомер карнитина (L-карнитин, левокарнитин). Более полувека ушло на то, чтобы его синтезировать. И еще десятилетия – на изучение основных функций карнитина в организме: участие в биоэнергетическом обмене веществ, связывание и выведение из тканей органических кислот – промежуточных продуктов окислительных процессов и др. Столь важное значение карнитина в метаболизме жиров, глюкозы, аминокислот и энергообразовании позволило отнести его к незаменимым веществам.
Карнитин содержится во всех органах, особенно в больших количествах в тканях, нуждающихся в высоком энергетическом обеспечении, – мышцах, миокарде, мозге, печени, почках. Потребность в карнитине индивидуальна (в среднем 200‒500 мг в сутки для взрослого человека) и возрастает в 4‒20 раз при умственных, физических и эмоциональных нагрузках, заболеваниях и функционально особых состояниях (стресс, беременность, спорт и т.п.). Эндогенный синтез у взрослого человека обеспечивает только около 10% потребности организма в карнитине и требует участия витаминов С, В3, В6, фолиевой кислоты, железа, ряда аминокислот и ферментов; при дефиците хотя бы одного из компонентов развивается недостаточность карнитина с ее многообразными системными проявлениями. У детей раннего возраста эндогенный синтез L-карнитина практически не осуществляется, что делает их более уязвимыми к дефициту экзогенного поступления карнитина с продуктами питания (особенно животного белка). Обычный пищевой рацион покрывает потребность в карнитине в лучшем случае наполовину. Все это обусловливает необходимость использования его дополнительных источников. 7
Являясь важным компонентом энергообеспечения клетки, L-карнитин воздействует на многие процессы жизнедеятельности организма, повышает его выносливость к нагрузкам – физическим и интеллектуальным, а его дефицит, сопровождающийся снижением концентрации вещества в сыворотке крови и тканях, может приводить к разнообразным нарушениям. Принимая во внимание это, а также то, что естественное поступление этого биологического вещества в организм и его эндогенный синтез (особенно при инфекционных заболеваниях) не покрывают всех потребностей, необходим дополнительный прием препаратов L-карнитина. 7
Особенно очевидным это становится при рассмотрении функций L-карнитина. Основная из них – биоэнергетическая: L-карнитин обеспечивает транспорт длинноцепочечных жирных кислот из цитоплазмы через внутреннюю мембрану в матрикс митохондрий, где осуществляется процесс β-окисления с последующим образованием АТФ, регулирует интенсивность митохондриального энергообмена путем конъюгации ацильного радикала и высвобождения КоА. 7 Доказано значение L-карнитина для связывания высокореакционных органических кислот (уксусной и др.), а также участие в процессе гликолиза, обмене кетоновых тел и холина.
L-карнитин обладает антигипоксантным, антиоксидантным действием, предотвращает дегенеративное поражение клеток нервной системы, способствуя восстановлению их целостности и функций. 7
Препараты на основе L-карнитина производятся во многих странах мира в различных лекарственных формах для перорального и парентерального введения. В России с 2000 года широко используется лекарственный препарат L-карнитина Элькар® (МНН: левокарнитин), разработанный отечественной компанией «ПИК-ФАРМА».
Области применения левокарнитина и уникальное сочетание его терапевтических эффектов отражены в зарегистрированных показаниях к применению препарата Элькар. 8
Витаминоподобное вещество L-карнитин участвует в переносе жирных кислот в митохондрии, где они используются для образования энергии (АТФ). Окисление жиров при участии L-карнитина дает до 75% внутриклеточной энергии. Это больше, чем в процессе окисления глюкозы.
L-карнитин, помимо биоэнергетической, выполняет ряд важных метаболических функций: 8
Два десятилетия наблюдений, многочисленных исследований и клинического применения препарата Элькар® при лечении различных заболеваний и патологических состояний у детей и взрослых показали высокую эффективность, безопасность и открыли широкие возможности его применения для лечения пациентов в кардиологии, эндокринологии, неврологии, гастроэнтерологии, спортивной медицине. В педиатрии препарат применяют при заболеваниях и состояниях, сопровождающихся снижением аппетита, уменьшением массы тела, истощением; у детей с самыми разными патологиями с рождения (недоношенные, дети с ослабленными пищевыми рефлексами, с гипотрофией, гипотонией и адинамией, перенесшие асфиксию и родовую травму); при заболеваниях, сопровождающихся недостатком карнитина или его повышенной потерей; в составе комплексной терапии ряда кожных болезней, при интенсивных спортивных тренировках и, конечно же, в период реконвалесценции после заболеваний, в том числе и ОРВИ.
Так, в исследовании С.О. Ключникова (2005) у часто болеющих детей, помимо иммунной патологии, был установлен клеточный энергодефицит. Для его устранения детям с ЛОР-патологией назначались энерготропные препараты, включая левокарнитин. Нормализация показателей фагоцитарной активности нейтрофилов, активности ферментов энергообмена лейкоцитов крови (СДГ, ЛДГ, ГФДГ, ГДГ) и восстановление ферментативной активности лимфоцитов (от 18 до 27%) привели к снижению заболеваемости ОРВИ у детей после приема курсового приема энерготропной терапии. 9 При этом у детей с дисбалансом вегетативной регуляции на фоне приема комплексной терапии с включением препарата левокарнитина в 100% случаев отмечено улучшение вегетативной реактивности, что привело к уменьшению жалоб, нормализации сна и аппетита, повышению физической выносливости. 9
Авторы исследования отметили отсутствие каких-либо побочных эффектов препарата левокарнитина даже у детей с отягощенным аллергоанамнезом и признаками поражения ЦНС. 10
Позже, в сравнительном плацебо-контролируемом исследовании по оценке эффективности применения Элькар® в лечении детей с хроническими бронхолегочными заболеваниями, сопровождающимися нарушениями гемодинамики в системе малого круга кровообращения (хронический бронхит, бронхоэктатическая болезнь, пороки развития легких, гиперчувствительный пневмонит, бронхиальная астма), Л.И. Агапитовым и Ю.М. Белозеровым (2010) 11,12 были продемонстрированы антиоксидантные свойства левокарнитина. После курса лечения у детей с хроническими бронхолегочными заболеваниями, получавших препарат Элькар в течение 4 недель (50 мг/кг в сутки), увеличились максимальная и тотальная эндотелий-зависимая вазодилатация (p 11,12
Оценку эффективности левокарнитина (Элькар®) у детей с бронхиальной астмой физического напряжения дали исследования Г.А. Новика (2009, 2012). Пациенты основной группы (с подтвержденным постнагрузочным бронхоспазмом) получали Элькар в течение 2 месяцев, дети группы сравнения препарат не получали (обе группы пациентов были сопоставимы по клиническим и лабораторным показателям). При динамическом наблюдении показатели внешнего дыхания и величина просвета бронхов у детей обеих групп существенно не изменились, но у детей основной группы, в отличие от контрольной, повысилась толерантность к физической нагрузке (р 13
Влияние Элькара на состояние вегетативной регуляции и повышение устойчивости к нагрузкам показано в исследовании С.Л. Морозова (2015). Так, при оценке показателей вариабельности сердечного ритма у детей отмечались нормализация состояния вегетативной нервной системы и, как следствие, повышение адаптации. 2
Улучшение адаптации, а также обмена веществ и энергообеспечения тканей при применении Элькар®, но уже у юных спортсменов доказало и исследование Л.А. Балыковой и соавт. 14,15 Дети со стрессорной кардиомиопатией принимали препарат курсом 1,5 месяца в лечебной дозе 75‒100 мг/кг/сут, спортсмены без признаков поражения сердца ‒ в профилактической дозе 30‒50 мг/кг/сут.
Прием левокарнитина (Элькар®) показал изменения в эффекторных и иммунорегуляторных звеньях врожденного и адаптивного иммунитета. У большинства юных спортсменов при приеме Элькар® показатели гуморального иммунитета достигли нормы, что в сочетании с улучшением показателей клеточного иммунитета (увеличение абсолютного количества нейтрофилов и их метаболической активности) способствовало повышению противоинфекционной резистентности организма и снижению заболеваемости ОРВИ. Кроме того, лечение способствовало возрастанию уровня физической работоспособности, оптимизации гемодинамики в области сердца и уменьшению уровня биохимических, психологических и других маркеров стресса. 14,15
Эффекты препарата Элькар ® при восстановлении после болезни:
Таким образом, приведенные данные исследований, а также многие другие, не вошедшие в этот обзор, свидетельствуют о сочетании метаболических, нейропротекторных и иммунокоррегирующих свойств левокарнитина и эффективности отечественного лекарственного препарата на его основе Элькар® (L-карнитин) в терапии и профилактике обширного круга состояний и заболеваний, сопровождающихся явлениями астении, в том числе и после ОРВИ.
Применение Элькара позволяет существенно улучшить состояние здоровья детей, нормализуя механизмы вегетативной регуляции, стабилизируя клеточный энергообмен, что, в свою очередь, способствует возрастанию их физической активности и повышению иммунитета.