гиперплазия костного мозга причины
Главный онколог «СМ-Клиника» рассказал об опухолях костного мозга
Среди всех опухолей в области центральной нервной системы поражения спинного мозга занимают примерно 12% у взрослых и около 5% у детей. В чем причина этих патологий и как их лечат?
АЛЕНА ПАРЕЦКАЯ
Врач-патофизиолог, иммунолог,
член Санкт-Петербургского
общества патофизиологов
АЛЕКСАНДР СЕРЯКОВ
Д.м.н., профессор, врач-онколог,
врач-гематолог, врач-радиолог
(лучевой терапевт) высшей категории,
ведущий онколог холдинга «СМ-Клиника»
Наиболее часто опухоли, локализованные в области спинного мозга, выявляются у людей в возрасте от 30 до 50 лет. Преимущественно, примерно в 85% случаев, они поражают оболочки мозга и окружающие его структуры.
Что нужно знать об опухоли спинного мозга
Что такое опухоль спинного мозга
– Опухоли спинного мозга, – говорит врач-онколог Александр Серяков, – это патологические новообразования злокачественной и доброкачественной природы, которые локализуются в области спинного мозга. Они встречаются редко.
По расположению бывают:
Причины опухоли спинного мозга у взрослых
Истинные причины опухолевого роста, который возникает в области спинного мозга, на сегодняшний день не определены. Ученые выделяют ряд факторов риска, которые могут повышать вероятность опухолевого роста у детей или взрослых, но однозначно не приводят к образованию патологии. Сюда включают:
Симптомы опухоли спинного мозга у взрослых
Нет типичных или характерных симптомов только для опухоли, все признаки могут имитировать и другие болезни, особенно на ранних стадиях. Поэтому стоит обращаться к врачу, чтобы определить или исключить проблему при следующих жалобах.
Болевой синдром. Наиболее частым проявлением опухоли становится боль, которая возникает в области позвоночника, где начала свой рост опухоль. В ранней стадии боль может быть легкой или более сильной, но выраженных неврологических симптомов при этом нет. По мере прогрессирования опухоли возникают расстройства чувствительности и движения, боль становится сильнее на фоне кашля или резких движений, чихания, физической нагрузки, ночью и при движениях, наклонах головы.
Двигательные расстройства. Возможна также слабость мышц, которая возникает в сочетании с расстройствами чувствительности, явления атрофии мышц, резкие и внезапные ее сокращения, подергивания мышечных групп, которые расслаблены.
Расстройства чувствительности. Иногда болевых ощущений нет, но могут страдать поверхностная чувствительность, на фоне сохранения глубокого тактильного чувства. Пациент может не ощущать боль, температуру, прикосновения, но воспринимает давление, вибрации.
Проблемы с работой сфинктеров. Возможны нарушения мочевыделительных функций, реже – опорожнения кишечника. Это приводит к задержке мочи или стула.
Также по мере прогрессирования процесса может возникать сколиоз позвоночника, который формируется из-за болевых ощущений, расстройств двигательной функции или разрушения тел позвонков.
Внешне определить опухоли спинного мозга невозможно, они расположены достаточно глубоко в области спинномозгового канала.
Классификация опухолей спинного мозга у взрослых
Существует достаточно много вариантов классификации опухолей, локализованных в области спинного мозга. Возможно разделение на группы по ряду признаков – расположение опухолевого очага относительно спинного мозга, позвоночника или мозговых оболочек, особенности гистологической картины, а также конкретная локализация поражения.
Если делить опухоли по происхождению, их можно отнести к двум группам:
По происхождению и типу клеток классификация очень большая, опухоли определяют по данным биопсии.
Лечение опухоли спинного мозга у взрослых
Диагностика
Проведение диагностики – это поэтапный процесс, который позволяет определить размеры, тип опухоли и составить план ее лечения. Прежде всего, врачу важны жалобы пациента, имеющиеся у него симптомы, история болезни. Важно – когда развились симптомы, как они изменялись со временем.
Также проводится полное неврологическое обследование – определение тонуса мышц, рефлексов, силы мышц, подвижности позвоночника, чувствительности.
Для утонения патологии необходимы:
Современные методы лечения
– Основной вид лечения, – рассказывает врач-онколог Александр Серяков, – это нейрохирургическая операция, при которой полностью удаляется новообразование и выполняется декомпрессия (устранение сдавления) спинного мозга. Используются часто микро-нейрохирургические техники, интра-операционная нейровизуализация и нейронавигация.
При злокачественных опухолях спинного мозга кроме хирургического лечения пациенту могут назначить химиотерапию и лучевую терапию (стереотаксическая радиотерапия и радиохирургия на линейных ускорителях типа «Кибер-Нож»).
Профилактика опухолей спинного мозга у взрослого в домашних условиях
Профилактика, по словам врача-онколога Александра Серякова, это здоровый образ жизни:
Популярные вопросы и ответы
Какие могут последствия у опухоли спинного мозга?
Какие симптомы должны быть поводом для визита к врачу?
При опухоли спинного мозга различают 3 клинических синдрома:
Гиперплазия костного мозга причины
а) Синонимы:
• Реконверсия костного мозга
1. Общие характеристики:
• Наиболее значимый диагностический признак:
о Изо- или гипоинтенсивность сигнала костного мозга позвонков по сравнению с межпозвонковыми дисками (которые в Т1 отличаются гиперинтенсивным сигналом)
• Размеры:
о Изменения обычно затрагивают весь позвоночник
• Морфология:
о Диффузные гомогенные изменения сигнала
о Пятнистая «географическая» картина
2. Рентгенологические данные гиперпластического костного мозга:
• Рентгенография:
о Гемолитические анемии:
— Расширение костномозговых пространств ребер, костей черепа, длинных трубчатых костей
— Истончение кортикальной кости
— Исчерченность костей свода черепа, напоминающая картину «вставших дыбом волос»
— Двояковогнутые позвонки при серповидноклеточной анемии
3. КТ при гиперпластическом костном мозге:
• Костная КТ:
о Позвонки, напоминающие букву «Н» вследствие инфарктов кости вблизи замыкательных пластинок при серповидноклеточной анемии
о Расширение костномозговых пространств при талассемии
4. МРТ при гиперпластическом костном мозге:
• Т1-ВИ:
о Изо- или гипоинтенсивность сигнала по сравнению с межпозвонковыми дисками:
— Изо- или некоторая гиперинтенсивность по сравнению с мышцами
— Ненормального костного мозга обычно выше, чем ИС мышц
о При исследовании на 1,5Ттомографе более низкая ИС костного мозга в Т1 по сравнению со скелетными мышцами или межпозвонковыми дисками не является нормой
о Наибольшая высокая диагностическая точность достигается при использовании в качестве стандарта ИС мышц при напряженности магнитного поля ЗТ
• Т2-ВИ:
о Промежуточная или низкая ИС:
— В Т2-режиме с подавлением сигнала жировой ткани ИС аналогична ИС мышц, но не превышает ее
• STIR:
о ИС аналогична ИС мышц и не превышает ее
о ИС гемопоэтического костного мозга > ИС жирового костного мозга
• Д-ВИ:
о Диффузия гемопоэтического костного мозга > диффузия жирового костного мозга
о Диффузионные характеристики костной ткани снижаются с возрастом
• Т1-ВИ с КУ:
о Минимальное контрастное усиление гадолинием:
— У взрослых старше 35 лет ИС костного мозга при КУ не должна увеличиваться более, чем на 35%
о При исследовании химического сдвига картина костного мозга тел позвонков может меняться по-разному:
— Снижение ИС более, чем на 20% на внефазовых изображениях по сравнению с фазовыми: это число считается пороговым значением, позволяющим дифференцировать доброкачественные и злокачественные изменения костного мозга позвонков
5. Радиоизотопные исследования:
• Костная сцинтиграфия:
о Дифосфонат 99m Тс или серный коллоид, меченый 99m Тс
— Зоны усиления захвата изотопа, представляющие собой расширенные костномозговые пространства:
Дистальные сегменты конечностей, свод черепа
• ПЭТ:
о Диффузное усиление захвата ФДГ наблюдается при лечении гранулоцитарными колониестимулирующими факторами:
— Усиление захвата и накопление ФДГ в нормальных, но подвергшихся стимуляции факторами роста клетках связано с активацией в этих клетках механизмов транспорта и метаболизации глюкозы
о При ПЭТ с ФДГ может выявляться фокальная гиперплазия костного мозга в виде небольшого усиления захвата ФДГ по сравнению с соседними участками красного костного мозга
6. Другие методы исследования:
• МР-исследование костного мозга с КУ оксидом железа:
о Нормальный или гиперклеточный костный мозг накапливает оксиды железа, обладающие супермагнитными свойствами:
— Выраженная потеря сигнала в STIR-режиме через 45-60 минут после инфузии оксида железа
о Метод может быть информативен при дифференциальной диагностике опухолевой инфильтрации от реконверсии костного мозга
7. Рекомендации по визуализации:
• Наиболее оптимальный метод диагностики:
о МРТ является методом выбора для исследования костного мозга:
— Т1-режим отличается высокой чувствительностью в отношении оценки клеточности костного мозга
• Протокол исследования:
о Т1-ВИ без КУ и с КУ и с подавлением сигнала жировой ткани о STIR или Т2-ВИ с насыщением жировой ткани:
— Для дифференциальной диагностики между гемопоэтическим костным мозгом и отеком или опухолевой инфильтрацией костного мозга
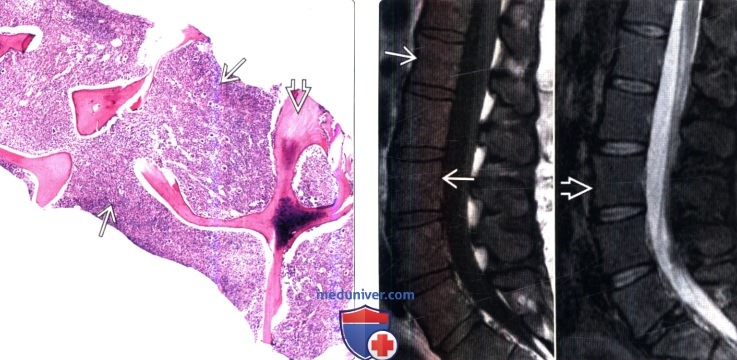
(Справа) На сагиттальных МР-И отмечается изоинтенсивность сигнала костного мозга позвонков относительно дисков. В STIR-режиме мы не наблюдаем патологической гиперинтенсивности сигнала костного мозга. Гиперплазия костного мозга характеризуется ИС, аналогичной ИС красного костного мозга.
в) Дифференциальная диагностика гиперпластического костного мозга:
1. Нормальный гемопоэтический костный мозг:
• Дети в возрасте примерно до 10 лет
2. Инфильтрация/замещение костного мозга:
• Лейкоз/лимфома
• Множественная миелома/метастазы:
о Диффузная или очаговая гипоинтенсивность Т1:
— Многоочаговое поражение легче отдифференцировать от гиперпластического костного мозга
— Диффузная инфильтрация костного мозга может характеризоваться такой же, как гиперплазия, картиной
о ИС обычно выше, чем ИС мышц в STIR или FS Т2
о Контрастное усиление гадолинием
о Усиление метаболической активности по данным ПЭТ
о Патологические компрессионные переломы
о Эпидуральный/паравертебральный мягкотканный компонент
3. Миелопролиферативное заболевание:
• Истинная полицитемия, хронический миелолейкоз, первичная тромбоцитемия, миелофиброз с миелоидной метаплазией
• МР-картина может напоминать нормальный гиперпластический костный мозг
4. Отек костного мозга:
• Различные причины, например, травма или инфекция:
о Гипоинтенсивность в Т1:
— ИС обычно меньше сигнала мышц
о Фокальная или распространенная гиперинтенсивность в STIR
о Интраспинальная или гематома мягких тканей при травме
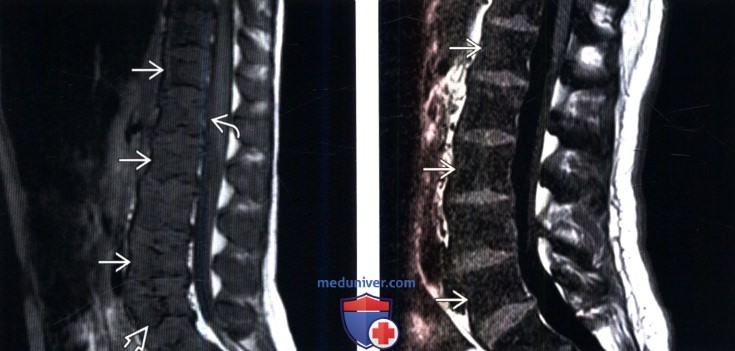
(Слева) Сагиттальный срез, Т1-ВИ: диффузная гипоинтенсивность сигнала костного мозга тел позвонков Б по сравнению со смежными межпозвонковыми дисками. Это томограмма пациентки с генерализованным метастатическим поражением на фоне рака молочной железы, которая кроме всего прочего получала стимулирующие гемопоэз препараты.
д) Клинические особенности:
1. Клиническая картина:
• Наиболее распространенные симптомы/признаки:
о Симптомов со стороны позвоночника может не быть
о Другие симптомы/признаки могутбыть связаны с анемией, гипоксемией:
— Бледность кожи и слизистых
— Слабость и утомляемость
— Одышка
— Застойная сердечная недостаточность
2. Демография:
• Этническая предрасположенность:
о Отсутствует, за исключением некоторых типов анемий:
— Серповидноклеточная анемия: афроамериканцы
— Талассемия: популяции, живущие вдоль восточного побережья Средиземного моря (греки, итальянцы, персы)
3. Лечение:
• Лечение причинного заболевания
• Гемотрансфузии
• Рекомбинантный эритропоэтин
е) Диагностическая памятка:
1. Следует учесть:
• Если в Т1-режиме выявляется гипоинтенсивность сигнала костного мозга, необходимо проводить исследование в Т2 (или STIR) с подавлением жировой ткани и Т1 с КУ
2. Советы по интерпретации изображений:
• Диффузная гипоинтенсивность Т1-сигнала костного мозга без значимого контрастного усиления или нарушения целостности кортикальных пластинок позволяет предположить гиперплазию костного мозга
• Нормальная в Т1 картина костного мозга при отсутствии адекватной настройки баланса между водой и жиром не всегда позволяет исключить инфильтрацию плазмоцитами или лимфоцитами
Редактор: Искандер Милевски. Дата публикации: 9.9.2019
Апластическая анемия
Апластическая анемия является тяжелым заболеванием крови, при котором развивается угнетение всех ростков костного мозга. Причины заболевания различные – от генетической предрасположенности до вредоносного действия ионизирующего излучения и различных химических соединений. Клинически заболевание проявляется анемическим, тромбоцитопеническим синдромом, а также выраженными инфекционными осложнениями.
Диагноз выставляется исходя из клинической картины, анализов крови и пункции костного мозга.
Что такое апластическая анемия?
Апластическая анемия является патологическим состоянием организма, при котором снижается количество всех трех типов клеток крови (эритроцитов, лейкоцитов и тромбоцитов) вследствие замедления или полного прекращения образования их в костном мозге.
По происхождению апластические анемии делятся на:
В большинстве случаев наблюдается угнетение всех трех ростков кроветворения, однако клинически замечено, что в различные фазы болезни может наблюдаться более выраженное угнетение какого-то одного из ростков
По преимущественному поражению костномозговых ростков выделяют:
Причины апластической анемии
Причины апластической анемии различаются при врожденной и приобретенной анемии.
Различают следующие причины приобретенных апластических анемий:
Некоторые вредоносные агенты непосредственно воздействуют на костный мозг (ионизирующее излучение, химические и лекарственные вещества). Иные воздействуют опосредованно через аутоиммунные механизмы (вирусный гепатит В).
Диагностика апластической анемии
Клиническая картина заболевания может в значительной степени ориентировать врача в направлении анемии, однако диагноз должен быть подтвержден или опровергнут при помощи лабораторных анализов и параклинических исследований.
Наиболее ценными дополнительными исследованиями являются:
Общий анализ крови
Данные общего анализа крови при апластической анемии свидетельствуют в пользу панцитопении (снижение количества всех трех типов клеток костного мозга). Уменьшение количества лейкоцитов наблюдается преимущественно за счет снижения гранулоцитов (нейтрофилы, эозинофилы и базофилы). Таким образом, относительно увеличивается процент лимфоцитов и моноцитов в лейкоцитарной формуле. На различных стадиях заболевания могут быть выявлены воспалительные признаки в той или иной мере.
Ориентировочными показателями ОАК при апластической анемии являются:
Гемоглобин (Hb) – менее 110 г\л (норма 120 – 160 г\л). Уменьшение за счет снижения числа эритроцитов.
Эритроциты – 0,7 – 2,5 х 1012\л (норма 3,7 х 1012\л). Снижение количества зрелых эритроцитов.
Цветовой показатель – 0,85 – 1,05 (норма 0,85 – 1,05) свидетельствует о нормохромном характере анемии (содержание гемоглобина в эритроците в пределах нормы).
Гематокрит (Ht) – менее 30 (норма 35 – 42 у женщин и 40 – 46 у мужчин). Соотношение клеточного состава крови к ее жидкой части. Наблюдается явное уменьшение доли клеток в периферической крови.
Тромбоциты – менее 35 промилле или 100 х 109\л. Снижение количества тромбоцитов.
Лейкоциты – 0,5 – 2,5 х 109\л (норма 4 – 9 х 109\л). Выраженная лейкопения за счет снижения числа гранулоцитов (нейтрофилы, эозинофилы и базофилы).
Палочкоядерные нейтрофилы – 0 – 2% (норма менее 6%). Снижение выработки молодых форм лейкоцитов.
Сегментоядерные нейтрофилы – 0 – 40% (норма 47 – 72%). Снижение количества зрелых форм нейтрофилов.
Миелоциты – 0 – 2% (в норме отсутствуют). В условиях гранулоцитопении и наслоения бактериальной инфекции наблюдается более выраженный, чем обычно, сдвиг лейкоцитарной формулы влево с появлением клеток предшественников лейкопоэза.
Эозинофилы – 0 – 1% (норма 1 – 5%). Снижение количества эозинофилов.
Базофилы – 0% (норма 0 – 1%). Единичные или полное отсутствие базофилов.
Лимфоциты – более 40% (норма 19 – 37%). Численное количество лимфоцитов остается в норме. За счет снижения фракции гранулоцитов наблюдается относительный лимфоцитоз (увеличение доли лимфоцитов в крови). Крайне выраженный лимфоцитоз может наблюдаться при наслоении вирусных инфекций.
Моноциты – более 8% (норма 6 – 8%). Количество моноцитов неизменно и находится в пределах нормы. Моноцитоз (увеличение доли моноцитов в крови) объясняется снижением процентной доли гранулоцитов в лейкоцитарной формуле.
Скорость оседания эритроцитов – более 15 – 20 мм\час (норма до 10 мм/час у мужчин и до 15 мм/час у женщин). Данный показатель отражает степень выраженности воспалительной реакции в организме.
Анизоцитоз – наличие в крови эритроцитов различного размера.
Пойкилоцитоз – наличие в крови эритроцитов различной формы.
Биохимический анализ крови
Некоторые виды биохимических анализов крови могут акцентировать внимание врача на отклонениях в организме, которые косвенно вписываются в три вышеперечисленных анемических синдрома.
Ориентировочными показателями БАК при апластической анемии являются:
Сывороточное железо более 30 мкмоль\л (норма 9 – 30 мкмоль/л). Увеличение сывороточного железа на фоне частых переливаний крови. Высокий риск развития гемохроматоза.
Эритропоэтин более 30 МЕ\л (норма 8 – 30 МЕ/л у женщин и 9 – 28 МЕ\л у мужчин). Увеличение эритропоэтина происходит по двум причинам. Во-первых, не происходит его потребления клетками эритроцитарного ростка. Во-вторых, компенсаторно усиливается его синтез в ответ на анемию.
С-реактивный белок – более 10 – 15 мг\л (норма 0 – 5 мг\л). Выявляется при воспалительной реакции на фоне ослабленного иммунитета.
Стернальная пункция
Данный вид исследования используется с целью визуализации клеток костного мозга и их процентного соотношения.
При апластической анемии миелограмма будет скудной, количество клеточных элементов значительно снижено. Камбиальные клетки эритроцитарного и лейкоцитарного ряда единичны или отсутствуют. Мегакариобласты отсутствуют. В редких случаях при пункции случается встретить сгруппированные очаги повышенной пролиферации клеток как компенсаторную реакцию здорового костного мозга на анемию. Такая миелограмма может сбить с толку, поскольку будет свидетельствовать в пользу отсутствия апластической анемии и поэтому будет ложноотрицательной.
Трепанобиопсия
Трепанобиопсия является способом изъятия части костного мозга из крыла подвздошной кости пациента. Преимущество данной процедуры над стернальной пункцией заключается в возможности забора большего количества материала с сохранением его структуры. Большее количество материала уменьшает вероятность ложноотрицательного результата апластической анемии, а изучение структуры костного мозга позволяет помимо цитологического исследования (миелограммы) провести еще и гистологическое.
При помощи анализа крови и результатов трепанобиопсии возможно определение степени тяжести апластической анемии.
гранулоциты менее 2,0 х 109\л;
тромбоциты менее 100 х 109\л;
ретикулоциты менее 2 – 3%;
гипоплазия костного мозга на трепанобиопсии.
гранулоциты менее 0,5 х 109\л;
тромбоциты менее 20 х 109\л;
ретикулоциты менее 1%;
аплазия костного мозга на трепанобиопсии.
гранулоциты менее 0,2 х 109\л;
тромбоциты единичные или отсутствуют;
ретикулоциты единичные или отсутствуют;
аплазия костного мозга на трепанобиопсии.
Прогноз при апластической анемии
Прогноз при апластической анемии во многом зависит от сроков обнаружения заболевания. При раннем обнаружении существует возможность более активного вмешательства в течение заболевания. При более позднем обнаружении шансы на излечение уменьшаются.
Врожденная апластическая анемия Фанкони в большинстве случаев крайне тяжело поддается лечению, поскольку костный мозг никогда не был здоровым и, соответственно, очень сложно восстанавливается. Наличие врожденных аномалий развития сильно ограничивает показания к пересадке костного мозга таким пациентам. В большинстве случаев больные погибают в детском возрасте от аномалий развития или инфекционных осложнений.
Приобретенные апластические анемии имеют более благоприятный прогноз, поскольку в некоторых случаях являются обратимыми после прекращения действия повреждающего фактора на костный мозг.
Врач лабораторной диагностики
Новополоцкой городской больницы
Костюк К.С.
Приемная главного врача
(+375 214) 50-62-70
(+375 214) 50-62-11 (факс)
Канцелярия
(+375 214) 50-15-39 (факс)
Диагностика и лечение хронической аутоиммунной гемолитической анемии
Больная Ш., 80 лет, пенсионерка. Из анамнеза известно, что в течение последних двух лет неоднократно проходила амбулаторное и стационарное лечение по поводу хронической B12–фолиеводефицитной анемии, диагностированной на основании анемического синдрома в сочетании с гиперхромией и макроцитозом эритроцитов. Стернальная пункция, определение уровня витамина B12 и фолиевой кислоты не проводились. Отмечался временный незначительный положительный эффект лечения витамином B12. С конца 2011 года, несмотря на ежемесячное введение витамина B12 в дозе 500γ в сочетании с фолиевой кислотой, стала нарастать анемия (14.02.2012 г. гемоглобин – 54 г/л). Для обследования и лечения госпитализирована в больницу № 40 с диагнозом: B12–фолиеводефицитная анемия тяжелой степени. ИБС. Стенокардия напряжения II ф. к. Гипертоническая болезнь II ст. Желчнокаменная болезнь. Хронический калькулезный холецистит. Мочекаменная болезнь. Конкремент правой почки, простые кисты обеих почек. Полипы желудка.
При поступлении жалобы на выраженную общую слабость, головокружения, головную боль, учащенное сердцебиение, перебои в работе сердца.
При объективном осмотре отмечены субиктеричность кожи и слизистых оболочек, умеренная гепатомегалия (+2 см) и спленомегалия (+ 2 см).
Результаты клинического анализа в динамике представлены в таблице 1.
Таблица 1. Клинические анализы крови пациентки Ш. в динамике
 |  | 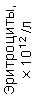 | 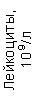 | 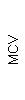 | 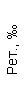 |  | 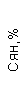 | 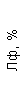 | 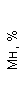 | 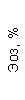 | 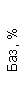 | 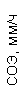 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.02.12 | 54 | 1.39 | 10.5 | 133 | 80 | 2 | 66 | 21 | 9 | 2 | — | 75 |
| 11.03.12 | 50 | 1.41 | 11.8 | 114 | 98 | 4 | 75 | 11 | 4 | 3 | 1 | 78 |
| 15.03.12 | 49 | 1.31 | 17.8 | 121 | 288 | 4* | 60 | 23 | 5 | 1 | — | 78 |
| 20.03.12 | 72 | 1.93 | 11.4 | 116 | 297 | 2 | 73 | 14 | 7 | 2 | 0 | 46 |
| 27.03.12 | 66 | 1.9 | 11 | 108 | 202 | 2 | 60 | 26 | 7 | 3 | 0 | 40 |
| 12.04.12 | 70 | 1.75 | 1.9 | 112 | 104 | 3 | 62 | 24 | 11 | 0 | 0 | 27 |
| 26.04.12 | 93 | 2.56 | 5.7 | 109 | 148 | 3 | 74 | 13 | 9 | 0 | 0 | 11 |
| 24.06.12 | 111 | 3.42 | 4.7 | 97 | 7 | 2 | 69 | 21 | 10 | 0 | 1 | 15 |
| 16.08.12 | 120 | 3.97 | 5.8 | 93 | 12 | — | 71 | 19 | 9 | 1 | 0 | 40 |
Примечание: * в лейкоцитарной формуле 15.03.12 выявлялись также миелоциты (2%) и метамиелоциты (5%).
В биохимическом анализе крови – повышение уровня креатинина (189 ммоль/л), билирубина (58 ммоль/л) за счет непрямого билирубина.
УЗИ органов брюшной полости: гепатоспленомегалия; камни желчного пузыря; диффузные изменения поджелудочной железы; простые кисты обеих почек, конкремент правой почки.
ФГДС: два полипа желудка размером до 0,5 см.
Учитывая высокий риск сердечно-сосудистых осложнений у пожилой пациентки с анемией тяжелой степени, проведены трансфузии эритроцитарной взвеси. На основании клинико-лабораторных данных (спленомегалия, гипербилирубинемия, гиперхромная анемия с ретикулоцитозом) и неэффективности лечения витамином B12 и фолиевой кислотой заподозрена гемолитическая анемия.
При исследовании крови на антиэритроцитарные антитела выявлены аутоантитела класса IgG ++++.
Результаты стернальной пункции представлены в таблице 2.
Таблица 2.Миелограмма пациентки Ш. от 17.02.12 г.
Заключение
Клеточный костномозговой пунктат. Эритропоэз – нормобластический. Гиперплазия эритроидного ростка – 74,8%. Со стороны эритрокариоцитов отмечаются клетки с цитоплазматическими мостиками, скопления в виде «эритроидных островков».
Мегакариоциты различной степени зрелости с умеренным тромбоцитообразованием.
На основании данных миелограммы (гиперплазия эритроидного ростка при нормобластическом типе кроветворения) и выявления антиэритроцитарных антител диагностирована аутоимунная гемолитическая анемия с тепловыми антителами. При дополнительном обследовании признаков вторичного характера анемии не выявлено.
С 11.03.12 г. начата пульс-терапия метипреднизолоном в дозе 500 мг 1 раз в день внутривенно в сочетании с пероральным приемом преднизолона в дозе 45 мг в сутки под прикрытием гастропротекторов. После 5 дней лечения анемический синдром продолжал нарастать, появился выраженный сдвиг лейкоцитарной формулы влево, увеличение количества ретикулоцитов (табл.1). Доза преднизолона перорально увеличена до 75 мг в сутки, к лечению добавлен азатиоприн по 100 мг/сутки per os, проведена трансфузия1 дозы эритроцитарной взвеси.
С 20.03.12 г. с учетом сохраняющегося гемолиза (ретикулоциты 297‰) проведен второй курс пульс-терапии метилпреднизолоном в дозе 500 мг в сутки № 4, однократно введен внутривенно циклофосфан в дозе 600 мг.
Лечение больная переносила хорошо. С 27.03.12 г. отмечена тенденция к увеличению уровня гемоглобина без поддерживающих гемотрансфузий. Решено продолжить введение циклофосфана по 200 мг в сутки, отменить азатиоприн. Анемический синдром продолжал уменьшаться: к 12.04.12 г. уровень гемоглобина достиг 70 г/л, снизился гемолиз (ретикулоцитов 104‰), однако развилась лейкопения (1,9×10 9 /л), в связи с чем циклофосфан был временно отменен. После восстановления количества лейкоцитов лечение циклофосфаном по 200 мг дважды в неделю было возобновлено на фоне постепенного снижения дозы преднизолона.
Больная в удовлетворительном состоянии 28.04.12 г. выписана из стационара. На амбулаторном этапе продолжено введение циклофосфана по 200 мг в сутки 2 раза в неделю, преднизолон в течение месяца полностью отменен.
В течение нескольких месяцев получала поддерживающую терапию циклофосфаном по 200 мг в сутки 2 раза в неделю (суммарная доза составила 7200 мг). На этом фоне уровень гемоглобина стабилен в пределах 100–120 г/л, количество ретикулоцитов не превышает 20%.
Комментарий к клиническому случаю
Аутоиммунная гемолитическая анемия (АИГА) – гетерогенная группа заболеваний и синдромов, обусловленных повышенным разрушением эритроцитов вследствие образования аутоантител. Частота АИГА во всех возрастных группах составляет 1:40000 – 1:80000, причем женщины болеют в 2 раза чаще мужчин. Выделяют первичные (идиопатические) и вторичные АИГА, которые чаще всего развиваются при лимфомах, солидных опухолях и заболеваниях соединительной ткани. По серологическим свойствам различают АИГА с тепловыми (85%) и холодовыми (15%) антителами; по месту разрушения эритроцитов выделяют АИГА с внутриклеточным (наиболее частым), внутрисосудистым и смешанным гемолизом.
Клинические проявления АИГА:
При внутрисосудистом гемолизе моча приобретает темно-бурую или черную окраску.
Лабораторные критерии:
Стандарт первой линии терапии АИГА – пероральные глюкокортикостероиды в начальной дозе 1 мг/кг в сутки, возможно проведение пульс-терапии метилпреднизолоном в дозе 0,5–1,0 г/сутки внутривенно в течение 3-5 дней. Второй линией терапии является спленэктомия, которая используется при отсутствии эффекта глюкокортикостероидов в течение 4–6 месяцев. У пожилых пациентов показано назначение иммунодепрессивных и цитостатических препаратов (азатипоприн, циклофосфон, циклоспорин). Значительно реже используют моноклональные антитела (ритуксимаб) и иммуноглобулин. Выживаемость больных АИГА в течение 5 лет составляет 75%.
При анализе данного случая обращает внимание длительное латентное течение заболевания у больной преклонного возраста с гиперхромной анемией, что послужило причиной ошибочного диагноза B12–дефицитной анемии (для АИГА характерен нормохромный характер анемии). С учетом возраста пациентки и наличия сопутствующих заболеваний было принято решение о подключении к лечению цитостатической терапии, позволившее получить ремиссию заболевания, отменить глюкокортикостероиды и отказаться от проведения спленэктомии.
