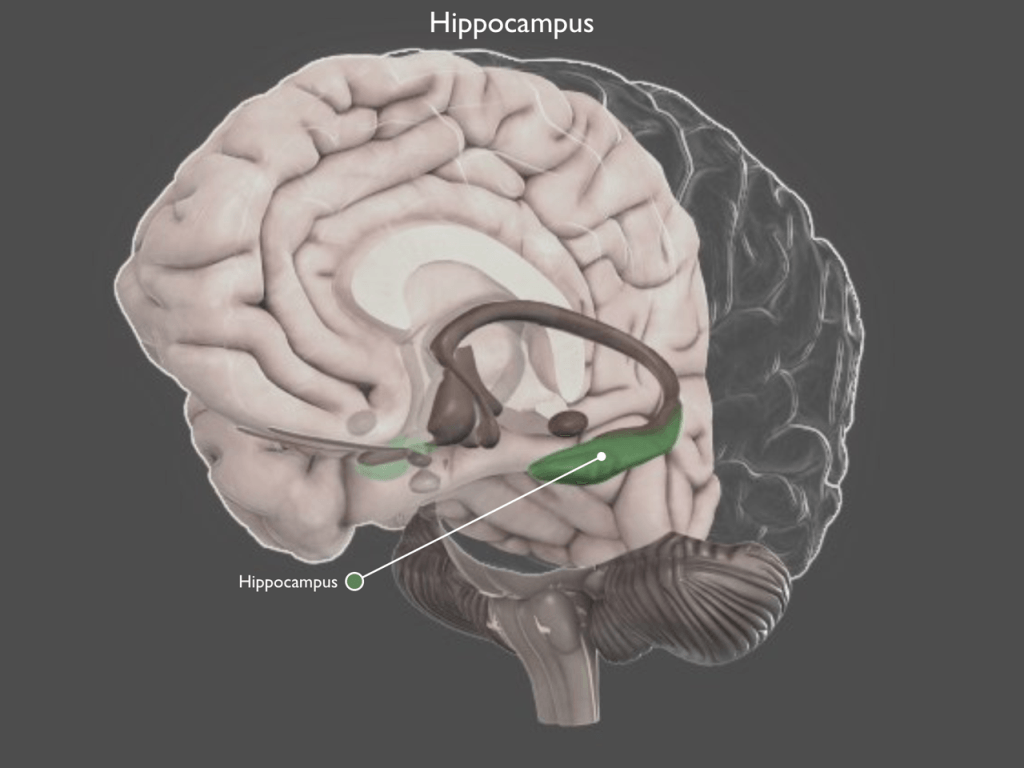
Гидроцефалия головного мозга на МРТ
Магнитно-резонансная томография (МРТ) – самый информативный и безопасный метод визуальной диагностики, позволяющий:
диагностировать гидроцефалию головного мозга (водянку);
оценить степень выраженности нарушений;
предположить источник проблемы и выбрать тактику лечения.
Введение контраста: по врачебным показаниям.
Подготовка к обследованию: нет.
Подготовка заключения: в течение часа или можно получить по почте.
Ограничения: вес свыше 250 кг
Стоимость: 4 500 рублей
В клинике СОЮЗ исследование выполняется на современном аппарате экспертного класса, поддерживающем продвинутые режимы сканирования. Благодаря этому, изображения полостей (желудочков) мозга и субарахноидального пространства получаются отчетливыми даже в тех случаях, когда визуализация затруднена (например, у больных с краниопластикой) или если в момент выполнения снимка пациент случайно слегка пошевелился.
Кроме того, на нашем томографе можно проводить исследование головного мозга при подозрении на гидроцефалию больным с весом до 250 кг. Для сравнения: высокопольные томографы предыдущего поколения, установленные в большинстве столичных медицинских центров, рассчитаны на пациентов весом не более 150 кг.
Мы также принимаем на обследование людей с кардиостимуляторами при условии, что имплантированное устройство поддерживает возможность настройки в специальный режим на время проведения МРТ.
Гидроцефалия головного мозга у взрослых: понятие, причины, симптомы, важность своевременной диагностики
В головном мозге постоянно присутствует спинномозговая жидкость – ликвор. Она заполняет желудочки мозга и соединяющие их протоки, субарахноидальное пространство. Ликвор выполняет защитную функцию, нивелируя механические воздействия на полушария, гипофиз и прочие связанные с мозгом структуры, а также являясь иммунобиологическим «барьером», препятствующим поступлению в ткани головного мозга токсинов, микроорганизмов, вирусов.
Кроме того, омывающая головной мозг жидкость, постоянно циркулирующая по его полостям, участвует в обменных процессах, поддерживая электролитный и кислотно-щелочной баланс.
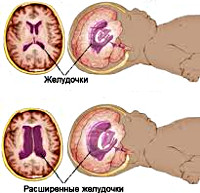
Однако если по каким-либо причинам количество жидкости увеличивается, у человека развивается гидроцефалия. При этом полости головного мозга расширяются, что отчетливо видно на МРТ.
МРТ-картинка гидроцефалии в норме
МРТ-картина гидроцефалии – расширения желудочков мозга из-за скопления жидкости
Гидроцефалия у взрослых людей может быть следствием:
Проявления гидроцефалии у взрослых на МРТ
Если у грудных детей прогрессирующая гидроцефалия вызывает быстрое увеличение размеров головы, то для взрослых людей, у которых кости черепа полностью сформировались и прочно «спаяны» между собой, такой симптом не характерен. Гидроцефалия у взрослых может проявляться:
распирающими головными болями, наиболее выраженными по утрам, часто сопровождающимися тошнотой и рвотой;
скачками артериального давления, недержанием мочи, шаткостью походки, апатией, сонливостью, пеленой перед глазами;
на поздних стадиях – психическими нарушениями вплоть до полной утраты интеллекта и навыков самообслуживания, параличами, потерей сознания, летальным исходом при отсутствии правильного лечения.
Вышеперечисленные и иные симптомы вызваны сдавливанием функциональных зон головного мозга, гипофиза, эпифиза, мозжечка, черепно-мозговых нервов, что вызывает нарушение их нормальной работы. Кроме того, пациента могут беспокоить проявления основного заболевания, приведшего к развитию гидроцефалии.
Важно помнить, что симптомы гидроцефалии проявляются не сразу, а с помощью МР-томографии ее признаки можно выявить на ранних, бессимптомных стадиях. Это позволяет врачу взять ситуацию под контроль и начать своевременное лечение, направленное на предупреждение прогрессирования водянки и ее осложнений.
Следует также добавить, что умеренная компенсаторная гидроцефалия у пожилых людей может ничем себя не проявлять. При медленном прогрессировании процесса такие пациенты не нуждаются ни в операции, ни в специфическом медикаментозном лечении.
МРТ-признаки гидроцефалии
О наличии заболевания может свидетельствовать обнаружение на снимках:
симптома Маусса (расширенные передние рога и тело боковых желудочков),
увеличения расстояния между внутренними костными пластинками (межжелудочковый индекс больше 0,5);
признаков отечности тканей вокруг полостей (перивентрикулярный отек);
ухудшения МР-сигнала в субарахноидальном пространстве и полости заднего желудочка;
повышенной интенсивности сигнала в режиме Т2 и других аномалий.
МРТ-признаки гидроцефалии: желтые стрелки – перивентрикулярный отек, красные – расширенные полости
В клинике СОЮЗ работают опытные рентгенологи, способные определить признаки гидроцефалии на снимках МРТ на самых ранних стадиях процесса, то есть тогда, когда принятие необходимых мер позволяет избежать тяжелых последствий, а в ряде случаев – добиться полного излечения.
Кто направляет на исследование гидроцефалии
На правление на магнитно-резонансную томографию выдает невролог, нейрохирург, эндокринолог, окулист, онколог или врач любой иной специальности, если у него есть основания считать, что имеющиеся у пациента заболевания головного мозга, обменные нарушения и другие проблемы могут сопровождаться гидроцефалией.
Особенности процедуры
Исследование безболезненно, безвредно, имеет минимум противопоказаний, не требует специальной подготовки и вследствие полного отсутствия лучевой нагрузки может проводиться столько раз, сколько это необходимо для постановки точного диагноза и контроля лечения.
Само обследование занимает от 30 минут до 1 часа (при сканировании с контрастом), еще через 1-2 часа вы получите заключение и диск с записью изображений. Результаты также можно записать на пленку или на флэшку.
Причины и виды склероза гиппокампа
Склероз гиппокампа – это одна из форм эпилепсии, причиной которой является патология отделов лимбической системы головного мозга. Основным генератором эпилептической активности считается глиоз в сочетании с атрофией кортикальной пластинки подлежащего белого вещества. Для диагностики заболевания неврологи Юсуповской больницы применяют современные методы инструментального исследования, выполняют лабораторные анализы и малоинвазивные диагностические процедуры.
Склероз гиппокампа сопровождается потерей нейронов и рубцеванием самой глубокой части височной доли. Часто обусловлено серьезными травмами головного мозга. Бывает левосторонним и правосторонним. Повреждение головного мозга вследствие травмы, новообразования, инфекции, недостатка кислорода или неконтролируемых спонтанных припадков приводит к образованию рубцовой ткани гиппокампа. Он начинает атрофироваться, нейроны отмирают и формируют рубцовую ткань.
На основании структурных изменений выделяют два основных вида эпилепсии височной доли:
Причины
Известны следующие причины склероза гиппокампа:
Сегодня основными считаются следующие теории развития склероза гиппокампа:
Симптомы
Склероз гиппокампа обычно приводит к очаговой эпилепсии. Эпилептические припадки появляются в группах или по отдельности. Они бывают комплексными, начинающимися со странных неописуемых ощущений, галлюцинаций или иллюзий с последующим оцепенением взгляда, пищевыми и ротаторными автоматизмами. Продолжаются около двух минут. При прогрессировании могут отмечаться генерализованные тонико-клонические судороги.
Приступы при склерозе гиппокампа могут сопровождаться различными симптомами:
У пациентов развивается нарушение когнитивных способностей (памяти, мышления, способности сконцентрироваться). Припадки, вследствие которых нарушается деятельность мозга, могут приводить к внезапной потере сознания, а также к вегетативной сердечной дисфункции. У пациентов с левосторонним склерозом гиппокампа более серьёзная парасимпатическая дисфункция по сравнению с пациентами, страдающими правосторонним мезиальным склерозом.
Приступы эпилепсии сопровождаются слуховыми или вестибулярными галлюцинациями, отрыжкой или вегетативными проявлениями, парестезиями и односторонними подергиваниями лица. Пациенты отмечают трудность обучения, нарушения памяти. Они конфликтны, эмоционально лабильны, обладают повышенным чувством долга.
Для диагностики заболевания врачи Юсуповской больницы применяют следующие методы обследования:
Исследование выполняют на современной аппаратуре ведущих мировых производителей.
Лечение
Для уменьшения симптомов заболевания неврологи Юсуповской больницы назначают противоэпилептические препараты. Средством первого выбора является Карбамазепин. К препаратам второго выбора относятся Вальпроат, Дифенин и Гексамидин. После лечения у части пациентов прекращаются приступы, наступает продолжительная ремиссия.
При устойчивости к проводимой терапии и прогрессировании склероза гиппокампа хирургическое лечение проводится в клиниках-партнёрах. Оно заключается в удалении височной доли мозга (лобэктомии). После операции в 70-95% случаев уменьшается количество приступов. Если вы столкнулись с проблемой склероза гиппокампа и желаете получить квалифицированную специализированную медицинскую помощь, позвоните по телефону. Вас запишут на консультацию невролога Юсуповской больницы.
Внутричерепная гипертензия — синдром повышенного интракраниального давления. Может быть идиопатическим или развиваться при различных поражениях головного мозга. Клиническая картина складывается из головной боли с давлением на глаза, тошнотой и рвотой, иногда — транзиторными расстройствами зрения; в тяжелых случаях отмечается нарушение сознания. Диагноз выставляется с учетом клинических данных, результатов Эхо-ЭГ, томографических исследований, анализа ликвора, внутрижелудочкового мониторинга ВЧД, УЗДГ церебральных сосудов. Лечение включает мочегонные препараты, этиотропную и симптоматическую терапию. По показаниям проводятся нейрохирургические операции.
МКБ-10
Общие сведения
Внутричерепная гипертензия — синдромологический диагноз, часто встречающийся как во взрослой, так и в детской неврологии. Речь идет о повышении внутричерепного (интракраниального) давления. Поскольку уровень последнего прямо отражается на давлении в ликворной системе, внутричерепная гипертензия также носит название ликворно-гипертензионный синдром или синдром ликворной гипертензии. В большинстве случаев внутричерепная гипертензия является вторичной и развивается вследствие травм головы или различных патологических процессов внутри черепа.
Широко распространена и первичная, идиопатическая, внутричерепная гипертензия, классифицируемая по МКБ-10 как доброкачественная. Она является диагнозом исключения, т. е. устанавливается только после того, как не нашли подтверждения все другие причины повышения интракраниального давления. Кроме того, выделяют острую и хроническую внутричерепную гипертензию. Первая, как правило сопровождает черепно-мозговые травмы и инфекционные процессы, вторая — сосудистые нарушения, медленно растущие внутримозговые опухоли, кисты головного мозга. Хроническая внутричерепная гипертензия зачастую выступает резидуальным следствием острых интракраниальных процессов (травм, инфекций, инсультов, токсических энцефалопатий), а также операций на головном мозге.
Причины и патогенез внутричерепной гипертензии
Повышение интракраниального давления бывает обусловлено целым рядом причин, которые можно разделить на 4 основные группы. Первая — наличие в полости черепа объемного образования (первичной или метастатической опухоли мозга, кисты, гематомы, аневризмы сосудов головного мозга, абсцесса головного мозга). Вторая — отек головного мозга диффузного или локального характера, который развивается на фоне энцефалита, ушиба головного мозга, гипоксии, печеночной энцефалопатии, ишемического инсульта, токсических поражений. Отек не собственно тканей мозга, а церебральных оболочек при менингите и арахноидите также приводит к ликворной гипертензии.
Следующая группа — это причины сосудистого характера, обуславливающие повышенное кровенаполнение мозга. Избыточный объем крови внутри черепа может быть связан с увеличением ее притока (при гипертермии, гиперкапнии) или затруднением ее оттока из полости черепа (при дисциркуляторной энцефалопатии с нарушением венозного оттока). Четвертую группу причин составляют ликвородинамические расстройства, которые в свою очередь бывают вызваны увеличением ликворопродукции, нарушением ликвороциркуляции или понижением абсорбции ликвора (цереброспинальной жидкости). В таких случаях речь идет о гидроцефалии — избыточном скоплении жидкости в черепной коробке.
Причины доброкачественной интракраниальной гипертензии не совсем ясны. Более часто она развивается у женщин и во многих случаях связана с набором массы тела. В связи с этим существует предположение о существенной роли в ее формировании эндокринной перестройки организма. Опыт показал, что к развитию идиопатической внутричерепной гипертензии может приводить избыточное поступление витамина А в организм, прием отдельных фармпрепаратов, отмена кортикостероидов после длительного периода их применения.
Поскольку полость черепа представляет собой ограниченное пространство, любое увеличение размеров находящихся в ней структур влечет за собой подъем интракраниального давления. Результатом является выраженное в различной степени сдавление головного мозга, приводящее к дисметаболическим изменениям в его нейронах. Значительное нарастание внутричерепного давления опасно смещением церебральных структур (дислокационным синдромом) с вклинением миндалин мозжечка в большое затылочное отверстие. При этом происходит компрессия мозгового ствола, влекущая за собой расстройство витальных функций, поскольку в стволе локализуются дыхательный и сердечно-сосудистый нервные центры.
У детей этиофакторами внутричерепной гипертензии могут выступать аномалии развития головного мозга (микроцефалия, врожденная гидроцефалия, артериовенозные мальформации головного мозга), внутричерепная родовая травма, перенесенная внутриутробная инфекция, гипоксия плода, асфиксия новорожденного. В младшем детском возрасте кости черепа более мягкие, а швы между ними эластичны и податливы. Такие особенности способствуют значительной компенсации интракраниальной гипертензии, что обеспечивает ее порой длительное субклиническое течение.
Симптомы внутричерепной гипертензии
Основным клиническим субстратом ликворно-гипертензионного синдрома выступает головная боль. Острая внутричерепная гипертензия сопровождается нарастающей интенсивной головной болью, хроническая — периодически усиливающейся или постоянной. Характерна локализация боли в лобно-теменных областях, ее симметричность и сопутствующее ощущение давления на глазные яблоки. В ряде случаев пациенты описывают головную боль как «распирающую», «изнутри давящую на глаза». Зачастую наряду с головной болью присутствует ощущение подташнивания, болезненность при движениях глазами. При значительном повышении внутричерепного давления возможна тошнота с рвотой.
Быстро нарастающая острая внутричерепная гипертензия, как правило, приводит к тяжелым расстройствам сознания вплоть до комы. Хроническая внутричерепная гипертензия обычно приводит к ухудшению общего состояния пациента — раздражительности, нарушениям сна, психической и физической утомляемости, повышенной метеочувствительности. Может протекать с ликворно-гипертензионными кризами — резкими подъемами интракраниального давления, клинически проявляющимися сильной головной болью, тошнотой и рвотой, иногда — краткосрочной потерей сознания.
Идиопатическая ликворная гипертензия в большинстве случаев сопровождается преходящими расстройствами зрения в виде затуманивания, ухудшения резкости изображения, двоения. Снижение остроты зрения наблюдается примерно у 30% пациентов. Вторичной интракраниальной гипертензии сопутствуют симптомы основного заболевания (общеинфекционные, интоксикационные, общемозговые, очаговые).
Ликворная гипертензия у детей до года манифестирует изменением поведения (беспокойством, плаксивостью, капризностью, отказом от груди), частыми срыгиваниями «фонтаном», глазодвигательными расстройствами, выбуханием родничка. Хроническая интракраниальная гипертензия у детей может стать причиной задержки психического развития с формированием олигофрении.
Диагностика внутричерепной гипертензии
Установка факта повышения интракраниального давления и оценка его степени является непростой задачей для невролога. Дело в том, что внутричерепное давление (ВЧД) существенно колеблется, и клиницисты до сих пор не имеют единого мнения его норме. Считается, что нормальное ВЧД взрослого человека в горизонтальном положении находится в пределах от 70 до 220 мм вод. ст. Кроме того, не существует пока простого и доступного способа точного измерения ВЧД. Эхо-энцефалография позволяет получить лишь ориентировочные данные, правильная интерпретация которых возможна только при сопоставлении с клинической картиной. О повышении ВЧД может свидетельствовать отек зрительных нервов, выявляемый офтальмологом при офтальмоскопии. При длительном существовании ликворно-гипертензионного синдрома на рентгенографии черепа обнаруживаются так называемые «пальцевые вдавления»; у детей могут отмечаться изменение формы и истончение черепных костей.
Достоверно определить внутричерепное давление позволяет только прямое введение иглы в ликворное пространство посредством люмбальной пункции или пункции желудочков мозга. В настоящее время разработаны электронные датчики, но их внутрижелудочковое введение по-прежнему является достаточно инвазивной процедурой и требует создания трепанационного отверстия в черепе. Поэтому подобную аппаратуру используют только нейрохирургические отделения. В тяжелых случаях внутричерепной гипертензии и в ходе нейрохирургических вмешательств она позволяет осуществлять мониторинг ВЧД. С целью диагностики причинной патологии применяют КТ, МСКТ и МРТ головного мозга, нейросонографию через родничок, УЗДГ сосудов головы, исследование цереброспинальной жидкости, стереотаксическую биопсию внутримозговых опухолей.
Лечение внутричерепной гипертензии
Консервативная терапия ликворной гипертензии осуществляется при ее резидуальном или хроническом характере без выраженного прогрессирования, в острых случаях — при медленном нарастании ВЧД, отсутствии данных за дислокационный синдром и серьезных расстройств сознания. Основу лечения составляют мочегонные фармпрепараты. Выбор препарата диктуется уровнем ВЧД. В острых и тяжелых случаях применяется маннитол и другие осмодиуретики, в остальных ситуациях препаратами выбора выступают фуросемид, спиронолактон, ацетазоламид, гидрохлоротиазид. Большинство диуретиков следует применять на фоне введения препаратов калия (калия аспарагината, хлорида калия).
Параллельно проводится лечение причинной патологии. При инфекционно-воспалительных поражениях мозга назначается этиотропная терапия (противовирусные препараты, антибиотики), при токсических — дезинтоксикация, при сосудистых — вазоактивная терапия (аминофиллин, винпоцетин, нифедипин), при венозном застое — венотоники (дигидроэргокристин, экстракт конского каштана, диосмин+гесперидин) и т. п. Для поддержания функционирования нервных клеток в условиях внутричерепной гипертензии в комплексной терапии используют нейрометаболические средства (гамма-аминомасляную кислоту, пирацетам, глицин, гидролизат головного мозга свиньи и др.). С целью улучшения венозного оттока может применяться краниальная мануальная терапия. В остром периоде пациент должен избегать эмоциональных перегрузок, исключить работу за компьютером и прослушивание аудиозаписей в наушниках, резко ограничить просмотр фильмов и чтение книг, а также другие виды деятельности с нагрузкой на зрение.
Хирургическое лечение внутричерепной гипертензии применяется ургентно и планово. В первом случае целью является неотложное снижение ВЧД во избежание развития дислокационного синдрома. В таких ситуациях нейрохирургами зачастую проводится декомпрессионная трепанация черепа, по показаниям — наружное вентрикулярное дренирование. Плановое вмешательство имеет целью устранение причины повышения ВЧД. Оно может заключаться в удалении интракраниального объемного образования, коррекции врожденной аномалии, ликвидации гидроцефалии при помощи церебрального шунтирования (кистоперитонеального, вентрикулоперитонеального).
Прогноз и профилактика внутричерепной гипертензии
Исход ликворно-гипертензионного синдрома зависит от основной патологии, скорости нарастания ВЧД, своевременности терапии, компенсаторных способностей мозга. При развитии дислокационного синдрома возможен летальный исход. Идиопатическая внутричерепная гипертензия имеет доброкачественное течение и обычно хорошо поддается лечению. Длительная ликворная гипертензия у детей может привести к задержке нервно-психического развития с формированием дебильности или имбецильности.
Предупредить развитие интракраниальной гипертензии позволяет профилактика интракраниальной патологии, своевременное лечение нейроинфекций, дисциркуляторных и ликвородинамических расстройств. К профилактическим мерам можно отнести соблюдение нормального режима дня, нормирование труда; избегание психических перегрузок; адекватное ведение беременности и родов.
Патогенез
Наиболее значимым фактором риска поражения мелких сосудов головного мозга является артериальная гипертензия [23]. При дисциркуляторной энцефалопатии встречаются как первичные сосудистые, так и вторичные дегенеративные изменения вещества головного мозга.
Выделяют несколько видов патологических изменений вещества головного мозга, ассоциированных с хроническим ишемическим повреждением [2,29,42].
Атеросклероз поражает артерии эластического и крупные артерии мышечного типа. В большинстве случаев атеросклероз приводит к развитию острых нарушений мозгового кровообращения с быстрым развитием выраженных очаговых симптомов. В патогенезе хронических сосудистых заболеваний головного мозга основное значение имеет поражение микроциркуляторного русла. Оно образовано терминальными ветвями крупных артерий каротидного и вертебрально-базилярного бассейна, а также притоками церебральных вен. Артерии микроциркуляторного русла подвержены изменениями при резких перепадах артериального давления поскольку на этом уровне не образуются анастомозы.
Болезнь мелких сосудов или микроангиопатия может иметь различной этиологии:
В ряде случаев, нарушения микроциркуляции могут быть вызваны патологией со стороны системы крови, без поражения кровеносных сосудов. Истинная полицитемия, гемоглобинопатии или протеинопатии могут повышать вязкость крови, что приводит к сопротивлению кровотоку и агрегации форменных элементов, является причиной церебральной ишемии. В редких случаях возможно развитие микроэмболии. Важными дополнительными факторами могут быть нарушения обмена веществ, прежде всего, сахарный диабет и нарушение венозного оттока.
Нарушения ауторегуляции мозгового кровообращения являются как причиной, так и следствием поражения микрососудов, принимая участие в порочном круге патологических изменений.
Лейкоареоз — нейровизуализационный термин (снижение рентгеновской плотности на КТ головного мозга, повышение интенсивности сигнала по данным МРТ в Т2/FLAIR режимах), описывающий неспецифические изменения подкоркового белого вещества головного мозга. Выявляются двусторонние очаговые, иногда сливные изменения. В основе лейкоареоза лежит поражение мелких артерий и артериол вследствие липогиалиноза (также обозначается как артериосклероз) и микроатероматоза [11].
Факторами риска развития лейкоареоза являются возраст, повышенное артериальное давление и сахарный диабет [18]. Повышение внутрижелудочкового давления рассматривается в качестве дополнительного механизма развития лейкоареоза, оно приводит к нарушению микроциркуляции в прилегающих к желудочкам участках головного мозга. У пациентов с нормотензивной гидроцефалией отмечаются распространённые изменения подкоркового белого вещества [21].
Доказана связь распространенности диффузных изменений белого вещества головного мозга с выраженностью депрессии и когнитивных нарушений [9,43].
В препаратах головного мозга лейкоареоз часто сочетается с расширением периваскулярных (Вирхова-Робина) пространств — криблюрами (‘etát criblé’). Этот феномен связывают с повторными эпизодами ишемии и плазматического пропитывания участков ткани, окружающих микрососуды.
Липогиалиноз — дистрофический процесс, поражающий пенетрирующие артерии и артериолы диаметром до 200 мкм. Протекает под действием повышения артериального давления, гипергликемии, а также вследствие возрастных изменений. Повышение тканево-сосудистой проницаемости в субэндотелиальном пространстве сосуда приводит к поступлению туда белков плазмы и адсорбции их на изменённых волокнистых структурах соединительной ткани с последующей преципитацией и образованием белка гиалина. В последующем, гиалин оттесняет и разрушает эластичную мембрану, средняя оболочка истончается, и перфорирующая артерия приобретает вид стекловидной трубочки. Просвет артерии резко сужается, возможно развитие окклюзии.
При развитии липогиалиноза фоне сахарного диабета субэндотелиально часто откладывается не только гиалин, но и липиды. Сосудистая стенка инфильтрируется макрофагами с включениям фагоцитированных липидов — пенистыми клетками. В изменённых тканях происходит отложение фибриноида (сложного вещества, состоящего из белков и полисахаридов, распадающихся коллагеновых волокон, межклеточного вещества и плазмы крови). В неблагоприятных условиях происходит гибель окружающих тканей — фибриноидный некроз. Этот патологических процесс выявляется в артериолах и капиллярах головного мозга, сетчатки и почек часто сочетается с гиалинозом.
Этот патологический процесс, видимо является реактивным феноменом. Он не рассматривается, как ведущая причина гипертонического внутричерепного кровоизлияния, так как в препаратах головного мозга в случаях острого внутричерепного кровоизлияния не обнаруживается на отдалении от гематомы. В лабораторных исследованиях выраженные изменения по типу фибриноидного некроза выявлялись вокруг стереотаксически введенных тромбов в опытах у грызунов, что могло указывать на его реактивное происхождение.
Вследствие нарушения работы ассоциации эндотелиоцит-глиальная клетка (астроцит)-нейрон (»нейроваскулярное звено«) страдают механизмы ауторегуляции мозгового кровотока на уровне капилляров и микроартериол. Это приводит к сужению диапазона допустимых показателей перфузии. Из-за того, что мелкие сосуды утрачивают способность расширяться, становится невозможным перераспределение кровотока в пользу активно работающих отделов мозга, а это в свою очередь приводит к их функциональной инактивации, а затем – и к необратимому повреждению. Преимущественное поражение белого вещества в перивентрикулярном и глубинных отделах при церебральной гипоперфузии объясняется особым характером их кровоснабжения сосудами терминального типа, не имеющими коллатералей.
Клетки нервной ткани различаются по чувствительности к ишемии. При нарушении кровотока, некротические изменения развиваются сначала в нейронах, затем олигодендроцитах, миелинизированных аксонах, астроцитах и наконец в эндотелиальных клетках [38]. После гибели наиболее чувствительных типов клеток — нейронов и олигодендроцитов, относительно резистентные к ишемии астроциты, выполняющие в головном мозге опорную функцию, замещают дефект за счёт увеличения в объёме своих отростков. Формируется глиальный рубец (»неполный» инфаркт») [33]. При тотальной гибели всех элементов участка мозговой ткани формируется участок некроза (лакуна), на периферии регенерация глиальных клеток формирует его «оболочку».
В патологоанатомических исследованиях отмечена связь липогиалиноза мелких артерий с лакунарными инфарктами головного мозга. Указывается на более высокую распространённость расширенных периваскулярных пространств у пациентов с сосудистой деменцией, чем у пациентов с болезнью Альцгеймера [30]. У здоровых пожилых пациентов с выявленными расширенными периваскулярными пространствами отмечались худшие результаты тестирования когнитивных функций.
Микроатероматоз — атеросклеротическое поражение артериол, приводит к развитию более крупных лакунарных инфарктов. В зависимости от локализации, инфаркты могут проявляться клиникой инсульта, но чаще (примерно в 80 % случаев) протекают субклинически (»немые» инфаркты)[40]. У части пациентов основные патологические процессы вызываются церебральной амилоидной ангиопатией (ЦАА) — отложением амилоидных пептидов (прежде всего Аβ — амилоида) в мышечной оболочке и адвентиции микрососудов и сосудов среднего калибра, значительно реже в стенках капилляров и вен.
Частота выявления амилоидоза церебральных артерий на аутопсии с возрастом увеличивается: на основании серии из 784 аутопсийных материалов, признаки умеренной и тяжёлой ЦАА встречались с частотой 2.3% в возрасте от 65 до 74 лет, 8.0% в возрасте от 75 до 84 лет, и 12.1% в возрасте старше 85 лет [14].
Значимых половых различий во встречаемости амилоидоза не выявлено. Несмотря на то, что вопрос связи ЦАА с артериальной гипертензией продолжает обсуждаться, очевидно, что в большом количестве случаев у пациентов при жизни отмечалось нормальное артериальное давление[3].
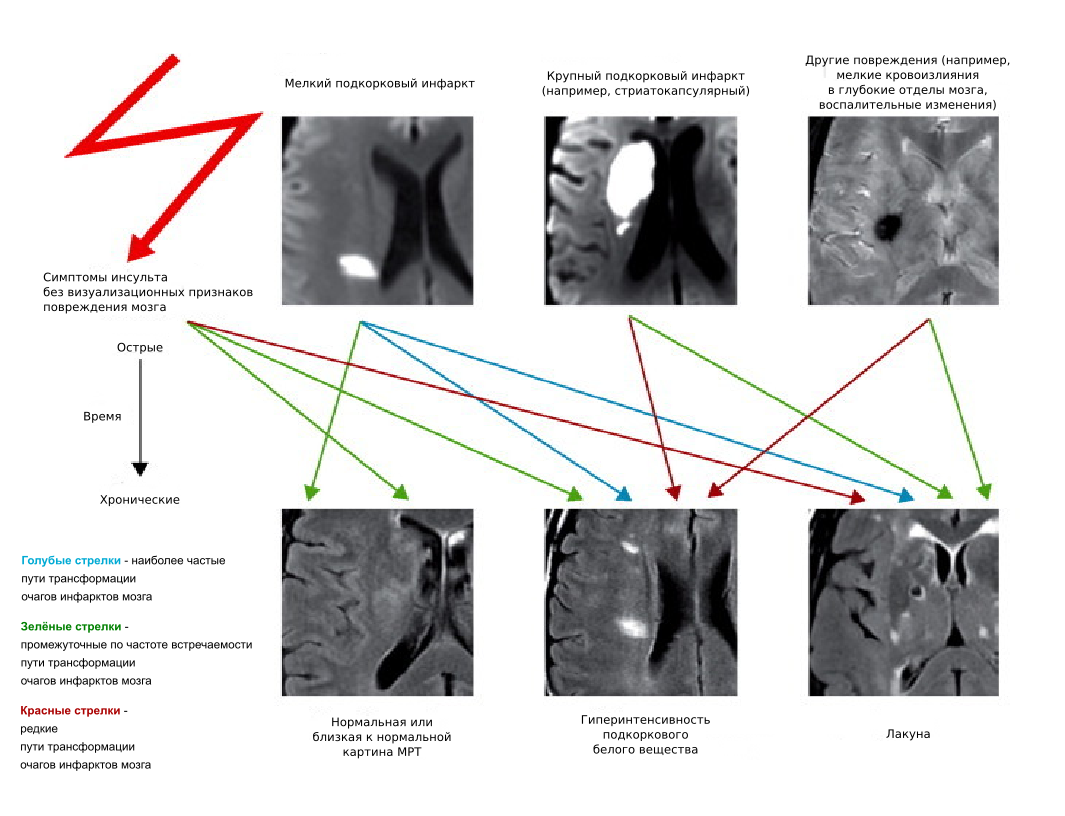
Рисунок 1. Пути трансформации мелких сосудистых очагов и сходство МРТ картины отдалённых последствий поражения мозга различной природы
Предполагается, что амилоидные пептиды, блокируют отток по переваскулярным пространствам, выполняющим в головном мозге дренажную функцию. Повышение ломкости стенки сосудов при отложении амилоида значительно увеличивает риск внутримозговых кровоизлияний. Они, как правило, имеют небольшие размеры и располагаются кнаружи от внутренней капсулы, в белом веществе больших полушарий, для сравнения, гипертонические кровоизлияния поражают преимущественно область подкорковых ядер. В связи с таким расположением микрокровоизлияний при ЦАА, подкорковые структуры остаются относительно интактными, поэтому, экстрапирамидные симптомы не характерны для клиники этого состояния. По данным Фрамингемского исследования установлена связь деменции и внутримозговых микрокровоизлияний, которая не зависела от выраженности других сердечно-сосудистых факторов риска. Наличие ЦАА предполагается у пациентов старше 55–60 лет с множественными лобарными кровоизлияниями без другой явной причины.
Бостонские критерии для кровоизлияний, связанных с церебральной амилоидной ангиопатией [19]
* приём варфарина с превышением целевого значения МНО (> 3,0), перенесённые инсульты и черепно-мозговые травмы, опухоли головного мозга, сосудистые аномалии и васкулиты, патология системы крови, коагулопатии [41].
У пациентов с подозрением на церебральную амилоидную ангиопатию, развитие острых и транзиторных неврологических нарушений может быть связано с геморрагическими осложнениями, что стоит принимать во внимание при планировании их обследования.
У пациентов с выраженным лейкоареозом и множественными лакунарными инфарктами в отсутствии факторов риска сосудистых заболеваний стоит предположить наличие церебральной аутосомно-доминантной артериопатии с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL) — наследственного заболевания, вызванного мутацией гена Notch 3 на 19-й хромосоме. У трети пациентов, страдающих этим заболеванием, отмечается мигрень с аурой, которая рассматривается как раннее проявление заболевания. Приблизительно у 75% лиц, носителей мутации, в конечном счёте развивается деменция[27].
Таким образом, хронические сосудистые поражения головного мозга определяются большим количеством факторов риска, как генетических, так и средовых. Профиль факторов риска развития дисциркуляторной энцефалопатии и инсульта не тождественны. Поражение артерий мозга может быть и изолированным — встречается у пациентов без поражения прецеребральных артерий и артериальной гипертензии.
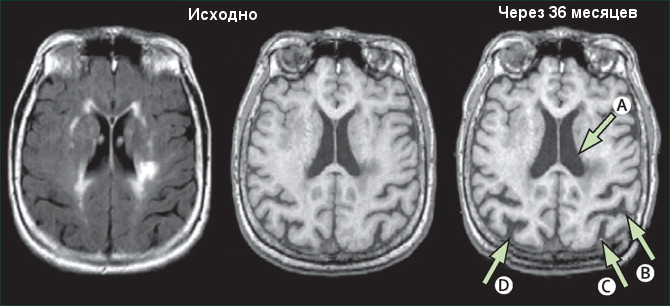
Рисунок 2. Динамика атрофических изменений вещества головного мозга
В патогенезе развития основных симптомов дисциркуляторной энцефалопатии (когнитивных нарушений, нарушений ходьбы, пирамидных и мозжечковых знаков, псевдобульбарного синдрома) лежит разобщение корковых и подкорковых структур вследствие поражения подкоркового белого вещества больших полушарий. Нарушается работа корково-подкорковых кругов, обеспечивающих последовательную избирательную активизацию отдельных участков коры головного мозга при выполнении сложных многоэтапных действий, поддерживающих общий уровень активности коры, несущих информацию для коррекции действий на стадии афферентного синтеза и исполнения (функции I [энергетического] и III [программирование, регуляция и контроль] блоков по А. Р. Лурия).
Клинико-нейровизуализационные соответствия
Термин «энцефалопатия» предполагает наличие не только субъективных жалоб, но и объективных признаков органического поражения мозга, выявляемых при неврологическом или нейропсихологическом исследовании [2]. Вместе с тем, обнаружение подобных признаков, даже вкупе с сосудистыми факторами риска, клиническими или параклиническими признаками цереброваскулярной патологии является необходимым, но недостаточным признаком ДЭП. Важнейшим принципом диагностики ДЭП должна стать констатация причинно-следственной связи между имеющимися у больного клиническими проявлениями и цереброваскулярным заболеванием.
Подобный принцип впервые был заложен в критерии клинической диагностики сосудистой деменции NINDS-AIREN. Представляется, что только следование этому принципу позволит избежать гипердиагностики ДЭП и отделить случаи ДЭП от нейродегенеративных заболеваний, широко представленных у лиц пожилого возраста (в первую очередь от болезни Альцгеймера или болезни Паркинсона, набор симптомов которых на начальных стадиях может соответствовать последствиям хронического сосудистого поражения головного мозга).
Доказательством причинно-следственной связи могут служить:
КТ или МРТ головного мозга при ДЭП могут выявить: двустороннее более или менее симметричное диффузное поражение белого вещества (лейкоареоз) в перивентрикулярной зоне, зрительной лучистости, семиовальном центре; множественные лакунарные очаги (размером 3–15 мм) в базальных ганглиях, таламусе, мосте, мозжечке, внутренней капсуле, белом веществе лобных долей; более крупные корковые и подкорковые инфаркты, отражающие патологию крупных артерий. Церебральная атрофия, выявляемая при КТ или МРТ у больных ДЭП, обычно сопровождает лейкоареоз, лакунарые или территориальные инфаркты [2]. Как правило, расширение желудочковой системы при ДЭП более выражено, чем расширение корковых борозд, и может отражать не только убыль мозгового вещества в глубинных отделах мозга, но и, возможно, снижение резистентности перивентрикулярных тканей к ликвородинамическим воздействиям [2].
В ряде исследований выявлена связь между тяжестью и/или локализацией нейровизуализационных изменений и выраженностью когнитивных и двигательных нарушений [18]. Так, показано, что умеренное когнитивное расстройство возникает, когда распространенность лейкоареоза превышает как минимум 10% белого вещества полушарий, а деменция – если распространенность лейкоареоза превысит 1/4 объема белого вещества полушарий. При наличии лакун выраженность когнитивных нарушений зависит не столько от числа лакунарных очагов, сколько от их локализации (глубинные отделы лобных долей, головка хвостатого ядра и переднее бедро внутренней капсулы, таламус). Выраженность когнитивных нарушений увеличивается при двустороннем поражении указанных структур и сочетании лакунарных очагов с лейкоареозом. Более того, должно быть соответствие между нейровизуализационными изменениями и профилем когнитивных нарушений. Например, в отсутствие соответствующих корковых очагов на КТ и МРТ у пациентов не должны выявляться признаки очагового поражения корковых функций: афазии, апраксии и агнозии. Отмечена также связь между распространенностью лейкоареоза, особенно в передних отделах мозга, локализацией лакунарных очагов в чечевицеобразном ядре и выраженностью нарушений ходьбы и равновесия.
Выраженность когнитивных и двигательных нарушений при ДЭП коррелирует и со степенью расширения боковых желудочков и особенно их передних рогов. С другой стороны, отсутствие сосудистых изменений на МРТ при клинической картине I-III стадий ДЭП и КТ при клинической картине II – III стадий ДЭП может заставлять усомниться в диагнозе. Данные КТ и МРТ имеют значение не только в диагностике ДЭП, но и могут помочь отслеживать динамику заболевания, быть маркером эффективности мер по коррекции факторов риска сердечно-сосудистых осложнений [2]. Отдельные нейровизуализационные феномены считаются нормальным проявлением старения: [12,42]