управление мозгом через магнитные наночастицы субстанции
Вакцина от Covid доставляет Наночастицы для контроля над разумом человека
Это никогда не было «вакциной» против вируса.
Это секретный нанотехнологический проект, разработан для того, чтобы захватить и контролировать мозг человеческой популяции.
Биолог Рикардо Дельгадо и врач, доктор Хосе Луис Севильяно, ведущие онлайн-программы под названием «La Quinta Columna» говорят, что руки некоторых людей становятся магнитными именно в том месте, где им сделали прививку. В этих местах прилипают не только магниты, но и ножницы, металлические детали, инструменты, даже мобильные телефоны!
Это явление не является исключительным для руки. В течение нескольких дней оно перемещается в сторону груди, шеи или верхней части позвоночника.
Они начали свои собственные исследования и обнаружили следующее:
1. Все вакцины производятся с использованием одной и той же нанотехнологии. В Испании его даже описывали как «секретные наночастицы». Эти наночастицы становятся магнитными, когда они достигают той же температуры, что и человеческое тело. Когда они остаются в среде с температурой ниже нуля градусов, они остаются немагнитными. [Почему они замораживают вакцины?]
2. Эти частицы должны быть нанотехнологичным материалом, называемым ГРАФЕНОМ. который является сверхпроводящим и высокоинтегрированным с нейронами клеток головного мозга: Ссылка
3. Европейский союз инвестировал один миллиард евро в проект под названием Флагман графена: Ссылка
4. Частицы ГРАФЕНА могут взаимодействовать с нейронами мозга в удаленном режиме, используя различные радиочастоты (5G могут быть одним из них), они могут отображать мозг и передавать и получать ИНСТРУКЦИИ удаленно: Ссылка
5. Это никогда не были «вакцины» против вируса, вместо этого все время это был секретный нанотехнологический проект, разработанный для достижения и контроля мозга человеческой популяции (до сих пор мы не знаем, могут ли они модифицировать ДНК с помощью 5G). В la Quinta Columna они обнаружили, что люди уже были намагничены с помощью графена присутствующего в масках, ПЦР-тестах, химтрэйлах и вакцинах против гриппа и covid
7. ГРАФЕН может естественным образом выводиться из организма, потому что существует фермент, называемый миелопероксидазой который, по-видимому, расщепляет молекулы графена. Удивительно, но потребление алкоголя или даже табака может помочь увеличить этот фермент. Вот почему они хотят, чтобы население вакцинировалось каждые 6-12 месяцев и было трезвым.
8. Взаимодействие между ГРАФЕНОМ у привитых людей и 5G может привести к летальному исходу, когда 5G будет полностью активирован в 2021, поэтому нам хотелось бы за короткий промежуток времени остановить это безумие и отменить программы вакцинации раз и навсегда.
9. Спикеры Graphene Flagship учитывают указания AstraZeneca, они находятся в очень тесном контакте с крупными фармацевтическими компаниями: «Университет Манчестера представит обзор графена и его использования в биомедицинских устройствах, а представители AstraZeneca, Glaxo Smith Kline, Pixtium Vision, Clinatec и Multichannel Systems расскажут о том, как завершаются эти передовые исследования в отрасли и о пути их продвижения». Ссылка
10. Компания Nanografi, базирующаяся в Турции, производит новую назальную версию вакцины covid для распыления непосредственно в нос (легко проникает в мозг). Они также участвуют в нанотехнологиях использующих графен.
11. ЕС инвестирует 2000 миллионов евро в исследования графена и восстановление человеческого мозга, Испания-страна с большим количеством рабочих групп.
12. Б. Гейтс профинансировал Имперский колледж Лондона на исследования о графене в технологии вакцин на сумму 4,5 миллиона фунтов стерлингов.
13. Майкл Л. Гордон, специалист по национальной безопасности из Wall Street Journal, который публично осудил «оружие массового поражения» (т.н. «белый порошок в пробирке») в Ираке, был тем же журналистом, который рассказал историю о китайском происхождении нового коронавируса в Ухане. «
Российские ученые научились управлять наночастицами в теле человека
МОСКВА, 2 ноя — РИА Новости. Исследователи из Балтийского федерального университета имени Иммануила Канта совместно с коллегами из Уральского федерального университета и Института электрофизики Уральского отделения РАН подтвердили возможность использования наночастиц оксидов железа в магнитном биодетектировании. Статья о проведенном исследовании опубликована в Journal of Magnetism and Magnetic Materials.
Магнитное биодетектирование — мультидисциплинарная область знаний на стыке физики, химии, материаловедения, нанотехнологий и медицины, призванная определять состояние организма по особенностям его отклика на приложение внешнего магнитного поля. Сами по себе ткани и жидкости живой системы обладают очень слабыми откликами на данное поле. Поэтому для биодетектирования необходимо вносить в организм магнитные метки — частицы, которые будут так или иначе реагировать на внешнее поле. Конечно, эти частицы должны быть безопасными для живых тканей и обладать малым размером, в пределах наномасштабов.
Устройство, с помощью которого осуществляется биодетектирование, называется биосенсором. Оно позволяет осуществлять сбор и хранение информации о биосистеме (в частности, о человеческом организме или его части) в автоматическом режиме. Даже не имеющий специальной медицинской подготовки человек может контролировать состояние и управлять различными биологическими системами, используя биосенсор.
В составе магнитного биосенсора работают как минимум два магнитных материала: сенсорный элемент, детектирующий слабые поля, а также наночастицы. Изменение магнитного поля в таком биосенсоре преобразуется в изменение частоты, тока или напряжения.
Использующиеся в биосенсоре магнитные наночастицы способны проникать в клетки избирательно. Например, только в раковые клетки, что позволяет диагностировать наличие и местоположение опухоли. Наночастицы эффективны и при лечении рака — переменное электромагнитное поле в определенных условиях приводит к быстрому разогреву наночастиц, находящихся внутри опухолевых клеток, что разрушает метастазы. Даже будучи установленным вне организма (но в зоне, максимально приближенной к опухоли), сенсор поля при внутривенном введении магнитных наночастиц дает возможность по силе сигнала точно определить момент, когда начать нагрев и уменьшить риск введения избыточного количества наночастиц в организм.
При этом специалисты отмечают: наночастицы, состоящие в ансамбле, несколько отличаются друг от друга по размеру, форме, особенностям поверхности. Следовательно, возникают различия в свойствах частиц (например, изменяется магнитный отклик), что может отразиться на качестве исследований. Самые малые отклонения параметров обеспечиваются только в пределах единовременно изготовленной партии. Потому для практических приложений важны новые способы, обеспечивающие получение больших партий одинаковых по свойствам магнитных наночастиц. Таким является метод лазерного испарения мишени для получения наночастиц из оксида железа, разработанный в Институте электрофизики Уральского отделения РАН.
Из полученных материалов в Уральском федеральном университете были созданы стабильные феррожидкости. Так называются системы, состоящие из воды или иного органического растворителя и крохотных частиц железосодержащего металла. При воздействии магнитного поля они меняют форму. В Балтийском федеральном университете имени Иммануила Канта in vitro (то есть вне живого организма, «в пробирке») исследовали феррожидкости с заданной концентрацией железа и клетки человека, полученные из жировой ткани. Эксперименты показали отсутствие повреждений живой ткани используемыми частицами.
Прямо в мозг: препятствия и способы их преодолеть
Введение наночастиц в носовую полость мыши для изучения транспорта веществ в мозг в обход гематоэнцефалического барьера.
рисунок автора статьи
Авторы
Редакторы
Статья на конкурс «Био/Мол/Текст»: В ходе работы мы выяснили механизм проникновения наночастиц из носовой полости в мозг, минуя гематоэнцефалический барьер (ГЭБ). Для этого были использованы наночастицы оксида марганца (Mn3O4), которые визуализировались при томографии. На данный момент описано несколько возможных путей транспорта веществ из носовой полости в мозг, но точный механизм еще не определен. Чтобы увидеть, как именно наночастицы проникают в мозг, проводились серии экспериментов по блокированию захвата/транспорта наночастиц в нейронах; проверялась и гипотеза транспорта по внеклеточному пространству. Актуальность данной работы — выявление путей доставки лекарственных препаратов и изучение проникновения вирусов в мозг в обход ГЭБ.
Конкурс «Био/Мол/Текст»-2020/2021

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение
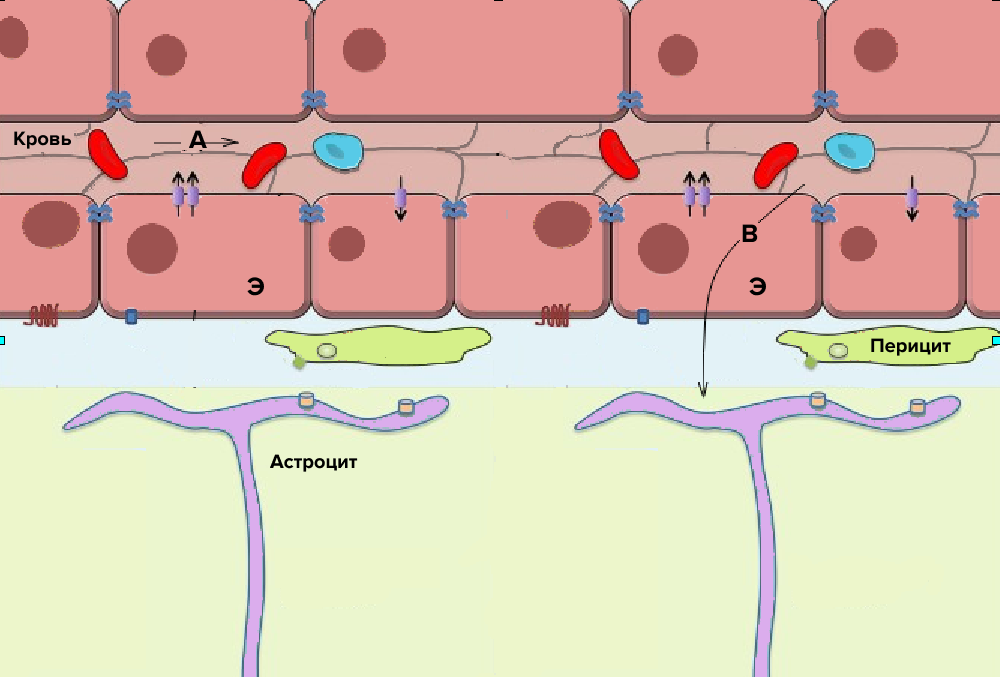
В организме человека существует специальная система защиты мозга от проникновения в него крупных молекул, в том числе инфекционных агентов — это гематоэнцефалический барьер (ГЭБ). Давайте подробнее рассмотрим его структуру (рис. 1). Первая линия защиты — плотный стой эндотелия капилляров, соединенных плотными контактами. В отличие от большинства капилляров тела, в них нет крупных щелей (пор) для прохождения некоторых белков плазмы [1]. Далее на пути к мозгу находятся перициты (клетки соединительной ткани) и астроциты (вспомогательные клетки в нервной ткани), которые механически не позволяют пройти молекулам крупнее определенного размера. Гематоэнцефалический барьер не пропускает вещества более 400–500 Да по массе, в зависимости от свойства вещества. (Для сравнения, сывороточный альбумин человека, самый распространенный белок в крови, имеет массу 65 000 Да). Также барьер непроницаем для ионов, но пропускает жирорастворимые вещества, воду, кислород, углекислый газ, некоторые обезболивающие и алкоголь (рис. 1).
Рисунок 1. Схема строения гематоэнцефалического барьера.
Э — клетки капилляров, соединенные плотными контактами; A — вещества, не проникающие через ГЭБ; B — вещества, проникающие через ГЭБ каким-либо способом, описанным ниже. Стрелками обозначены белковые системы транспорта веществ внутрь клетки и из нее.
рисунок автора статьи
Таким образом, долгое время считалось, что мозг полностью защищен от проникновения некоторых веществ из крови, пока не было обнаружено возможности прохода через ГЭБ. Такой способ доставки нужен прежде всего для доставки лекарств в нервную систему, поэтому было важно найти способы преодолеть барьер: ослабить клеточные контакты эндотелия (клеточного слоя) капилляров мозга, использовать системы транспорта веществ через мембрану капилляров или проникнуть в мозг с помощью эндоцитоза [2]. У данных способов есть свои недостатки, например, разрушение плотных контактов эндотелия приводило к местному накоплению веществ в мозге, повышению внутричерепного давления и требовало значительного времени на восстановление барьера [3]. Использование систем транспорта растворимых в воде метаболитов для доставки действующего вещества в мозг накладывает ограничения на само вещество. В данном случае оно должно либо имитировать «привычный» для данного белка-транспортера метаболит клетки, либо связываться с метаболитом для прохождения через мембрану [4]. Транспорт веществ путем эндоцитоза (захвата внешнего материала) клетками эндотелия тоже имеет свои недостатки — неспецифический эндоцитоз сведен к минимуму в капиллярах мозга, а специфический эндоцитоз часто включает в себя частичное пропускание вещества. Например, при доставке ионов железа посредством белка ферритином этот белок связывается с рецептором на эндотелии капилляра, проникает в клетку, высвобождает ионы железа для их дальнейшего транспорта в мозг, а потом удаляется из клетки обратно в просвет капилляра [5]. У всех перечисленных выше способов есть общий нюанс — вещество попадает в мозг через кровь, а значит, вещество распределяется равномерно по всему организму, поэтому нужно учитывать его системный эффект. Это накладывает дополнительные ограничения и увеличивает время испытания нового лекарства. В последние десятилетия ученые пытались преодолеть барьер и доставить лекарства с помощью наночастиц, введенных в кровь [6–8].
Наночастицы — собирательное название для группы веществ размером от 1 до 1000 нм. Они могут иметь различаться по форме и своим свойствам, в зависимости от пути преодоления ГЭБа. Это могут быть различные полимеры, натуральные или синтетические, или металлические частицы. Однако пока что наночастицы показывают не лучшие результаты в качестве транспортеров лекарств через барьер, если их вводить в кровь, а способ их проникновения через барьер — все еще спорный вопрос [9]. Как отметил Франческо Элдро, было потрачено много времени на изменение (модификацию) действующих веществ в составе лекарств для преодоления барьера, но гораздо меньше изучали способы их проникновения в мозг [10], [11].
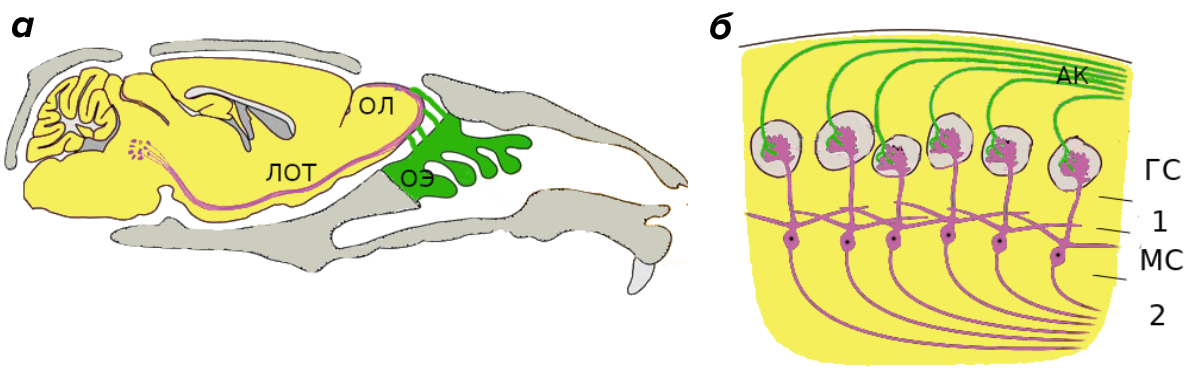
Существуют способы проникнуть в нервную систему, даже минуя стадию попадания в кровь. Конечно, можно просверлить отверстие в черепе и ввести вещество иглой через барьер — это довольно эффективный способ преодолеть ГЭБ. Единственный недостаток в том, что введенное вещество практически не распространяется по мозгу [12]. Но есть и гораздо менее инвазивный вариант — проникнуть в мозг через носовую полость в обход ГЭБа. Рассмотрим, почему этот способ вызывает особый интерес у ученых. Вспомним строение обонятельной системы позвоночных на примере мыши (рис. 2). В носовой полости есть специальный участок скопления рецепторных окончаний нейронов — обонятельный эпителий. От дендритов сигнал проходит через тело, транспортируется по аксону и передается митральной клетке, входящей в состав обонятельной луковицы; место передачи называется синапсом.
Рисунок 2. Строение обонятельной системы.
(a) — строение обонятельной системы мыши в разрезе. ОЭ — обонятельный эпителий, ОЛ — обонятельная луковица, ЛОТ — латеральный обонятельный тракт.
(б) — cтроение обонятельной луковицы мыши. АК) — аксоны обонятельных рецепторов, ГС — гломерулярный слой, МС — митральный слой, 1 и 2 — внешний и внутренний плексиформные слои обонятельной луковицы.
рисунок автора статьи
Тела митральных клеток образуют митральный слой, а аксоны этих клеток формируют латеральный обонятельный тракт. По нему передается информация о запахах в центры головного мозга, которые обрабатывают сигнал. Из-за «доступности» такого способа попадания в мозг, который вдобавок не требует серьезных ограничений по структуре и размерам веществ, данная тема требует более подробного анализа.
Данная работа посвящена изучению процесса проникновения наночастиц в головной мозг через носовую полость. Этот путь актуален не только с точки зрения доставки лекарственных препаратов, но и с точки зрения изучения процесса проникновения вирусов в головной мозг. У всех сейчас на слуху специфический симптом коронавирусной инфекции — потеря обоняния, что свидетельствует о возможности неспецифического проникновения любого вещества в нашу нервную систему.
Описание эксперимента и результаты
Для более точной визуализации транспорта веществ в мозг через носовую полость мы использовали наночастицы оксида марганца (Mn3O4, диаметр
34 нм). Введя их в одну ноздрю мыши, можно увидеть положение наночастиц при томографии (рис. 3).
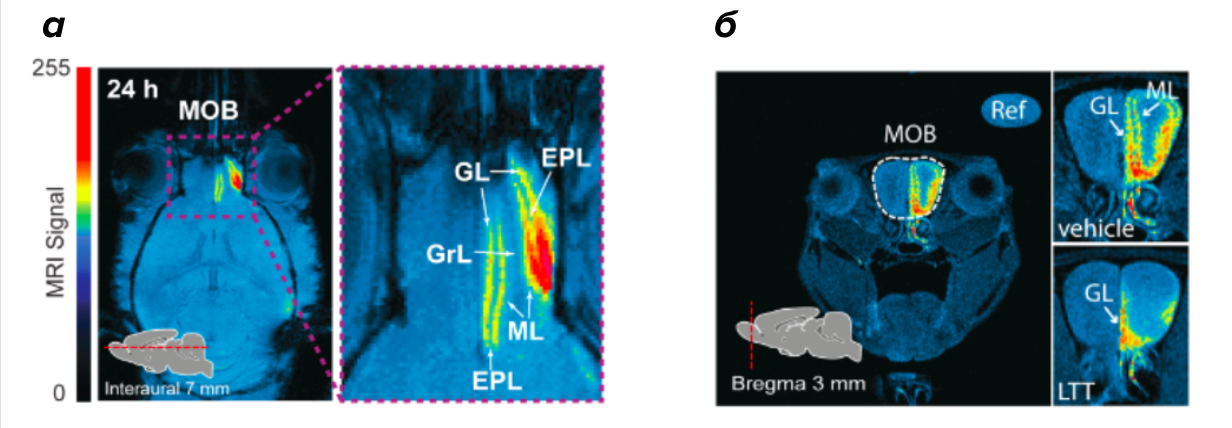
Рисунок 3. Томограмма обонятельной луковицы мыши.
(a) — распределение МРТ сигнала по слоям обонятельной луковицы (MOB): гломерулярному слою (GL), наружному плексиформному слою (EPL), слою митральных клеток (ML), слою зернистых клеток (GrL) спустя 24 часа после введения Mn3O4-наночастиц в правую ноздрю. Интенсивность сигнала выделена с помощью псевдоокрашивания (компьютер окрашивает изображение в различные цвета в зависимости от интенсивности МРТ-сигнала).
(б) — снимок в присутствии (LTT) и отсутствии (vehicle) ингибитора пресинаптической активности нейрона. Белыми стрелками показаны слои: гломерулярный слой (GL) и слой митральных клеток (ML).
рисунок автора статьи
В ходе работы было проанализировано влияние различных ингибиторов на захват и транспорт наночастиц в головной мозг мыши для ответа на основной вопрос: наночастицы проходят из носовой полости по нейронам или они попадают в нервную систему через внеклеточное пространство [13].
Чтобы проследить путь наночастиц из обонятельного эпителия в обонятельную луковицу, были использованы специфические и неспецифические ингибиторы эндоцитоза, а также вещества, разрушающие плотные контакты клеток обонятельного эпителия. Отличия между ингибиторами эндоцитоза в том, что специфические ингибиторы блокируют захват клетками определенного вещества, а неспецифические снижают общую способность клеток к эндоцитозу. Исходя из полученных данных, мы заключили, что частицы поглощаются клетками ольфакторного эпителия, а не проходят между ними. Также можно сделать вывод, что захват наночастиц происходит без сопряжения с каким-либо веществом, так как специфические ингибиторы эндоцитоза не влияли на уровень МРТ-сигнала.
Чтобы проследить дальнейший путь наночастиц, мы использовали ингибиторы аксонального транспорта (колхицин, лидокаин). Колхицин блокирует перемещение грузов от тела нейронов до синапса; лидокаин подавляет проведение импульсов в нейронах вследствие блокирования натриевых каналов (поэтому наночастицы, попав в нейрон, не могут передаваться дальше в синапс). Оба ингибитора достоверно повлияли на транспорт Mn3O4-наночастиц из носовой полости в мозг. Таким образом, мы показали, что Mn3O4-наночастицы проникают в обонятельную луковицу через аксон, а их транспорт зависит от активности нейрона.
Продолжая двигаться в мозг с наночастицами, мы попадаем во внешний слой обонятельной луковицы. Здесь наночастицы стоят перед выбором: либо идти через синапс в следующий нейрон и дальше транспортироваться по латеральному обонятельному тракту, либо перемещаться через межклеточное пространство.
Понять это возможно посредством влияния блокаторов. Ингибиторы пре- и постсинаптической активности нейронов влияют лишь на стадию транспорта наночастиц из обонятельной луковицы (MOB) в латеральный обонятельный тракт (LOT). Причем значительное влияние оказывают только ингибиторы пресинаптической активности — баклофен и LTT (левитриацетам). Такой эффект появляется из-за того, что наночастицы не работают как нейромедиаторы. Чтобы вызвать у нейрона постсинаптическую активность, вещество должно связаться с рецептором на поверхности нейрона и вызвать появление потенциала действия в нем (передать сигнал дальше по нервной цепочке). Наночастицы не могут связываться со специфическими рецепторами; они попадают в следующий нейрон за счет неспецифического эндоцитоза. Из-за этого ингибиторы постсинаптической активности практически никак не влияют на транспорт наночастиц из обонятельной луковицы в латеральный обонятельный тракт. Поэтому можем сделать вывод: наночастицы передаются транссинаптически по структурам головного мозга, отвечающим за обоняние в обход ГЭБ.
Обсуждение
Таким образом, на примере магнитных наночастиц мы показали, что возможен транспорт частиц из носа в мозг в обход ГЭБ внутри нейрональных клеток. Более того, процесс назального транспорта частиц зависит от активности нейронов. Так как данные наночастицы схожи по размерам и другим физическим свойствам с респираторными вирусами, можно предположить что транспорт вирусов в нервную систему возможен не только путем проникновения через ГЭБ [14]. Таким образом, найденный способ транспорта наночастиц в обход ГЭБ дает основу для исследования передачи вирусных заболеваний этим путем, а также для создания новых противовирусных препаратов. Особой актуальностью обладает исследование транспорта SARS-CoV-2, так как одним из симптомов коронавирусной инфекции является потеря вкуса и обоняния.
Заключение
Итогом работы стало подтверждение гипотезы о том, что наночастицы транспортируются через нейроны в головной мозг, а не через межклеточное пространство. Также мы можем сказать, что они не только захватываются обонятельными рецепторами, но и проходят через синапс в митральную клетку обонятельной луковицы, после чего по латеральному обонятельному тракту транспортируются в головной мозг. Понимание точного механизма транспорта веществ в обход ГЭБ может значительно упростить создание лекарственных препаратов против известных заболеваний — болезни Паркинсона и болезни Альцгеймера, а также поможет расширить представление о способах проникновения вирусов в нервную систему человека.
Глубокая стимуляция мозга с помощью наночастиц
В нейронауке не обойтись без прямого воздействия на мозг. Мы часто видим подопытных мышей или обезьян, из головы которых торчит громоздкая конструкция, и из неё тянется кабель. В медицине, связанной со стимуляцией мозга, картина похожая: врачи вставляют людям электроды, чтобы заставить клетки работать. Это все ещё грубо, неудобно и чревато. Но ситуация скоро изменится: разработан метод, позволяющий безопасно стимулировать скопления клеток в любом месте мозга, включая глубокие зоны. Технология не требует вживления электродов и способна произвести революцию в нейромедицине. Важность разработки пока видна не всем — российские журналисты, пишущие о науке, не обратили на неё должного внимания. Но мы непременно расскажем.
В области изучения мозга и лечения нервной системы идёт борьба за глубину воздействия. Разные методы либо «бьют» по верхним слоям коры, либо ставят перед необходимостью вводить стимуляторы в ткань мозга. Учёные Массачусетского технологического института (MIT) нашли новый способ управлять нервными клетками. Они вызвали активность нейронов в мозге мышей с помощью наночастиц, о чём в марте 2015-го сообщили в журнале Science. Методике придумали название «беспроводная термомагнитная глубокая стимуляция мозга» (wireless magnetothermal deep brain stimulation). Про частицы ни слова, но легко догадаться, что в основе — магниты и тепло. Метод не нуждается в электродах и не использует электричество.
Чтобы оценить его красоту и значение, необходимо взглянуть на ситуацию в этой области исследований.
Не электродом единым
Технологии слежения и управления нервными клетками делятся на два класса: требующие хирургического вмешательства (инвазивные) и не требующие (неинвазивные) такого вмешательства. Первые используют вживление в ткань электродов разных модификаций в зависимости от задач. Так, в медицине все шире применяется «глубокая стимуляция мозга» (Deep brain stimulation, DBS): длинный штырь вводится сверху в голову на 7—8 см, достигая ядер таламуса, куда подаются серии электрических импульсов. Терапию используют для облегчения симптомов болезни Паркинсона, для борьбы с ожирением, и, порой, чтобы вывести человека из состояния минимального сознания.
Другая линия инвазивных методов представлена электродными матрицами, стремящимися не в глубину мозга, а к высокому разрешению сигналов на поверхности. Эти технологии чаще связаны с протезированием. Чтобы человек свободно управлял искусственной конечностью, сигнал следует считывать с максимально возможного числа клеток моторной коры. На системе из 192-х электродов инженеры из Университета Питтсбурга создали механическую «руку» с 10-ю степенями свободы, подчиняющуюся сигналам мозга парализованной женщины. Силой мысли пациентка направляет протез к банке с колой, хватает её механической кистью, подносит ко рту и, выпив содержимое, ставит банку на стол. Движение требует точной координации, и протез её обеспечивает.
В группу неинвазивных входят разные способы считывания электроэнцефалограммы (ЭЭГ) мозга с помощью электродов, прилагаемых к коже. Стимуляция постоянным током также не требует вмешательства — ток в буквальном смысле течёт между двумя электродами, касающимися головы в разных точках. Отметим и технологию транскраниальной магнитной стимуляции (ТМС), где возбуждение и торможение верхних слоёв коры достигается при помощи магнитного поля. Сходных результатов можно добиться, воздействуя на мозг слабым фокусированным ультразвуковым лучом.
Эксперименты по ультразвуковой стимуляции проводились в СССР ещё в 1970-е годы, но потом их оставили, и в наши дни метод возвращается в науку уже силами американцев и европейцев. С помощью ультразвука можно улучшить восприятие человека и даже стимулировать отдельные нервные пути, вызывая соматосенсорные ощущения. Канадские учёные смогли открыть ультразвуком гематоэнцефалический барьер (что важно для доставки лекарств), а австралийские убрали амилоидные бляшки в мозге мышей-моделей синдрома Альцгеймера.
Свет и нанотехнологии решают
Над «старыми» методами возвышается оптогенетика — молодая технология, умеющая стимулировать клетки одного типа, не затронув остальные. К этим клеткам вирус доставляет светочувствительные белки, и затем интересующее место освещают вспышками света. Белки, закрепившиеся на мембране клеток, исполняют роль каналов. При попадании света они пропускают ионы, заставляя нейрон разрядиться. Соседние клетки, не снабжённые каналами, на свет не реагируют.
Так оптогенетика элегантно решила вечную проблему нейрофизиологов — как включать и выключать клетки выбранного типа, ведь в тканях нейроны разных типов часто перемешаны. Все прочие методы не избирательны и действуют в пределах досягаемости на все клетки. Сегодня учёные ставят опыты, невозможные 10 лет назад. Например, путём стимуляции изучают функции нейронов конкретного типа в выбранном месте мозга. Лечение станет прицельным: затронет только нужные группы клеток и только в заданный промежуток времени.
При очевидных плюсах оптогенетики её инвазивность остаётся минусом — чтобы осветить клетки, череп приходится вскрывать. Метод не требует вживления электродов, но свет проникает в ткань лишь на несколько миллиметров. Чтобы стимулировать глубокие слои мозга, нужно тянуть к ним оптоволокно.
Частицы излучают тепло в ответ на действие магнитного поля. С частотой 500 кГц поле меняет знак, что приводит к их нагреванию. Физика процесса основана на магнитном гистерезисе — тепловая энергия выделяется за счёт смены вектора магнитных моментов в наночастицах. Цепь событий выглядит так: включение магнита — нагрев частиц — реакция белков на тепло — разрядка нейрона.
Вся инвазивность сводится к инъекции, что гораздо лучше постоянно вставленного электрода или оптоволоконного кабеля. Что касается наночастиц, медики давно используют их в диагностике. В малых количествах они безопасны и выводятся из организма естественным путём. Слабое магнитное поле также безвредно (нас ежесекундно пронизывают ЭМ поля разной частоты), и для него проницаема любая область мозга. В сумме это означает, что глубокая стимуляция (DBS) в будущем может стать простой и удобной процедурой. Люди смогут включать магнит дома — например, чтобы снизить депрессию.
Дальше — только лучше
Пока нас не унесло в научную фантастику, сделаем ряд оговорок. Термомагнитная стимуляция сейчас в статусе подтверждённой идеи (proof-of-concept). Учёные показали: магнитным полем за счёт переноса тепла от наночастиц можно возбуждать нервные клетки в живом мозге. Чтобы довести идею до технологии, нужно разработать генератор поля для людей. Желательно сократить время отклика нейрона — пока нагревание и передача тепла занимает пять секунд. Для обычных задач терапевтической стимуляции это не играет роли, но в других случаях будет критичным (эпилепсия, интерфейсы).
Проблему можно решить путём создания частиц с более эффективным излучением тепла, что позволит — по словам исследователей — ускорить нагрев в 5—10 раз. Ещё один резерв — прикрепить частицы к мембранам клеток, чтобы их разделяло минимальное расстояние. В эксперименте они плавали во внеклеточном пространстве, и перенос тепла по нему занимал время. Окружение мембраны частицами сократит его ещё в несколько раз.
Наука получает удобный инструмент фундаментальных исследований. Провода не нужны, и ничто не мешает животным двигаться. Опыты со свободным поведением будут проводить в пространстве, куда просто подаётся магнитное поле. Мыши с частицами в мозге внешне неотличимы от обычных, но включение магнита активирует у них нужные участки мозга. Такими экспериментами учёные займутся летом 2015-го.
В планах — создание нескольких видов частиц. Их спроектируют под разные параметры переменных магнитных полей. Частицы можно доставлять к нейронам избирательно, в зависимости от того, какие белки у них на мембране (какие гены экспрессируются). Такой подход позволит неинвазивно управлять клетками разных типов в любом месте мозга, просто меняя параметры поля. Это будет посильнее оптогенетики.
К чему готовиться
Почему об этом стоит думать? Потому что стимуляция обещает стать главным инструментом лечения неврологических болезней, вытеснив лекарства. Ещё одну заманчивую перспективу открывает исследование биологов из Университета Дюка. Они показали, что нейроны могут запускать нейрогенез из присутствующих в мозге стволовых клеток. Иными словами, нервные клетки контролируют производство других нервных клеток. Быть может, врачи смогут восстанавливать и омолаживать нервную ткань, подавая сигналы определённому классу нейронов. В целом будущее нейромедицины лежит в области диалога с нервной системой.
Язык для такого диалога пока не разработан. В ближайшие годы нейробиологи будут исследовать, как кодируется и передаётся информация внутри нейросетей. Благодаря их усилиям появятся новые знания и технологии, и ими затем воспользуется медицина. В первую очередь медицина тех стран, которые готовы инвестировать в фундаментальную и прикладную науку. Граждане тех стран, что не готовы или не могут, будут читать об этом в прессе.