эритроидная гиперплазия костного мозга
Диагностика и лечение хронической аутоиммунной гемолитической анемии
Больная Ш., 80 лет, пенсионерка. Из анамнеза известно, что в течение последних двух лет неоднократно проходила амбулаторное и стационарное лечение по поводу хронической B12–фолиеводефицитной анемии, диагностированной на основании анемического синдрома в сочетании с гиперхромией и макроцитозом эритроцитов. Стернальная пункция, определение уровня витамина B12 и фолиевой кислоты не проводились. Отмечался временный незначительный положительный эффект лечения витамином B12. С конца 2011 года, несмотря на ежемесячное введение витамина B12 в дозе 500γ в сочетании с фолиевой кислотой, стала нарастать анемия (14.02.2012 г. гемоглобин – 54 г/л). Для обследования и лечения госпитализирована в больницу № 40 с диагнозом: B12–фолиеводефицитная анемия тяжелой степени. ИБС. Стенокардия напряжения II ф. к. Гипертоническая болезнь II ст. Желчнокаменная болезнь. Хронический калькулезный холецистит. Мочекаменная болезнь. Конкремент правой почки, простые кисты обеих почек. Полипы желудка.
При поступлении жалобы на выраженную общую слабость, головокружения, головную боль, учащенное сердцебиение, перебои в работе сердца.
При объективном осмотре отмечены субиктеричность кожи и слизистых оболочек, умеренная гепатомегалия (+2 см) и спленомегалия (+ 2 см).
Результаты клинического анализа в динамике представлены в таблице 1.
Таблица 1. Клинические анализы крови пациентки Ш. в динамике
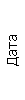 | 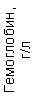 | 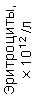 | 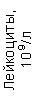 | 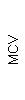 | 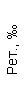 |  | 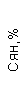 | 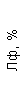 | 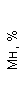 | 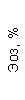 | 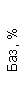 | 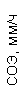 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.02.12 | 54 | 1.39 | 10.5 | 133 | 80 | 2 | 66 | 21 | 9 | 2 | — | 75 |
| 11.03.12 | 50 | 1.41 | 11.8 | 114 | 98 | 4 | 75 | 11 | 4 | 3 | 1 | 78 |
| 15.03.12 | 49 | 1.31 | 17.8 | 121 | 288 | 4* | 60 | 23 | 5 | 1 | — | 78 |
| 20.03.12 | 72 | 1.93 | 11.4 | 116 | 297 | 2 | 73 | 14 | 7 | 2 | 0 | 46 |
| 27.03.12 | 66 | 1.9 | 11 | 108 | 202 | 2 | 60 | 26 | 7 | 3 | 0 | 40 |
| 12.04.12 | 70 | 1.75 | 1.9 | 112 | 104 | 3 | 62 | 24 | 11 | 0 | 0 | 27 |
| 26.04.12 | 93 | 2.56 | 5.7 | 109 | 148 | 3 | 74 | 13 | 9 | 0 | 0 | 11 |
| 24.06.12 | 111 | 3.42 | 4.7 | 97 | 7 | 2 | 69 | 21 | 10 | 0 | 1 | 15 |
| 16.08.12 | 120 | 3.97 | 5.8 | 93 | 12 | — | 71 | 19 | 9 | 1 | 0 | 40 |
Примечание: * в лейкоцитарной формуле 15.03.12 выявлялись также миелоциты (2%) и метамиелоциты (5%).
В биохимическом анализе крови – повышение уровня креатинина (189 ммоль/л), билирубина (58 ммоль/л) за счет непрямого билирубина.
УЗИ органов брюшной полости: гепатоспленомегалия; камни желчного пузыря; диффузные изменения поджелудочной железы; простые кисты обеих почек, конкремент правой почки.
ФГДС: два полипа желудка размером до 0,5 см.
Учитывая высокий риск сердечно-сосудистых осложнений у пожилой пациентки с анемией тяжелой степени, проведены трансфузии эритроцитарной взвеси. На основании клинико-лабораторных данных (спленомегалия, гипербилирубинемия, гиперхромная анемия с ретикулоцитозом) и неэффективности лечения витамином B12 и фолиевой кислотой заподозрена гемолитическая анемия.
При исследовании крови на антиэритроцитарные антитела выявлены аутоантитела класса IgG ++++.
Результаты стернальной пункции представлены в таблице 2.
Таблица 2.Миелограмма пациентки Ш. от 17.02.12 г.
Заключение
Клеточный костномозговой пунктат. Эритропоэз – нормобластический. Гиперплазия эритроидного ростка – 74,8%. Со стороны эритрокариоцитов отмечаются клетки с цитоплазматическими мостиками, скопления в виде «эритроидных островков».
Мегакариоциты различной степени зрелости с умеренным тромбоцитообразованием.
На основании данных миелограммы (гиперплазия эритроидного ростка при нормобластическом типе кроветворения) и выявления антиэритроцитарных антител диагностирована аутоимунная гемолитическая анемия с тепловыми антителами. При дополнительном обследовании признаков вторичного характера анемии не выявлено.
С 11.03.12 г. начата пульс-терапия метипреднизолоном в дозе 500 мг 1 раз в день внутривенно в сочетании с пероральным приемом преднизолона в дозе 45 мг в сутки под прикрытием гастропротекторов. После 5 дней лечения анемический синдром продолжал нарастать, появился выраженный сдвиг лейкоцитарной формулы влево, увеличение количества ретикулоцитов (табл.1). Доза преднизолона перорально увеличена до 75 мг в сутки, к лечению добавлен азатиоприн по 100 мг/сутки per os, проведена трансфузия1 дозы эритроцитарной взвеси.
С 20.03.12 г. с учетом сохраняющегося гемолиза (ретикулоциты 297‰) проведен второй курс пульс-терапии метилпреднизолоном в дозе 500 мг в сутки № 4, однократно введен внутривенно циклофосфан в дозе 600 мг.
Лечение больная переносила хорошо. С 27.03.12 г. отмечена тенденция к увеличению уровня гемоглобина без поддерживающих гемотрансфузий. Решено продолжить введение циклофосфана по 200 мг в сутки, отменить азатиоприн. Анемический синдром продолжал уменьшаться: к 12.04.12 г. уровень гемоглобина достиг 70 г/л, снизился гемолиз (ретикулоцитов 104‰), однако развилась лейкопения (1,9×10 9 /л), в связи с чем циклофосфан был временно отменен. После восстановления количества лейкоцитов лечение циклофосфаном по 200 мг дважды в неделю было возобновлено на фоне постепенного снижения дозы преднизолона.
Больная в удовлетворительном состоянии 28.04.12 г. выписана из стационара. На амбулаторном этапе продолжено введение циклофосфана по 200 мг в сутки 2 раза в неделю, преднизолон в течение месяца полностью отменен.
В течение нескольких месяцев получала поддерживающую терапию циклофосфаном по 200 мг в сутки 2 раза в неделю (суммарная доза составила 7200 мг). На этом фоне уровень гемоглобина стабилен в пределах 100–120 г/л, количество ретикулоцитов не превышает 20%.
Комментарий к клиническому случаю
Аутоиммунная гемолитическая анемия (АИГА) – гетерогенная группа заболеваний и синдромов, обусловленных повышенным разрушением эритроцитов вследствие образования аутоантител. Частота АИГА во всех возрастных группах составляет 1:40000 – 1:80000, причем женщины болеют в 2 раза чаще мужчин. Выделяют первичные (идиопатические) и вторичные АИГА, которые чаще всего развиваются при лимфомах, солидных опухолях и заболеваниях соединительной ткани. По серологическим свойствам различают АИГА с тепловыми (85%) и холодовыми (15%) антителами; по месту разрушения эритроцитов выделяют АИГА с внутриклеточным (наиболее частым), внутрисосудистым и смешанным гемолизом.
Клинические проявления АИГА:
При внутрисосудистом гемолизе моча приобретает темно-бурую или черную окраску.
Лабораторные критерии:
Стандарт первой линии терапии АИГА – пероральные глюкокортикостероиды в начальной дозе 1 мг/кг в сутки, возможно проведение пульс-терапии метилпреднизолоном в дозе 0,5–1,0 г/сутки внутривенно в течение 3-5 дней. Второй линией терапии является спленэктомия, которая используется при отсутствии эффекта глюкокортикостероидов в течение 4–6 месяцев. У пожилых пациентов показано назначение иммунодепрессивных и цитостатических препаратов (азатипоприн, циклофосфон, циклоспорин). Значительно реже используют моноклональные антитела (ритуксимаб) и иммуноглобулин. Выживаемость больных АИГА в течение 5 лет составляет 75%.
При анализе данного случая обращает внимание длительное латентное течение заболевания у больной преклонного возраста с гиперхромной анемией, что послужило причиной ошибочного диагноза B12–дефицитной анемии (для АИГА характерен нормохромный характер анемии). С учетом возраста пациентки и наличия сопутствующих заболеваний было принято решение о подключении к лечению цитостатической терапии, позволившее получить ремиссию заболевания, отменить глюкокортикостероиды и отказаться от проведения спленэктомии.
Эритроидная гиперплазия костного мозга
Согласно классификации ВОЗ (2008 г.), острый эритроидный лейкоз, также называемый эритролейкозом, включает два подтипа: острый эритромиелоидный лейкоз и острый чисто эритроидный лейкоз. При этом первый подтип чаще встречается у взрослых пациентов, а второй подтип в основном наблюдается у пожилых пациентов и характеризуется более низкой выживаемостью [6]. Однако острый чисто эритроидный лейкоз может встречаться и в детском возрасте.
Острый эритромиелоидный лейкоз определяется наличием в костном мозге ≥ 50 % от всей ядерно-клеточной популяции эритроидных предшественников и ≥ 20 % миелобластов от неэритроидной клеточной популяции; острый чисто эритроидный лейкоз представляет неопластическую пролиферацию незрелых клеток, коммитированных исключительно в эритроидную линию (≥ 80 % клеток костного мозга) с отсутствием значимого миелобластического компонента [3].
Эритролейкоз можно рассматривать как многоступенчатую модель лейкемогенеза. На начальных стадиях развития эритролейкоза выделяют несколько основных провоцирующих событий. К ним относятся нарушения, не затрагивающие последовательности ДНК, но приводящие к экспрессии генов, отвечающих за пролиферацию эритроидных клеток; нарушение регуляции микро-РНК; изменения уровня фактора транскрипции, ведущие к остановке дифференцировки и устойчивости к апоптозу среди проэритробластов. В итоге, проэритробласты становятся функционально дефектны, неполноценны, гиперпролиферативны; отмечается накопление мутаций в генах сигнального путь, включая TP53, из-за извращенной клеточной пролиферации, приводящей к лейкемической трансформации дефектных проэритробластов. Последующему поддержанию и размножению лейкозных бластов способствует постоянное присутствие генетических/эпигенетических изменений в уже трансформированных проэритробластах [5].
Острый эритромиелоз характеризуется наличием в костном мозге всех стадий эритроидных предшественников, при этом преобладают наиболее незрелые формы. Выявление подобных изменений требуют проведения дифференциальной диагностики с такой патологией, как гемолитические анемии, пернициозная анемия, а также с любой другой патологией, на фоне которой наблюдается неэффективный эритропоэз.
Морфология ядросодержащих красных клеток при остром эритролейкозе бывает весьма различной: от мало отличающихся от нормальных клеток, до двух- и трехъядерных эритробластов с перекрученными ядрами неправильной формы. Очень часто патологические клетки напоминают мегалобласты пернициозной анемии и лишь отсутствие ретикулоцитарного криза и признаков улучшения в ответ на терапию витамином В12 заставляет усомниться в предполагаемой пернициозной анемии. При остром эритромиелозе нередко может наблюдаться дифференцировка клеток до стадии оксифильного нормоцита и до эритроцита, а не только до проэритробластов.
Следует еще раз подчеркнуть, что морфология бластных клеток при остром эритролейкозе может быть различна. При остром чисто эритроидном лейкозе субстрат опухоли представлен ядросодержащими клетками красного ряда и недифференцируемыми бластами, в то время как при остром эритромиелоидном лейкозе наряду с лейкозными клетками красного ряда встречаются и миелобласты.
Одновременное присутствие в костном мозге и крови эритробластов и их потомства, миелобластов, монобластов и даже мегакариобластов может быть объяснено возникновением данного лейкоза на уровне клетки-предшественницы миелопоэза, которая частично сохраняет способность к дифференцировке по двум или трем направлениям. [1, с. 84-86]
Также при остром эритролейкозе проводится цитогенетическое исследование.
Обычный цитогенетический анализ проводится на метафазных клетках с G-полосой, полученных из аспиратных культур костного мозга, с использованием стандартных методов во время первоначальной диагностики. Наличие или отсутствие моносомного кариотипа, который определялся как включающий по крайней мере две аутосомные моносомии или одну моносомию с дополнительными структурными аномалиями, также используется для стратифицированных случаев [6].
На цитогенетическом уровне в большинстве случаев чисто эритроидный лейкоз имеет сложный кариотип, с частыми аномалиями, включающими хромосомы 5 и 7 случайные гены слияния, вторичные по отношению к хромосомным транслокациям, были описаны в чисто эритроидном лейкозе, такие как t(1;16)(p31;q24)/NFIA‐CBFA2T3 и t(11;20)(p11;q11)/ZMYND8‐RELA [9]. При остром эритроидном лейкозе наблюдается абберантный кариотип. Наиболее часто мутируют TP53, RUNX1, NPM1 и DNMT3A, также могут наблюдаться мутации других генов и белков, но в меньшей степени и не у всех пациентов. Нарушения в генах сильно зависят от возраста, особенно тех генов, которые управляют клональным кроветворением, так, например, мутации чаще наблюдаются у пожилых людей по сравнению с детьми. Высокая частота мутации TP53 способствует объяснению неблагоприятного исхода при остром эритромиелозе, так как именно этот ген отвечает за стабильность генома и за генетическую однородность клеток в целостном организме.
Тактика лечения у пациентов с острым эритромиелозом всегда должна учитывать цитогенетическое исследование и, в будущем, молекулярные мутационные профили с акцентом на NPM1, RUNX1 и TP53 [7].
На сегодняшний день изучение кариотипа пациентов с острым эритролейкозом находится на стадии исследования, а значит до конца еще не ясен механизм развития мутаций, их количество и последствия.
Для идентификации лейкозных бластов при остром эритролейкозе, также как и при других типах лейкоза, используется цитохимическое окрашивание. Некоторые бласты типа М6 (острый эритролейкоз) проявляют PAS-реакцию [4].
Таким образом, на фоне острого эритролейкоза преобладает эритроидная популяция. Появление в крови большого количества эритробластов (до сотен тысяч в 1мм3) наряду с присутствием миелобластов и других молодых клеток белой крови, свидетельствует о наличии особого системного заболевания у человека– эритромиелоза. Исследование костного мозга является наиболее значимым методом диагностики. Метод позволяет выявить все стадии эритроидных предшественников, при этом преобладают наиболее незрелые. Идентификация лейкозных бластов проводится с помощью цитохимического окрашивания, иммунофенотипического анализа. Также возможно цитогенетическое исследование.
Эритроидная гиперплазия костного мозга
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Научно-клиническое отделение гематологической хирургии Гематологического научного центра Минздрава РФ, Москва
Алгоритм исследования трепанобиоптатов костного мозга при миелодиспластических синдромах
Журнал: Архив патологии. 2014;76(1): 50-56
Капланская И. Б., Гласко Е. Н. Алгоритм исследования трепанобиоптатов костного мозга при миелодиспластических синдромах. Архив патологии. 2014;76(1):50-56.
Kaplanskaya I B, Glasko E N. Algorithm for examination of bone marrow trephine biopsy specimens in myelodysplastic syndromes. Arkhiv Patologii. 2014;76(1):50-56.
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
На основании анализа более 1000 трепанобиоптатов костного мозга у больных с миелодиспластическими синдромами до начала какой-либо специфической терапии предложены гистологические критерии их оценки (алгоритм исследования), оптимальная панель иммуногистохимического исследования, гистологические критерии прогноза течения заболевания.
Московский научно-исследовательский онкологический институт им. П.А. Герцена — филиал ФГБУ «Национальный медицинский исследовательский радиологический центр» Минздрава России, Москва, Россия
Научно-клиническое отделение гематологической хирургии Гематологического научного центра Минздрава РФ, Москва
Патофизиологические механизмы МДС сложны и недостаточно изучены. В основе лежат выраженный апоптоз кроветворных элементов на ранних стадиях и усиленная пролиферация с утерей способности к дифференцировке клеток-предшественников на поздних стадиях заболевания. В качестве основного механизма МДС рассматривается нарастание степени апоптоза активно пролиферирующими ГСК, что ассоциируется с изменениями экспрессии в кроветворных клетках про- и антиапоптотических белков. В популяции CD34-положительных бластных клеток костного мозга больных МДС по сравнению с нормой увеличено соотношение продуктов экспрессии онкогенов c-MYC и BCL2 (соответственно способствующих увеличению апоптоза и повышающих выживаемость клеток). Важную роль в индукции апоптоза в клетках костного мозга играет система, включающая антиген Fas/Apo (CD95) и его лиганд Fas-L, которые при иммуноцитохимическом исследовании обнаруживаются на поверхностных мембранах клеток при МДС и не определяются на CD34+CD14+-клетках в норме. Имеется также корреляция между интенсивностью программированной гибели клеток эритроидного, гранулоцитарного, мегакариоцитарного ростка и стромальных клеток при МДС и экспрессией фактора некроза опухоли α (TNFα) и трансформирующего фактора роста β (TGFβ). С увеличением интенсивности апоптоза при МДС ассоциируется повышенная экспрессия белка р53 [1, 2].
Характерными клиническими симптомами МДС являются одно-, двух- и чаще трехростковая цитопении, существенно реже имеет место органомегалия и/или лимфаденопатия 3. Эта группа заболеваний привлекает к себе внимание еще с середины прошлого века. В последние годы классификация МДС постоянно совершенствуется, что обусловлено появлением новых данных о биологическом поведении входящих в него форм и совершенствованием диагностических возможностей. Последняя классификация, разработанная группой экспертов ВОЗ, была предложена в 2008 г. [6, 7]. В ней в отличие от предыдущих, базировавшихся в основном на данных гемо- и миелограммы, учитываются результаты цитогенетических исследований и в соответствии с этим выделено уже 8 вариантов МДС.
Классификация МДС (ВОЗ, 2008):
— рефрактерная анемия (РА);
— РА с ринг-сидеробластами;
— РА с мультилинейной дисплазией;
— РА с мультилинейной дисплазией и ринг-сидеробластами;
— РА с мультилинейной дисплазией и избытком бластов;
— РА с изолированной делецией 5q;
— МДС у детей (РА в детском возрасте).
В отличие от предыдущих классификаций в последней снижен уровень бластных клеток в костном мозге с 30 до 20%, при котором уже диагностируется трансформация МДС в острый лейкоз.
В соответствии с этой классификацией диагностика МДС до сих пор основывается на данных цитологического исследования периферической крови и/или костного мозга и наличии цитогенетических поломок.
По мере изучения МДС стали появляться работы о гистологической диагностике этого заболевания на основании исследования трепанобиоптатов костного мозга (ТБКМ). Однако и до последнего времени их гистологическая верификация вызывает большие трудности [8, 9].
В отличие от цитологического исследования периферической крови или костного мозга гистологическое исследование ТБКМ более точно позволяет оценить клеточность костного мозга, соотношение и локализацию клеток различных ростков гемопоэза, состояние стромы, васкуляризацию костного мозга, наличие реактивных изменений в виде лимфоидной гиперплазии, в том числе с формированием реактивных лимфоидных узелков, наличия плазматических клеток, гистиоцитов, макрофагов, тучных клеток, нарушения обмена железа.
В связи с этим на основании анализа более 1000 ТБКМ у больных с МДС, обследованных до начала терапии, и данных литературы мы сочли возможным предложить разработанный нами алгоритм гистологического исследования ТБКМ при МДС.
Алгоритм исследования трепанобиоптатов костного мозга при МДС (гистологические параметры оценки ТБКМ):— клеточность костного мозга;
— соотношение клеток гранулоцитарного и эритроидного ростков;
— локализация клеток различных ростков гемопоэза;
— отсутствие или наличие ALIP;
— наличие или отсутствие клеток-предшественников CD34-позитивных;
— наличие или отсутствие фиброза;
— наличие лимфоидной гиперплазии;
— наличие моноцитарно-гистиоцитарной пролиферации;
— наличие тучных клеток;
При МДС в ТБКМ чаще выявляется гиперплазия костного мозга (гиперпластический вариант) (рис. 1).МДС. 




Гипопластический вариант представляет большие трудности в диагностике, при этом надо проводить дифференциальную диагностику в первую очередь с апластической анемией и гипопластическим вариантом острого лейкоза [10]. Нередко для их дифференциации необходимо динамическое исследование ТБКМ в сопоставлении с клиническими и цитогенетическими данными. В отличие от МДС при апластической анемии мегакариоциты полностью отсутствуют или их количество минимальное, в них отсутствуют признаки дисплазии. Дифференциация с гипопластическим вариантом острого лейкоза возможна в основном только с привлечением иммуногистохимического (ИГХ) исследования.
В отличие от цитологических препаратов только ТБКМ позволяют охарактеризовать локализацию клеток гемопоэза. Это особенно важно для атипичной локализации клеток-предшественников миелопоэза, так называемый ALIP (рис. 6). 

В гистологических препаратах ТБКМ в отличие от цитологических препаратов костного мозга можно охарактеризовать состояние стромы, что в первую очередь касается фиброзных изменений, степени их выраженности (рис. 8). 
Гистологическое исследование костного мозга, особенно с использованием ИГХ-исследования, позволяет оценить выраженность ангиогенеза (рис. 9). 
По нашим данным, примерно в 50% случаев МДС в ТБКМ имеет место лимфоидная гиперплазия разной степени выраженности. В ряде случаев она бывает выражена столь значительно, что возникает необходимость проведения дифференциальной диагностики с лимфопролиферативными заболеваниями, в частности Т-клеточной природы, которые нередко протекают с цитопеническим синдромом и картиной гипоплазии костного мозга, часто сопровождаемой вторичным МДС. В таких случаях дифференциальная диагностика возможна только с привлечением иммуногистохимических методов исследования.
В ряде работ, в том числе и наших исследованиях, показано, что в костном мозге при МДС имеет место увеличение CD8-положительных цитотоксических Т-лимфоцитов, которые наряду с нарушениями в генах, определяющих клеточный цикл, транскрипционными и супрессивными факторами, нарушениями в соотношении апоптоз/пролиферация играют роль в патогенезе заболевания, подавляя дифференцировку эритроидных и гранулоцитарных предшественников 17.
В развитии цитопении при МДС также может играть определенную роль наличие в клетках костного мозга различных вирусов. По нашим данным, при ИГХ-исследовании ТБКМ в мегакариоцитах, лимфоидных клетках, клетках эритроидного и гранулоцитарного ростка выявляются вирус Эпштейна-Барр, цитомегаловирус, вирусы простого герпеса I и II типа (рис. 10). 
На основании изложенных данных мы предлагаем не только алгоритм исследования ТБКМ при МДС, но и оптимальную, на наш взгляд, панель ИГХ-исследования.
Следует отметить, что на основании ТБКМ не всегда можно верифицировать вариант МДС в соответствии с классификацией ВОЗ. Это возможно только при сочетании с клинико-лабораторными, в том числе цитогенетическими, данными. Однако на основании исследования ТБКМ можно диагностировать такой вариант, как 5q-синдром, для которого характерны гиперплазия и выраженная дисплазия в клетках мегакариоцитарного ростка, отсутствие изменений или минимально выраженные изменения в эритроидном и гранулоцитарном ростке. При таких вариантах МДС, как 7q, нарушениях в 8-й, 20-й и других хромосомах характерных гистологических изменений не найдено. Также имеются довольно характерные гистологические изменения при рефрактерной анемии с мультилинейной дисплазией, проявляющиеся снижением количества клеток гранулоцитарного ростка, задержкой их созревания вплоть до появления бластных клеток, которые могут располагаться не только эндостально. Для этого варианта также характерен выраженный неоангиогенез. При этом варианте в ТБКМ отмечается увеличение по сравнению с нормой количества эндотелиальных клеток, аналогичное выявляемому при остром миелобластном лейкозе.
На основании собственных и литературных данных мы выделили ряд гистологических параметров, влияющих на прогноз заболевания. В международной прогностической счетной системе при прогнозировании течения заболевания, в том числе трансформации в острый лейкоз, придается значение гистологическому исследованию костного мозга, в частности такому гистологическому показателю, как ALIP. Наличие последнего указывает на возможную эволюцию процесса в сторону острого лейкоза [19, 20]. Ряд исследователей считают, что ALIP и процент идентифицированных иммуногистохимически CD34-положительных клеток является важнейшим прогностически значимым признаком в разных группах риска при МДС. Помимо этих параметров, прогностическое значение придается фиброзу, который рассматривается как неблагоприятный фактор. Ниже приведены наиболее значимые прогностически неблагоприятные гистологические признаки, которые можно выявить в ТБКМ при МДС.
Гистологические прогностические критерии при МДС по данным трепанобиоптатов костного мозга:
— фиброз костного мозга;
— увеличение количества CD8-позитивных Т-клеток.
Как уже отмечалось, при МДС, особенно его гипопластическом варианте, необходимо проводить дифференциальную диагностику с такими заболеваниями, как апластическая анемия, гипопластический вариант острого лейкоза, а также с постмедикаментозными цитопениями. Нередко приходится проводить дифференциальную диагностику с такой группой заболеваний, как МДС/МПЗ (миелопролиферативные заболевания) [21, 22], а также вторичными МДС, которые могут сопровождать другие заболевания системы крови, в том числе специфическое поражение костного мозга при лимфомах, или быть обусловлены предшествующей полихимиотерапией.
В последние годы рядом исследователей выявлена группа больных, у которых изменения в крови и костном мозге не укладываются в диагностические критерии МДС, разработанные классификацией ВОЗ. Гематологические нарушения у них проявлялись длительной одно-, би- или панцитопенией периферической крови или умеренным цитопеническим синдромом с наличием 10% и более диспластически измененных клеток в разных линиях гемопоэза в костном мозге при отсутствии интеркуррентных заболеваний или циторедуктивной терапии. Для обозначения этих состояний предложены термины: «идиопатическая цитопения неопределенного значения (ИЦНЗ)» и «идиопатическая дисплазия неопределенного значения (ИДНЗ)».
ИДНЗ свойственна пациентам молодого возраста.
В периферической крови отсутствует или умеренно выражен цитопенический синдром с макроцитозом эритроцитов и псевдопельгеровской аномалией в лейкоцитах. Клеточность кроветворной ткани варьирует, среди клеток разных линий гемопоэза определяется не менее 10% диспластически измененных клеток. Кариологические нарушения минимальные, не строго специфичны для МДС и в части наблюдений совсем не выявляются.
ИЦНЗ и ИДНЗ рассматриваются как предфаза МДС. Дифференциация этих нарушений невозможна на гистологическом уровне без учета данных клинико-лабораторных исследований. В то же время сочетания морфологических особенностей ИЦНЗ и ИДНЗ в сопоставлении с данными клиники и кариологии являются основанием для диагноза одного из вариантов МДС. Каждый из вышеперечисленных вариантов может эволюционировать в типичный МДС. Латентный период трансформации в МДС, а также в МДС/МПЗ или острый миелобластный лейкоз может быть продолжительным, в частности, потому что патологический клон при ИЦНЗ в течение ряда лет может продуцировать лишь минимальную популяцию патологических клеток, и может ускоряться с появлением новых генетических поломок. В связи с этим исследование костномозгового кроветворения у больных с подозрением на МДС должны проводиться в динамике с одновременным исследованием кариотипа 24.
Основываясь на вышеизложенном хочется подчеркнуть крайнюю трудность диагностики МДС как клиницистами, так и врачами-патоморфологами. В связи с этим мы сочли возможным предложить алгоритм исследования ТБКМ больных с предполагаемым диагнозом МДС, в котором предусмотрены не только характерные гистологические особенности, включающие оценку клеточности костного мозга, изменения в соотношении и в каждом ростке гемопоэза, выраженность диспластических изменений, топографию клеток разных ростков гемопоэза, а также стромальные реакции. Несмотря на это, формирование окончательного диагноза МДС невозможно без учета данных клинических и цитогенетических исследований.
